法律案新旧対照条文 (55 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/topics/bukyoku/soumu/houritu/217.html |
| 出典情報 | 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律案 成立(5/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第六十八条の十五 (略)
2~4 (略)
より、その成果を厚生労働大臣に報告しなければならない。
2・3 (略)
(機構による感染症定期報告に係る情報の整理及び調査の実施)
第六十八条の十五 (略)
2~4 (略)
的に報告しなければならない。
2・3 (略)
(機構による感染症定期報告に係る情報の整理及び調査の実施)
第六十八条の二十五 (略)
2~4 (略)
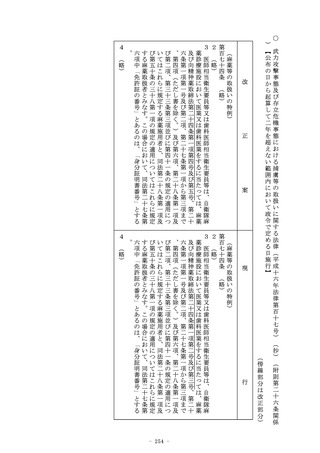
(生物由来製品に関する感染症定期報告)
第六十八条の二十四 生物由来製品の製造販売業者、外国製造医薬
品等特例承認取得者又は外国製造医療機器等特例承認取得者は、
厚生労働省令で定めるところにより、その製造販売をし、又は第
十九条の二若しくは第二十三条の二の十七の承認を受けた生物由
来製品又は当該生物由来製品の原料若しくは材料による感染症に
関する最新の論文その他により得られた知見に基づき当該生物由
来製品を評価し、その成果を厚生労働大臣に定期的に報告しなけ
ればならない。
2・3 (略)
(機構による感染症評価報告に係る情報の整理及び調査の実施)
第六十八条の二十五 (略)
2~4 (略)
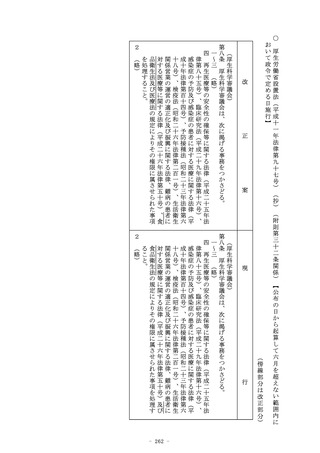
(立入検査等)
第六十九条 厚生労働大臣又は都道府県知事は、医薬品、医薬部外
品、化粧品、医療機器若しくは再生医療等製品の製造販売業者若
しくは製造業者、医療機器の修理業者、第十八条第五項、第二十
三条の二の十五第五項、第二十三条の三十五第五項、第六十八条
の五第四項、第六十八条の七第六項若しくは第六十八条の二十二
第六項の委託を受けた者又は第八十条の六第一項の登録を受けた
者(以下この項において「製造販売業者等」という。)が、第十
二条の二、第十三条第五項若しくは第六項(これらの規定を同条
(生物由来製品に関する感染症評価報告)
第六十八条の二十四 生物由来製品の製造販売業者、外国製造医薬
品等特例承認取得者又は外国製造医療機器等特例承認取得者は、
厚生労働省令で定めるところにより、その製造販売をし、又は第
十九条の二若しくは第二十三条の二の十七の承認を受けた生物由
来製品又は当該生物由来製品の原料若しくは材料による感染症に
関する最新の論文その他により得られた知見に基づき当該生物由
来製品を評価し、厚生労働省令で定めるところにより、その成果
を厚生労働大臣に報告しなければならない。
2・3 (略)
(立入検査等)
第六十九条 厚生労働大臣又は都道府県知事は、医薬品、医薬部外
品、化粧品、医療機器若しくは再生医療等製品の製造販売業者若
しくは製造業者、医療機器の修理業者、第十八条第五項、第二十
三条の二の十五第五項、第二十三条の三十五第五項、第六十八条
の五第四項、第六十八条の七第六項若しくは第六十八条の二十二
第六項の委託を受けた者又は第八十条の六第一項の登録を受けた
者(以下この項において「製造販売業者等」という。)が、第十
二条の二、第十三条第五項若しくは第六項(これらの規定を同条
- 53 -