法律案新旧対照条文 (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/topics/bukyoku/soumu/houritu/217.html |
| 出典情報 | 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律等の一部を改正する法律案 成立(5/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
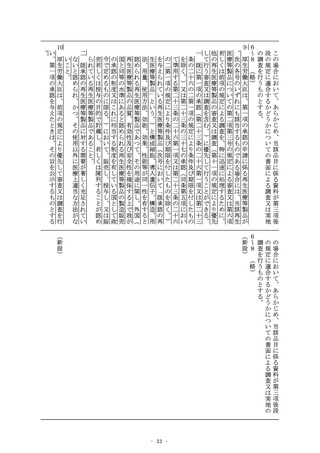
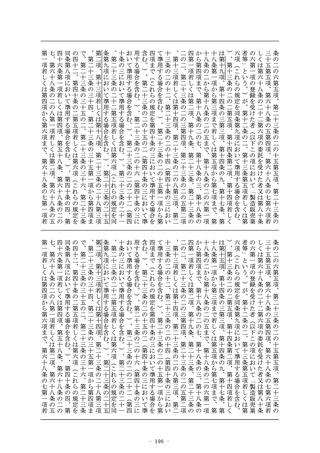
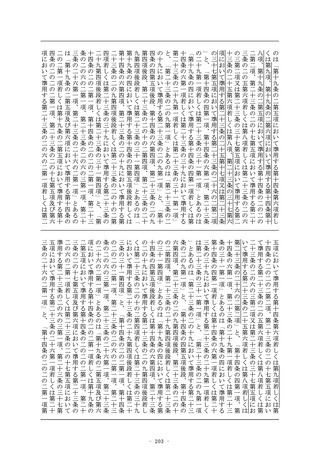
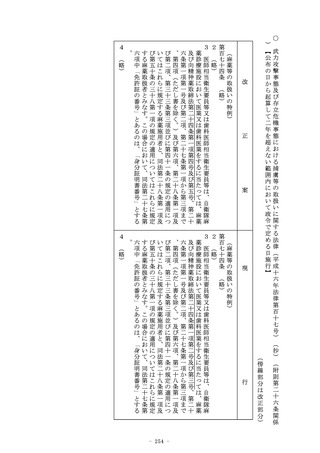
する全ての製造所(当該医療機器又は体外診断用医薬品の製造
工程のうち同項第二号に規定する厚生労働省令で定めるものの
みをするものを除く。以下この号において同じ。)が前号に掲
げる医療機器又は体外診断用医薬品を製造する製造所(当該承
認を受けようとする者又は当該承認を受けた者が製造販売をし
、又は製造販売をしようとする医療機器又は体外診断用医薬品
の製造工程と同一の製造工程が、当該製造所において、同号に
掲げる医療機器又は体外診断用医薬品の製造工程として行われ
ている場合に限る。)であるものに限る。)
2 前項の基準適合証の有効期間は、前条第六項に規定する政令で
定める期間とする。
3 (略)
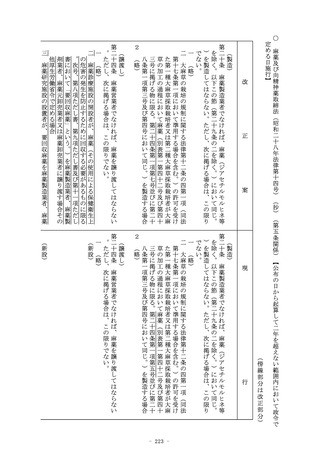
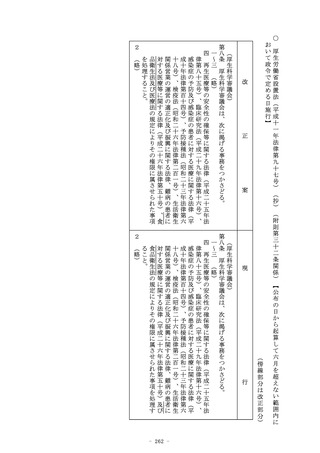
(条件付承認)
第二十三条の二の六の二 第二十三条の二の五の承認の申請者が製
造販売をしようとする物が、次の各号のいずれにも該当する医療
機器又は体外診断用医薬品である場合には、厚生労働大臣は、同
条第二項(第三号イ及びロに係る部分に限る。)及び第十二項の
規定にかかわらず、薬事審議会の意見を聴いて、当該医療機器又
は体外診断用医薬品の品質、有効性及び安全性に関する調査とし
て厚生労働省令で定める調査の実施を条件とするほか、適正な使
用の確保のために必要な措置の実施その他の必要な条件を付して
その品目に係る同条の承認を与えることができる。
一 申請に係る医療機器又は体外診断用医薬品が希少疾病用医療
機器若しくは希少疾病用医薬品、先駆的医療機器若しくは先駆
的医薬品又は特定用途医療機器若しくは特定用途医薬品その他
の医療上特にその必要性が高いと認められるものであること。
二 申請に係る効果又は性能を有すると合理的に予測できるもの
であること。
医療機器にあつては、申請に係る効果又は性能に比して著し
三
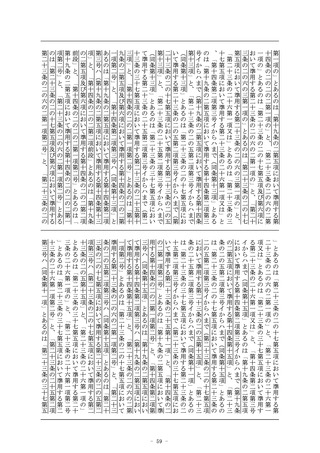
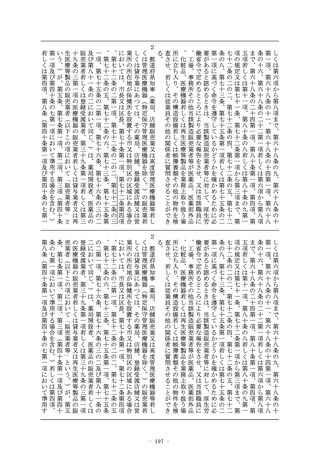
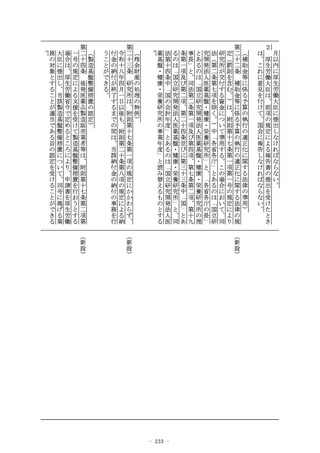
区分に属するもの(当該医療機器又は体外診断用医薬品を製造
する全ての製造所(当該医療機器又は体外診断用医薬品の製造
工程のうち同項第二号に規定する厚生労働省令で定めるものの
みをするものを除く。以下この号において同じ。)が前号に掲
げる医療機器又は体外診断用医薬品を製造する製造所(当該承
認を受けようとする者又は当該承認を受けた者が製造販売をし
、又は製造販売をしようとする医療機器又は体外診断用医薬品
の製造工程と同一の製造工程が、当該製造所において、同号に
掲げる医療機器又は体外診断用医薬品の製造工程として行われ
ている場合に限る。)であるものに限る。)
2 前項の基準適合証の有効期間は、前条第七項に規定する政令で
定める期間とする。
3 (略)
(新設)
- 22 -