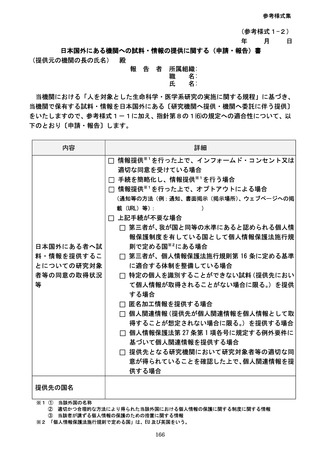
参考資料3-2:人を対象とする生命科学・医学系研究に関する倫理指針 ガイダンス (98 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58031.html |
| 出典情報 | 生命科学・医学系研究等における個人情報の取扱い等に関する合同会議(第11回 5/22)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
⑷
既存試料・情報の提供のみを行う者等の手続
既存試料・情報の提供のみを行う者等は、⑶の手続に加えて、次に掲げる全ての要件
を満たさなければならない。
ア 既存試料・情報の提供のみを行う者が所属する機関の長(以下「所属機関の長」と
いう。)は、既存試料・情報の提供が適正に行われることを確保するために必要な体
制及び規程(試料・情報の取扱いに関する事項を含む。)を整備すること
イ 既存試料・情報の提供のみを行う者は、⑶ア(ア)又はイ(ア)①、②(ⅰ)若しくは(イ)に
より既存試料・情報の提供を行う場合、その提供について所属機関の長に報告するこ
と
ウ 既存試料・情報の提供のみを行う者は、⑶ア(イ)若しくは(ウ)又はイ(ア)②(ⅱ)、(ウ)若
しくは(エ)により既存試料・情報を提供しようとするときは、倫理審査委員会の意見
を聴いた上で、所属機関の長の許可を得ていること
エ 既存試料・情報の提供のみを行う者が⑶ア(イ)若しくは(ウ)又はイ(ウ)若しくは(エ)に
より既存試料・情報の提供を行う場合には、所属機関の長は、当該既存試料・情報の
提供に関する情報を研究対象者等に通知し、又は研究対象者等が容易に知り得る状
態に置かれることを確保すること
1
第8の1⑷の規定は、既存試料・情報の提供のみを行う者等の手続について定めたもの
である。既存試料・情報の提供のみを行う者等が、他の研究機関に既存試料・情報を提供
する場合、第8の1⑴の新規取得の場合における研究協力機関とは異なり、提供元となる
当該者が提供に係るインフォームド・コンセント等の手続を実施する必要がある。
2
アの「既存試料・情報の提供が適正に行われることを確保するために必要な体制及び規
程(試料・情報の取扱いに関する事項を含む。)を整備」に関しては、あらかじめ当該機
関の長が他の研究機関への提供時の取扱いや手続等(機関の長へ報告するための方法や試
料・情報の提供に関する記録の保存方法等)に関する規程を定めることが考えられる。な
お、試料・情報の提供に関する記録については、第8の3の解説を参照。
3
イに関し、既存試料・情報の提供に際し、インフォームド・コンセントの手続等が不要
な場合(前記第8の1⑶の解説を参照。)には、その提供について所属機関の長に報告す
る必要がある。
4
ウに関し、既存試料・情報の提供に際し、インフォームド・コンセントの手続等が必要
な場合(前記第8の1⑶の解説を参照。)には、インフォームド・コンセントの手続、説
明内容又は通知若しくは研究対象者等が容易に知り得る状態に置くべき事項について倫
理審査委員会の意見を聴いた上で、既存試料・情報の提供のみを行う機関の長の許可を得
ている必要がある。ウの「倫理審査委員会の意見を聴いた上で」について、既存試料・情
報の提供のみを行う者は、必要に応じて、提供先その他の機関に設置された倫理審査委員
会に審査を依頼することもできる。既存試料・情報の提供の適否について倫理審査委員会
95