参考資料3-2:人を対象とする生命科学・医学系研究に関する倫理指針 ガイダンス (117 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58031.html |
| 出典情報 | 生命科学・医学系研究等における個人情報の取扱い等に関する合同会議(第11回 5/22)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
る者に提供する場合はその旨も併せて説明することとする。
なお、試料・情報の提供に関する記録の作成方法等については、不適切と考えられる試
料・情報の流通が発生した際に事後的に流通経路を追跡することができるように記録を残
すという趣旨であるため、一義的には研究対象者等に説明する必要はない。
5
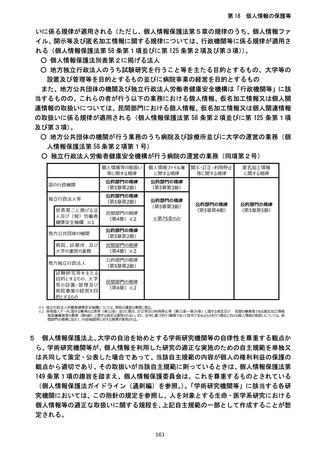
⑪の規定に関して、研究対象者等に係る個人情報を他の研究機関に提供するとき(委託
や共同利用に伴って個人情報を提供する場合を含む。)は、提供する個人情報の内容、提
供を受ける研究機関の名称、当該研究機関における利用目的、提供された個人情報の管理
について責任を有する者の氏名又は名称を含めて説明する必要がある。試料に係る情報の
取扱いについても含む。なお、共同研究機関に提供された個人情報について、研究対象者
等から、個人情報保護法に規定される開示、訂正等及び利用停止等に関する求めがなされ
たときは、該当する個人情報を保有している全ての共同研究機関において対応が必要とな
る場合がある。
6
⑫の規定に関して、研究に用いられる情報の管理について、クラウドサービスを利用す
る場合には、クラウドサービス提供事業者の名称及び情報が保存されるサーバが所在する
国の名称について説明することが望ましい。また、この場合においては、これらの内容に
変更が生じた場合の公表方法(場所等)についても予め説明しておくこと。
7
⑭の規定に関しては、第 10 の1の解説を参照。
8
⑮の規定に関して、他の研究対象者等の個人情報や研究者等の知的財産権の保護等の観
点から回答ができないことがある場合は、その旨を説明する必要がある。
9
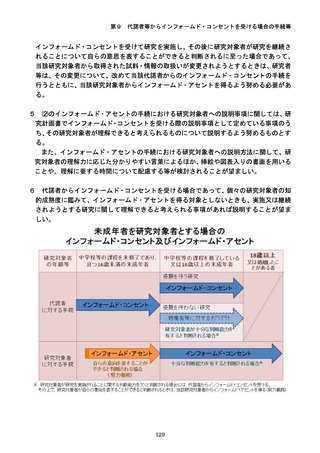
⑱の規定に関して、説明を要する「他の治療方法」は、原則として既に確立した治療法
に限られるが、必要に応じて他の研究への参加等について説明してもよい。また、研究の
内容によっては、積極的な治療以外の選択肢(緩和ケアや経過観察等)についても説明を
要する「他の治療方法等」に含まれる。
10
㉑の規定に関して、同意を受ける時点では特定されない研究を将来的に行う可能性があ
る場合(別の研究を行う場合のほか、先行する研究を計画変更する場合を含む。)は、先
行する研究に係るインフォームド・コンセントの手続において、将来の研究への利用の可
能性を含め、少なくとも②、③、④、⑥、⑫及び⑬について、想定される内容を可能な限
り説明するものとする。「実施される研究及び提供先となる研究機関に関する情報を研究
対象者等が確認する方法」とは、例えば、電子メールや文書による通知、ホームページの
URL、電話番号等が考えられる。
研究対象者等から、将来の研究への利用について同意を受けている場合は、第8の1⑵
ア(ウ)及びイ(ウ)並びに⑶ア(イ)及びイ(ウ)の規定により、研究対象者等に情報を通知し、又は
研究対象者等が容易に知り得る状態に置き、同意を撤回できる機会を保障することにより、
114