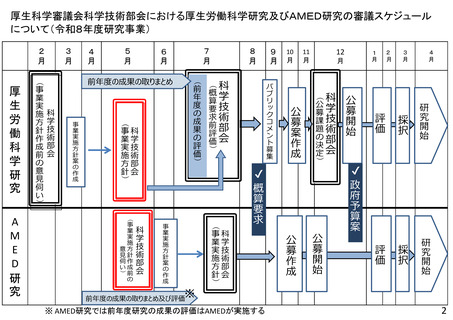
【資料2】令和8年度研究事業実施方針作成のための意見伺い(AMED研究) (42 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_57788.html |
| 出典情報 | 厚生科学審議会 科学技術部会(第144回 5/14)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
研究事業名
主管部局・課室名
AMED担当部・課名
省内関係部局・課室名
再生・細胞医療・遺伝子治療 PJ
再生医療等実用化研究事業
医政局研究開発政策課
再生・細胞医療・遺伝子治療事業部 再生医療研究開発課
健康・生活衛生局難病対策課、健康・生活衛生局がん・疾病対策課
当初予算額(千円)
Ⅰ
令和4年度
2,712,244
令和5年度
2,712,244
令和6年度
2,712,244
実施方針の骨子
1 研究事業の概要
(1)研究事業の目的・目標
【背景】
再生医療等は、これまでの治療では対応困難であった疾患に対する新たな治療法とな
り得るものであり、最新の再生医療を世界に先駆けて実用化することを目的として、倫
理性及び科学性が十分に担保された臨床研究や医師主導治験等を支援する必要がある。
また、令和6年3月5日に「再生医療等の安全性の確保等に関する法律及び臨床研究法
の一部を改正する法律案」を閣議決定したところであるが、法案が成立した場合は in
vivo 遺伝子治療も法の対象となり、これまでの細胞・細胞医療に加えて普及の促進を図
っていくこととなる。
【事業目標】
再生医療等に関して、基礎から臨床段階まで切れ目なく一貫した支援を行うととも
に、高品質な臨床用 iPS 細胞、体性幹細胞、in vivo 遺伝子治療等の安定的な供給に向
けた取組等、実用化を見据えた基盤を整備する。実用化の道筋が明確な研究を支援し、
再生医療等製品等の治験・先進医療に着実に繋げる。また、iPS 細胞等を用いた病態解
明、創薬研究及び創薬支援ツール等の産業化に向けた汎用性のある製造技術の基盤の開
発・整備により、新薬開発の効率性の向上を目指す。
【研究のスコープ】
・品質・安全性の確保のための研究
・治療方法探索のための研究
・実用化を見据えた製法開発に関する研究
・産学連携による研究
・臨床研究等の実施中に生じた課題解決のための研究
・多能性幹細胞・体性幹細胞等を利用した創薬応用のための研究
・再生医療等技術の効率化のための研究
・再生医療等技術の国際展開のための研究
【期待されるアウトプット】(※)
「再生・細胞医療・遺伝子治療プロジェクト」に基づき、文部科学省事業によって非
臨床段階から臨床段階へ移行した課題について、切れ目なく支援を行い、臨床研究又は
治験に移行する課題の拡大、iPS 細胞等を用いた病態解明等を目指す。
【令和2年度~令和6年度までの KPI】
治験に移行した研究課題数:14 件
38