【資料1-1】令和8年度研究事業実施方針(AMED研究)(案) (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59644.html |
| 出典情報 | 厚生科学審議会 科学技術部会(第145回 7/16)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
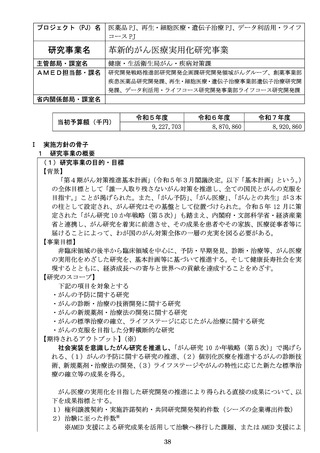
【概要】生殖・妊娠期から老年期までのライフコースに着目した医薬品等の研究開発に
おいては、それぞれの段階に特有の課題を考慮することが求められている。本研究で
は、リアルワールドデータ等を活用した周産期の薬物治療と児への影響評価にかかわ
る基盤整備や安全性評価研究を実施する。また、小児向けの治験における患者負担の
軽減に資する微量採血手法の実施に関する検討とガイドライン等の整備を実施する。
【成果の活用】妊婦および児の安全性評価研究の強化により、周産期医療における新規
医薬品開発の促進と市販後の医薬品リスク低減に寄与する。また小児治験の効率的な
実施により、緊縛の課題となっている小児用医薬品のドラッグラグ・ロスの解消への
貢献が期待される。
Ⅱ
参考
1 研究事業と各戦略(新しい資本主義のグランドデザイン及び実行計画・フォローアップ、
成長戦略、骨太方針、統合イノベーション戦略、健康・医療戦略)との関係
【統合イノベーション戦略 2025】(令和7年6月6日閣議決定)
別添 Society5.0 の実現に向けた科学技術・イノベーション政策
4.官民連携により分野別先約の推進
(戦略的に取り組むべき応用分野)(一部抜粋)
医療分野の研究開発の環境整備として、橋渡し研究支援拠点や臨床研究中核病院におけ
る体制や仕組みの整備、生物統計家などの専門人材及びレギュラトリーサイエンスの専
門家の育成・確保、研究開発におけるレギュラトリーサイエンスの普及・充実等を推進
する。
【健康・医療戦略】(令和7年 2 月 18 日閣議決定)
2.3-2 社会的課題の解決に資する研究開発の推進(一部抜粋)
新規モダリティ製品等に対応するレギュラトリーサイエンス(Regulatory Science)研
究を推進する
4. 具体的施策
4.1 世界最高水準の医療の提供に資する医療分野の研究開発の推進
(4) 8つの統合プロジェクト 医薬品プロジェクト
国民に最新の医薬品を速やかに届けるため、創薬標的の探索から臨床研究・治験に至る
まで、幅広い研究開発を行う。また、アカデミアやスタートアップに対する絶え間ない
シーズ開発支援により、革新的な新薬の創出を目指す。さらに、創薬研究開発に必要な
高度解析機器・技術支援基盤及び大規模生産を見据えた製造技術基盤の構築や創薬エコ
システムを構成する人材の育成・拡充など、研究開発力の向上に向けた環境整備に取り
組み、持続可能な創薬力の強化を目指す。
4.2
研究開発の環境の整備及び成果の普及等
○ レギュラトリーサイエンス、国際規制調和の推進
・ 国際的な規制調和を前提とした医薬品等の品質、有効性及び安全性に関する研究の
支援、最新動向の把握や専門的知識の向上等に精通する審査員の育成・確保等を通じて、
研究開発におけるレギュラトリーサイエンスを普及・充実させる。
・ 新規モダリティ等に対する評価系の開発等の研究推進と合わせて、規制当局が新規
モダリティの国際的な開発動向を把握し、レギュラトリーサイエンス研究によりその特
徴を踏まえたガイドラインを作成し、国際的な規制調和の場である ICH や国際薬事規
制当局連携組織(International Coalition of Medicines Regulatory Authorities:
16