会議資料 (431 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
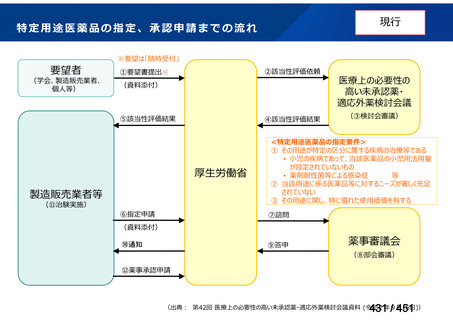
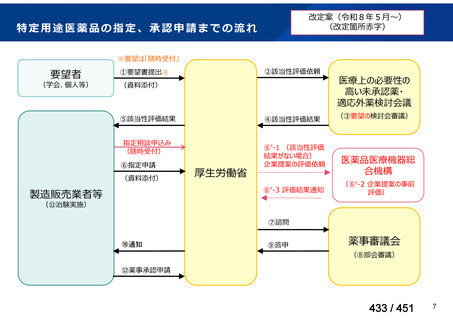
特定用途医薬品の指定、承認申請までの流れ
※要望は「随時受付」
要望者
(学会、製造販売業者、
個人等)
②該当性評価依頼
①要望書提出※
(資料添付)
⑤該当性評価結果
④該当性評価結果
厚生労働省
製造販売業者等
(⑪治験実施)
⑥指定申請
医療上の必要性の
高い未承認薬・
適応外薬検討会議
(③検討会審議)
<特定用途医薬品の指定要件>
① その用途が特定の区分に属する疾病の治療等である
• 小児の疾病であって、当該医薬品の小児用法用量
が設定されていないもの
• 薬剤耐性菌等による感染症
等
② 当該用途に係る医薬品等に対するニーズが著しく充足
されていない
③ その用途に関し、特に優れた使用価値を有する
⑦諮問
(資料添付)
⑨答申
⑩通知
薬事審議会
(⑧部会審議)
⑫薬事承認申請
431 / 451
(出典: 第42回 医療上の必要性の高い未承認薬・適応外薬検討会議資料 (令和2年9月16日))
5