会議資料 (294 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
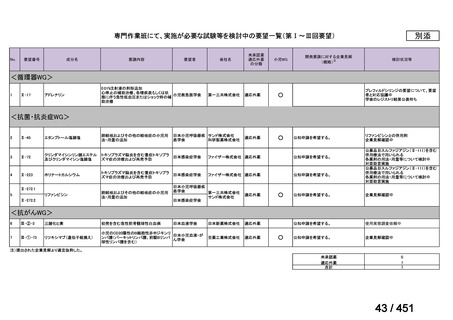
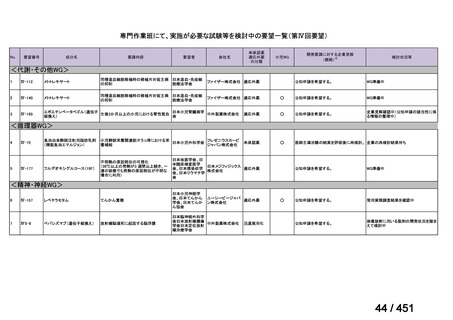
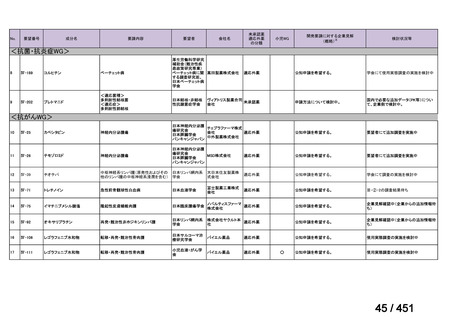
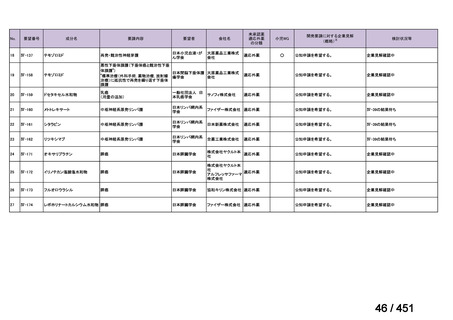
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
が承認され、15 年以上の日本人の安全性情報が集積されている。また、既報の代表的な論
文における有害事象の発現状況は「5.要望内容に係る国内外の公表文献・成書等につい
て(1)無作為化比較試験、薬物動態試験等の公表論文としての報告状況」の項に記載の
とおりであり、国内外における新たな安全性上の懸念は認められていない。なお、国内外
の臨床試験成績等で認められた主な有害事象は、現行の添付文書において副作用として注
意喚起されている事象、または移植や併用薬等のその他の要因に関連して認められる事象
であると考えられる。
以上より、適応疾患を問わず同種造血幹細胞移植の前治療に対して本剤を使用する際の安
全性については、同種造血幹細胞移植に十分な知識・経験を持つ医師のもとで、本剤の既
承認の効能又は効果と同様の適切な安全対策が講じられる場合には、既知の安全性情報の
範囲内で使用可能であると考える。
(3)要望内容に係る公知申請の妥当性について
上記(1)及び(2)での有効性及び安全性の総合評価、日欧米等の診療ガイドライン及び
教科書の記載内容、本邦及び海外臨床試験成績等から、本要望に関して公知申請を行うこ
とは妥当と考える。
8.効能・効果及び用法・用量等の記載の妥当性について
(1)効能・効果について
日欧米等の診療ガイドライン及び教科書の記載内容において、同種造血幹細胞移植の前治
療(MAC 及び RIC/NMA)としてのフルダラビンの投与が標準治療の一つとして推奨され
ている。ことから、疾患名を問わず、
「同種造血幹細胞移植の前治療」とすることが妥当と
考える。
また、国内外の臨床試験等において同種造血幹細胞移植の前治療としての本剤の使用実態
が確認できた疾患以外も含め、本剤の効能又は効果を、適応疾患を問わず、
「同種造血幹細
胞移植の前治療」と設定することを踏まえ、効能又は効果に関連する注意において以下の
注意喚起を設定する予定である。
本剤の投与にあたっては、国内外の最新のガイドライン等を参考に、適応患者の選択
を行うこと。
(2)用法・用量について
日欧米等の診療ガイドライン及び教科書に記載されたフルダラビンリン酸エステルの用
法・用量並びに本邦及び海外臨床試験における用法・用量を考慮すると、下記とすること
が妥当と考える。
「フルダラビンリン酸エステルとして、1 日量 30mg/m2(体表面積)を 6 日間連日点滴静注
(約 30 分)する。なお、患者の状態により、投与量及び投与日数は適宜減ずる。
」
52
294 / 451