会議資料 (258 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
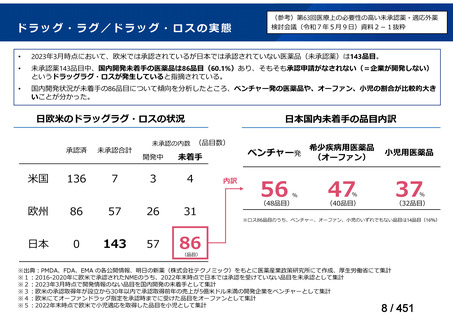
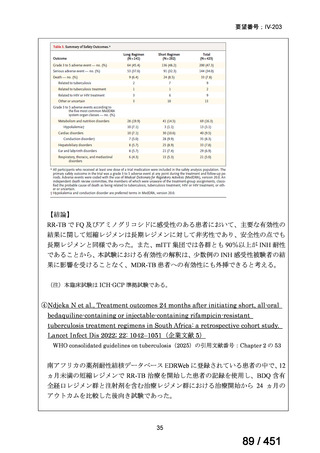
5)
Cardiac
1
1.6
0
—
1
0.8
Coagulation
2
3.1
1
1.6
3
2.4
GI, upper
20
31.3
10
16.1
30
23.8
GI, lower
13
20.3
5
8.1
18
14.3
Hepatic
21
32.8
20
32.3
41
32.5
Infection
44
68.8
31
50.0
75
59.5
Neurologic
0
—
0
—
0
—
Pulmonary
1
1.6
2
3.2
3
2.4
Renal
1
1.6
2
3.2
3
2.4
Rambaldi A, et al. Busulfan plus cyclophosphamide versus busulfan plus fludarabine as a
preparative regimen for allogeneic haemopoietic stem-cell transplantation in patients with
acute myeloid leukaemia: an open-label, multicentre, randomised, phase 3 trial. Lancet Oncol.
2015;16:1525–36.
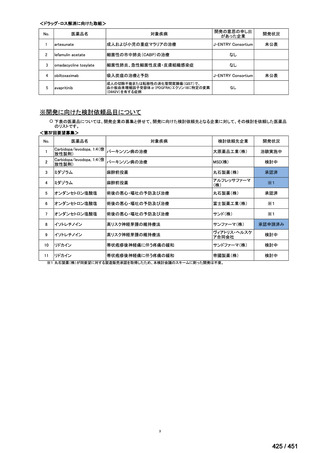
イタリアの 25 の病院移植センターとイスラエルの 1 つの病院移植センターにおい
て、急性骨髄性白血病患者を対象とした非盲検多施設共同無作為化第 III 相試験が実
施された。
対象患者は 40~65 歳で、Eastern Cooperative Oncology Group(ECOG)の全身状態
(PS)が 3 未満であり、完全寛解状態にある患者であった。患者は、Bu/Cy の静脈内
投与群と Bu/Flu の静脈内投与群に 1:1 の割合で無作為に割り付けらた。Bu/Cy 群に割
り当てられた患者は、4 日間連続して Bu0.8 mg/kg を 1 日 4 回、2 時間ずつ静脈内投与
され(-9 日目から-6 日目まで 16 回投与、総投与量 12.8 mg/kg)
、Cy は 2 日間連続し
て 1 日 60 mg/kg 投与された(-4 日目と-3 日目、総投与量 120 mg/kg)。Bu/Flu 群に割
り当てられた患者は、同量の Bu を静脈内投与され(-6 日目から-3 日目まで)、Flu は
4 日間連続して 1 日 40 mg/m 2 投与された(-6 日目から-3 日目まで、総投与量
160 mg/m2)。主要評価項目は 1 年非再発死亡率であり、これは ITT に基づいて評価さ
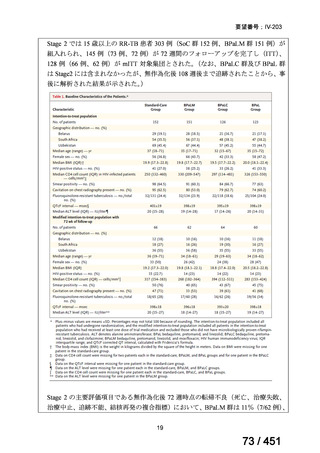
れ、安全性評価はプロトコルに準拠した集団で評価された。252 例の患者を登録し、
Bu/Cy(n=125)または Bu/Flu(n=127)を投与する群に無作為に割り付けた。追跡期
間の中央値は 27.5 か月であった。1 年無再発死亡率は、Bu/Cy 群で 17.2%(95% CI
11.6–25.4)、Bu/Flu 群で 7.9%(95% CI 4.3–14.3)であった(Gray 検定、p=0.026)
。最
も頻度が高かったグレード 3 以上の有害事象は、消化器系の有害事象(Bu/Cy 群の
121 例の患者のうち 28 例 [23%]、Bu + Flu 群の 124 例の患者のうち 26 例 [21%])
および感染症(Bu/Cy 群の 21 例 [17%]、Bu/Flu 群の 13 例 [10%] の患者に少なくと
も 1 つのイベントが認められた)であった。
高齢の急性骨髄性白血病患者において、MAC における Bu/Flu のレジメンは、Bu/Cy
のレジメンよりも移植関連死亡率が低いことが示され、強力な抗白血病作用も維持さ
16
258 / 451