会議資料 (324 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
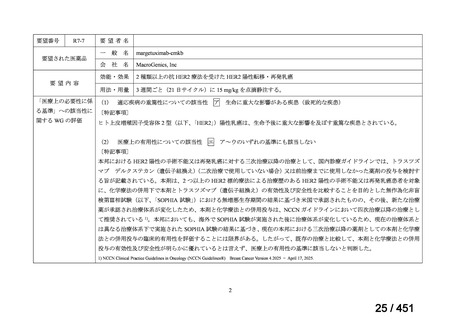
要望番号;IV-145
X 連鎖性副腎白質ジストロフィーの同種造血幹細胞移植の主要な特徴)。
3) Hematopoietic Stem Cell Transplantation to Treat Leukodystrophies: Clinical Practice Guidelines
from the Hunter’s Hope Leukodystrophy Care Network. Biol Blood Marrow Transplant.
2019;25(12): e363-e374. 3)
(2)欧米等6カ国での標準的使用状況について 米国の項に記載
4) EBMT/ESID inborn errors working party guidelines for hematopoietic stem cell transplantation
for inborn errors of immunity. Bone Marrow Transplant.2021;56:2052-62. 6)
(2)欧米等6カ国での標準的使用状況について 英国の項に記載
<日本におけるガイドライン等>
3) 造血細胞移植ガイドライン
移植前処置(第 2 版)2020 年 5 月 33)
Ⅲ.同種造血幹細胞移植の移植前処置
1.骨髄破壊的前処置(MAC)
⑵ FLU+BU4
CY の肝毒性や心毒性は、重篤な合併症をもたらす可能性がある。それらの毒性を回避
するために、CY をプリンアナログ系抗腫瘍薬のフルダラビンに置換し BU と併用する
移植前処置が開発された。
FLU は強力な免疫抑制効果に加えて、アルキル化剤との相乗効果を有している。
MAC としての FLU(25~30 mg/m2/day × 5~6 days)+ivBU(3.2 mg/kg/day × 4 days)を
本稿では FLU+BU4 と表記する。
骨髄系腫瘍に対する FLU+BU4 を用いた同種造血幹細胞移植の治療関連毒性は比較的
軽度であることが報告されている。
FLU+BU4 と BU+CY を比較する後方視的研究や前方視的研究においては、両者の治
療成績はほぼ同等であることが示されている。
一方、FLU+BU4 と BU+CY との無作為化比較試験においては、Lee らは FLU+BU4
群の生存率が劣ると報告しているが、Rambaldi らは FLU+BU4 群で有意に非再発死亡
率が低く、両者の生存率には有意差を認めないことを示している。
わが国の日常診療においては、FLU+BU4 は既に汎用されている MAC の一つである。
⑷ FLU+BU+MEL
FLU+BU4 は、進行期の骨髄系腫瘍に対する前処置として用いた際の移植後再発と、臍
帯血移植に用いた際の生着不全のリスクが高いことが問題である。Yamamoto らは、FLU
+BU4 に MEL を加えて抗腫瘍効果と免疫抑制効果を強化する前処置を開発した。非寛
解期の骨髄系腫瘍患者 51 例に対して、移植前処置として FLU(30 mg/m2/day ×6 days,
day -7~-2)+ivBU(3.2 mg/kg/day×4 days, day -7~-4)+MEL(40 mg/m2/day ×2 days,
day -3~-2)を用いた CBT を実施した。好中球生着は 90.2%で得られ、移植片の拒絶や
25
324 / 451