会議資料 (429 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
優先的な取扱い
(1)
優先相談
総合機構で実施されている対面助言等で、他の医薬品等に優先した取扱いを受けることができる
(2)
優先審査
「医療上特にその必要性が高いと認められるもの」 審査期間
に該当するため
(80%タイル)
通常の審査
特定用途
希少疾病用
12ヶ月
9ヶ月
9ヶ月
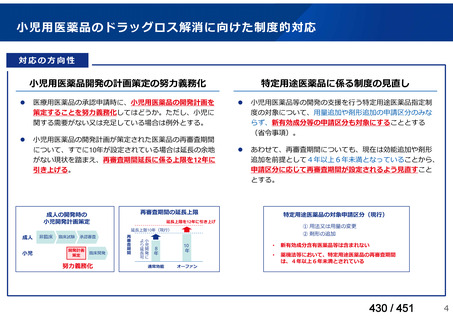
再審査期の付与
・特定用途医薬品
4年以上6年未満で厚生労働大臣が指定する期間
医療用医薬品の再審査期間について(令和2年8月31日付け薬生発0831第11号)
再審査期間の取扱いについて(令和2年8月31日付け薬生薬審発0831第16号)
資金の確保及び税制上の措置
• 特定用途医薬品等は資金の確保及び税制上の措置の対象(法第77条の3及び第77条の4)
• 対象患者数が5万人以下の特定用途医薬品等は、助成金及び税制上の措置の対象(規則第251条の5及び第251条の6)
ただし、税制上の措置は以下の要件あり
• 医薬基盤・健康・栄養研究所からの助成金の交付を受けて行う特定用途医薬品等に関する試験研究は、特別試験研究の額にかかる税
制控除制度の対象
ただし、その助成金の交付を受ける法人の常時使用従業員数が1,000人以下であることが要件
429 / 451