会議資料 (192 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
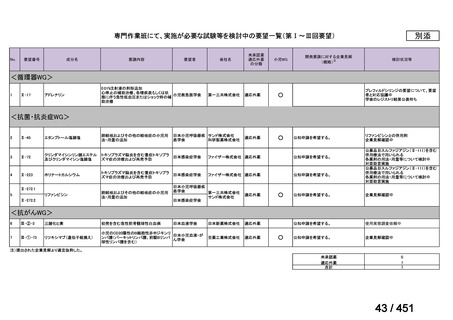
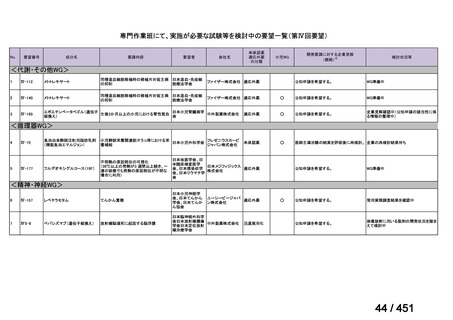
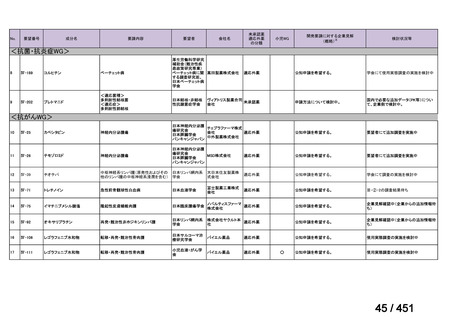
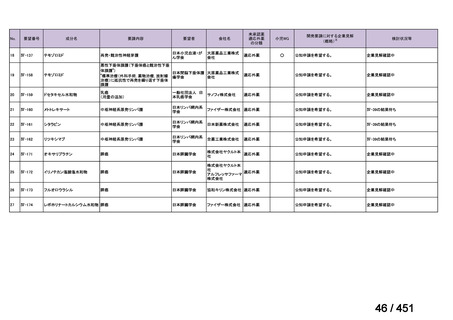
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
療について、単剤治療は禁忌であり、多剤併用レジメンでの治療が必須とされ、治
療においては各患者の服薬管理及び安全性モニタリングが必須とされる。MFLX が
本適応で承認された場合に国内では、INH 及び RFP(又はリファブチン:RBT)、
BDQ、LZD、EB、PZA、TH、DLM、CFZ、CS、SM(又は KM 又は EVM)及びプ
レトマニド(現在、国内未承認)との併用が考えられる。
18~20 ヵ月長期レジメンで使用する抗結核薬の安全性を検討した IPD メタアナ
リシス〔企業文献 24、WHO ガイドライン(2025)〕においては、MFLX は
LVFX、CFZ 及び BDQ と共に、抗結核薬の中では永続的な投与中止に繋がる
AE、及び SAE の発現頻度が低いことが示されている。
国外の成書、並びに WHO ガイドライン(2025)(企業文献 2)では、長期レジ
メン及び 9 ヵ月の BDQ を含む全経口多剤併用療法レジメンで推奨又は標準的治療
薬の FQ として LVFX 又は MFLX と設定されている。この場合、安全性の側面か
らも両剤の使用において優先順位はない。
WHO ガイドライン(2025)では FQ の選択として、LVFX 又は MFLX とある場
合、MFLX の心毒性がわずかに高い可能性から、LVFX がしばしば好まれる傾向に
はあるが、LVFX 又は MFLX のいずれの選択に関わらず、すべての患者に対して
薬剤の安全性モニタリングと管理が必要としている。
6 ヵ月 BPaLM レジメン及び 9 ヵ月 BLMZ レジメンについても、MFLX に特化し
た安全性の注意喚起はない。
以上のことから、MFLX の多剤耐性肺結核症の治療に際した安全性は、下記の
点から特段の問題はないと考えられる。
1 申請する用法・用量は、すでに承認を取得している適応症の治療に対する用
法・用量(1 日 1 回 400mg)を超えない(同一)である。また、本薬の薬物動
態に関して、臨床上問題となる民族差は認められなかった。
2 成書やガイドラインで多剤耐性肺結核症に推奨されるレジメンは、アジア(日
本以外)を含む国際共同、前向き無作為化比較試験、後ろ向き観察研究等で得
られた安全性を含むエビデンスを分析した上で推奨に至っている。
3 多剤耐性結核症への治療に対して、MFLX が単剤で使用されることはない。国
外の成書及び WHO ガイドラインにおいて MFLX を含む推奨レジメンを使用す
る場合、各患者の服薬管理及び安全性モニタリングが必須とされるが、これは
結核治療の原則でもある。FQ を含むレジメンにおいては、MFLX と LVFX の
間に使用に関する優先順位はなく、また、本剤に特化した安全性管理の注意喚
起はないことを確認した。
(3)要望内容に係る公知申請の妥当性について
MFLX は、国内外において当該効能又は効果に対して未承認である。日本人の
結核症患者に対して MFLX が使用されたデータは限られるが、多剤耐性肺結核症
138
192 / 451