よむ、つかう、まなぶ。
総-1参考1 (90 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64319.html |
| 出典情報 | 中央社会保険医療協議会 総会(第619回 10/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
5. Q & A
改訂案
5 エレビジスを構成するAAVrh74ベクターが患者以外の家族などに感染し、
第三者がセロコンバージョンする可能性はありますか?
AAVrh74ベクターへの意図しない曝露による第三者のセロコンバージョンは報告されていません。
( 体重70kg未満)
又は9.31×1015vg
( 体重70kg以上)
を単回静脈内投与
男性DMD患者に本品1.33×10 14vg/kg
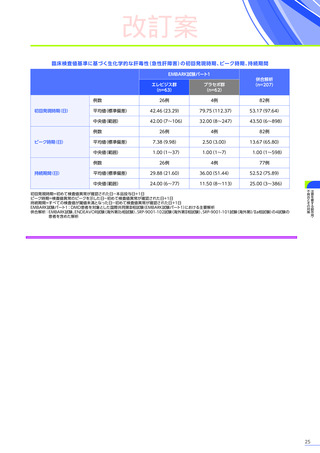
したときの唾液及び尿中の平均ベクターゲノム濃度はDay 1~2がピークで、それぞれ4.46×107~1.42×108vg/mL
および3.99×105~8.06×106vg/mLでした。糞便中の平均ベクターゲノム濃度はWeek 1がピークで、2.27×107~
2.38×10 8 vg/μgでした。いずれのコホートにおいても、唾液、糞便及び尿中のベクター排出量のピーク時から
Week 4までの減少率は99.5%を超え、4つのコホート全体で排泄物中のベクターの消失[最初に検出限界未満
(BLOD)
の検体が確認され、その後2回連続してBLODの検体が確認されることにより判定]
が認められた投与後の
期間の中央値は、唾液、尿及び糞便中でそれぞれ7.29、11.00及び25.07週間でした18)。
6 体内に遺伝子を取り込むことにより、発がん性に影響を与えることはありませんか?
ヒトにおける発がん性のリスクは低いものと考えられます。
AAVを用いた遺伝子治療を行った新生児げっ歯類において、追跡調査24カ月以内に肝細胞がんの発現が認められて
いますが、
これらの観察結果はげっ歯類特有でヒトゲノムには存在しないRIAN遺伝子座の変異等によって認められて
います66)。また、AAVを用いた遺伝子治療を行ったイヌにおいても、最長10年間の追跡調査で発がん性は認められ
ていません67)。
加えて、国内外で実施された本品の臨床試験
(EMBARK試験を含む)
の統合解析の結果、本品投与後に発がんに至っ
た症例は報告されておらず、
ヒトにおける発がん性のリスクの理論上の可能性は低いものと考えられます68)。
しかしながら、症例数や追跡期間が十分ではないことから、安全性検討事項の
「重要な不足情報」
に設定しています35)。
90
改訂案
5 エレビジスを構成するAAVrh74ベクターが患者以外の家族などに感染し、
第三者がセロコンバージョンする可能性はありますか?
AAVrh74ベクターへの意図しない曝露による第三者のセロコンバージョンは報告されていません。
( 体重70kg未満)
又は9.31×1015vg
( 体重70kg以上)
を単回静脈内投与
男性DMD患者に本品1.33×10 14vg/kg
したときの唾液及び尿中の平均ベクターゲノム濃度はDay 1~2がピークで、それぞれ4.46×107~1.42×108vg/mL
および3.99×105~8.06×106vg/mLでした。糞便中の平均ベクターゲノム濃度はWeek 1がピークで、2.27×107~
2.38×10 8 vg/μgでした。いずれのコホートにおいても、唾液、糞便及び尿中のベクター排出量のピーク時から
Week 4までの減少率は99.5%を超え、4つのコホート全体で排泄物中のベクターの消失[最初に検出限界未満
(BLOD)
の検体が確認され、その後2回連続してBLODの検体が確認されることにより判定]
が認められた投与後の
期間の中央値は、唾液、尿及び糞便中でそれぞれ7.29、11.00及び25.07週間でした18)。
6 体内に遺伝子を取り込むことにより、発がん性に影響を与えることはありませんか?
ヒトにおける発がん性のリスクは低いものと考えられます。
AAVを用いた遺伝子治療を行った新生児げっ歯類において、追跡調査24カ月以内に肝細胞がんの発現が認められて
いますが、
これらの観察結果はげっ歯類特有でヒトゲノムには存在しないRIAN遺伝子座の変異等によって認められて
います66)。また、AAVを用いた遺伝子治療を行ったイヌにおいても、最長10年間の追跡調査で発がん性は認められ
ていません67)。
加えて、国内外で実施された本品の臨床試験
(EMBARK試験を含む)
の統合解析の結果、本品投与後に発がんに至っ
た症例は報告されておらず、
ヒトにおける発がん性のリスクの理論上の可能性は低いものと考えられます68)。
しかしながら、症例数や追跡期間が十分ではないことから、安全性検討事項の
「重要な不足情報」
に設定しています35)。
90