よむ、つかう、まなぶ。
総-1参考1 (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64319.html |
| 出典情報 | 中央社会保険医療協議会 総会(第619回 10/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
改訂案
特定の背景を有する患者に関する注意
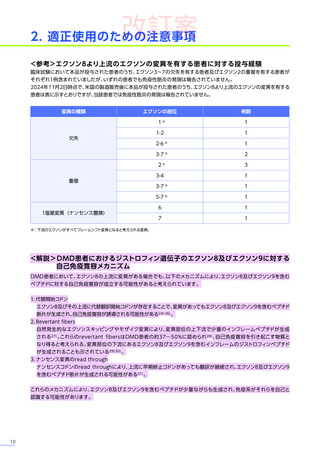
ジストロフィン遺伝子のエクソン1-17及び/又はエクソン59-71の欠失を有する患者に関する注意
ジストロフィン遺伝子のエクソン1-17及び/又はエクソン59-71の領域に欠失を有する患者さんは、重度の免疫介在性
の筋炎発現のリスクが高いおそれがあります。
⇒禁忌・禁止 p9参照
⇒筋炎 p32参照
<解説>
臨床試験
(EMBARK試験パート1)
では、エクソン1~17に変異のある患者さんは非適格として除外されています17)。
⇒臨床試験成績
p60参照
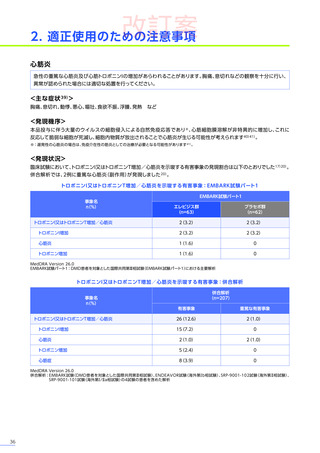
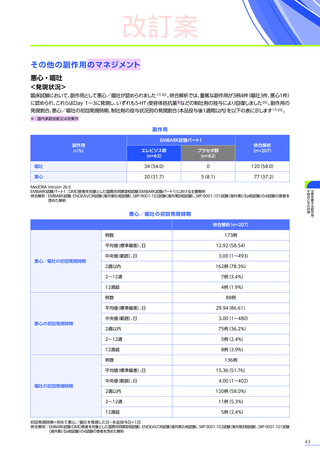
心エコーで左室駆出率が40%未満の患者さん及び症候性の心筋症を有する患者さんは、心筋炎の発現のリスクが高い
エレビジスの
投与対象の確認
心機能障害のある患者に関する注意
おそれがあります。臨床試験において、
これらの患者さんの十分なデータはありません。
⇒心筋炎 p36参照
<解説>
臨床試験(EMBARK試験パート1)
では、心エコーで左室駆出率が40%未満の患者さん及び心筋症を有する患者さんは
除外されています17)。
⇒臨床試験成績
p60参照
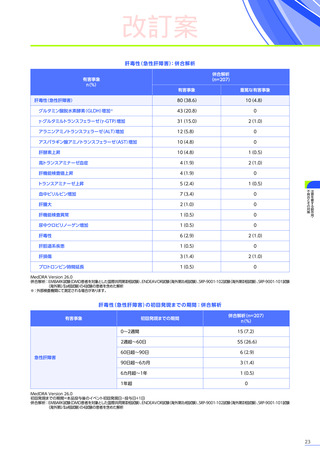
肝機能障害患者に関する注意
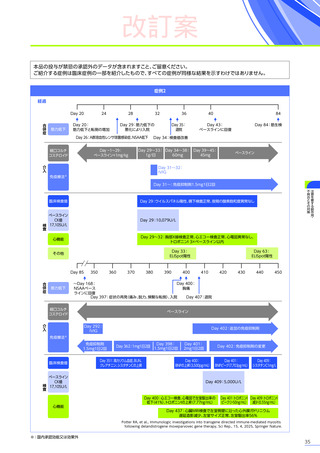
肝障害、慢性肝疾患又は急性肝疾患
(急性の肝ウイルス性感染症)
を有する患者さんは、重篤な急性肝障害発現のリスク
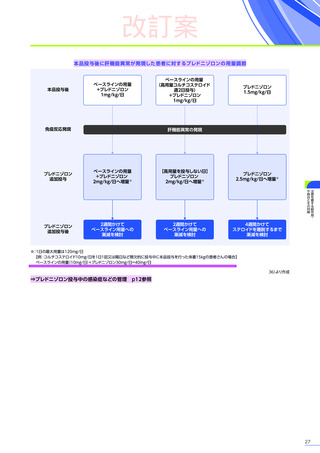
が高いおそれがあります。また、急性肝疾患を有する患者さんでは回復又は管理できる状態になるまで本品の投与を
延期してください。
⇒肝機能障害、急性肝不全 p21参照
<解説>
DMD患者では、変性した筋肉に由来する、
トランスアミナーゼや乳酸脱水素酵素の高値
(AST・ALTは最高で基準値上限の
22倍に達する)
を認め、本品投与前のベースラインより肝機能検査値が正常範囲を超えている場合が想定されます32)33)。
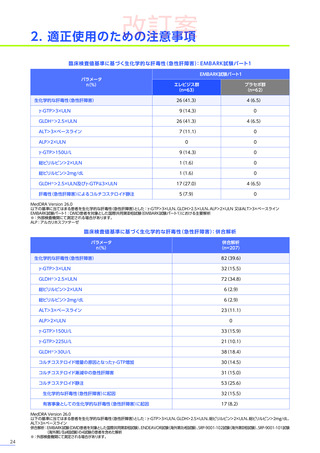
(n=207)
では、ベースラインの中央値
(範囲)
はASTが315.50U/L
(31~891)
、ALTが477.00U/L
臨床試験の併合解析※
(42~1,242)
、
γ-GTPが9.00U/L
(4.00~41.00)
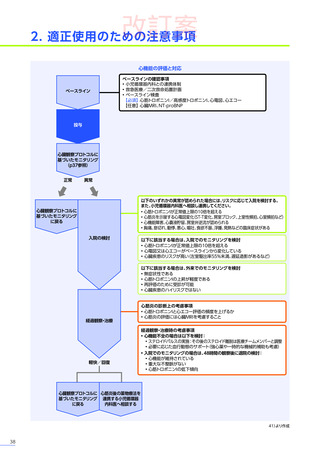
でした20)。本品の投与前には、肝機能検査及び画像検査を行い、異常が
認められた場合には投与の延期等の適切な対応を行ってください。
⇒肝機能検査(投与前) p15参照
⇒各副作用マネジメントのための他科/他施設との連携
p19参照
※:EMBARK試験
(DMD患者を対象とした国際共同第Ⅲ相試験)
、ENDEAVOR試験
(海外第Ⅰb相試験)
、SRP-9001-102試験
(海外第Ⅱ相試験)
、SRP-9001101試験
(海外第Ⅰ/Ⅱa相試験)
の4試験の患者を含めた解析
<参考>
• 臨床試験
(EMBARK試験パート1)
では、
γ-GTPが正常域上限
(ULN)
の2倍超、GLDHが15U/L超、総ビリルビンがULNを
超えている
(ジルベール症候群によると思われる増加が確認された場合以外)
をはじめとする臨床検査値異常が認められる
患者さんは除外されています17)。
⇒臨床試験成績
p60参照
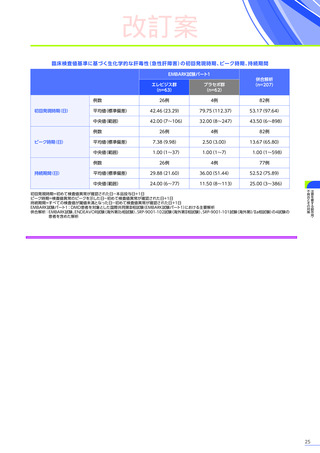
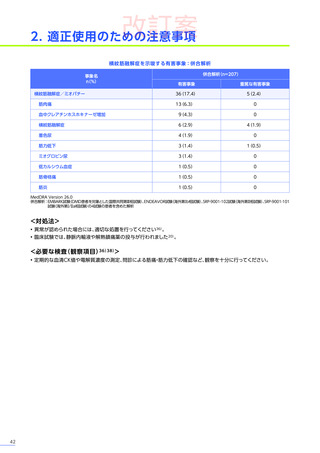
• DMD患者における脂肪肝の合併に関して、歩行可能なDMD患者21例中
[年齢中央値
(範囲)
:8.5歳
(3~18.5)
]
、脂肪肝
を合併している患者は3例
(14.28%)
であったという報告があります34)。
AST:アスパラギン酸アミノトランスフェラーゼ、
ALT:アラニンアミノトランスフェラーゼ、
γ-GTP:γ-グルタミルトランスフェラーゼ、
GLDH:グルタミン酸脱水素酵素
11
特定の背景を有する患者に関する注意
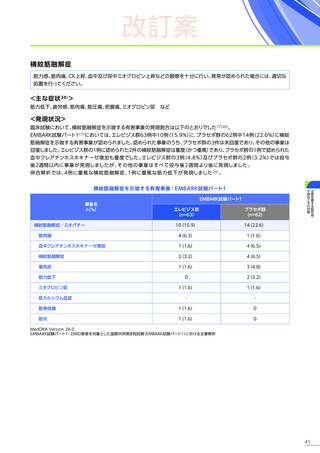
ジストロフィン遺伝子のエクソン1-17及び/又はエクソン59-71の欠失を有する患者に関する注意
ジストロフィン遺伝子のエクソン1-17及び/又はエクソン59-71の領域に欠失を有する患者さんは、重度の免疫介在性
の筋炎発現のリスクが高いおそれがあります。
⇒禁忌・禁止 p9参照
⇒筋炎 p32参照
<解説>
臨床試験
(EMBARK試験パート1)
では、エクソン1~17に変異のある患者さんは非適格として除外されています17)。
⇒臨床試験成績
p60参照
心エコーで左室駆出率が40%未満の患者さん及び症候性の心筋症を有する患者さんは、心筋炎の発現のリスクが高い
エレビジスの
投与対象の確認
心機能障害のある患者に関する注意
おそれがあります。臨床試験において、
これらの患者さんの十分なデータはありません。
⇒心筋炎 p36参照
<解説>
臨床試験(EMBARK試験パート1)
では、心エコーで左室駆出率が40%未満の患者さん及び心筋症を有する患者さんは
除外されています17)。
⇒臨床試験成績
p60参照
肝機能障害患者に関する注意
肝障害、慢性肝疾患又は急性肝疾患
(急性の肝ウイルス性感染症)
を有する患者さんは、重篤な急性肝障害発現のリスク
が高いおそれがあります。また、急性肝疾患を有する患者さんでは回復又は管理できる状態になるまで本品の投与を
延期してください。
⇒肝機能障害、急性肝不全 p21参照
<解説>
DMD患者では、変性した筋肉に由来する、
トランスアミナーゼや乳酸脱水素酵素の高値
(AST・ALTは最高で基準値上限の
22倍に達する)
を認め、本品投与前のベースラインより肝機能検査値が正常範囲を超えている場合が想定されます32)33)。
(n=207)
では、ベースラインの中央値
(範囲)
はASTが315.50U/L
(31~891)
、ALTが477.00U/L
臨床試験の併合解析※
(42~1,242)
、
γ-GTPが9.00U/L
(4.00~41.00)
でした20)。本品の投与前には、肝機能検査及び画像検査を行い、異常が
認められた場合には投与の延期等の適切な対応を行ってください。
⇒肝機能検査(投与前) p15参照
⇒各副作用マネジメントのための他科/他施設との連携
p19参照
※:EMBARK試験
(DMD患者を対象とした国際共同第Ⅲ相試験)
、ENDEAVOR試験
(海外第Ⅰb相試験)
、SRP-9001-102試験
(海外第Ⅱ相試験)
、SRP-9001101試験
(海外第Ⅰ/Ⅱa相試験)
の4試験の患者を含めた解析
<参考>
• 臨床試験
(EMBARK試験パート1)
では、
γ-GTPが正常域上限
(ULN)
の2倍超、GLDHが15U/L超、総ビリルビンがULNを
超えている
(ジルベール症候群によると思われる増加が確認された場合以外)
をはじめとする臨床検査値異常が認められる
患者さんは除外されています17)。
⇒臨床試験成績
p60参照
• DMD患者における脂肪肝の合併に関して、歩行可能なDMD患者21例中
[年齢中央値
(範囲)
:8.5歳
(3~18.5)
]
、脂肪肝
を合併している患者は3例
(14.28%)
であったという報告があります34)。
AST:アスパラギン酸アミノトランスフェラーゼ、
ALT:アラニンアミノトランスフェラーゼ、
γ-GTP:γ-グルタミルトランスフェラーゼ、
GLDH:グルタミン酸脱水素酵素
11