よむ、つかう、まなぶ。
総-1参考1 (81 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64319.html |
| 出典情報 | 中央社会保険医療協議会 総会(第619回 10/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
改訂案
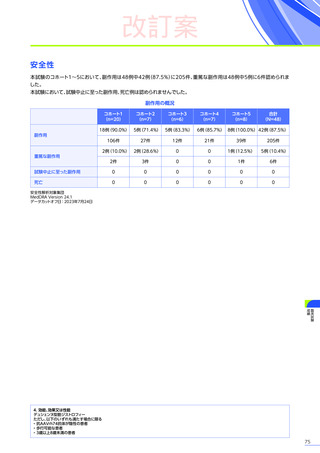
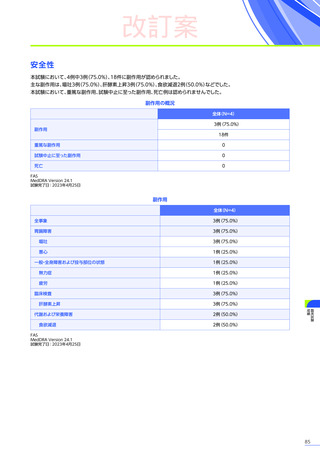
安全性
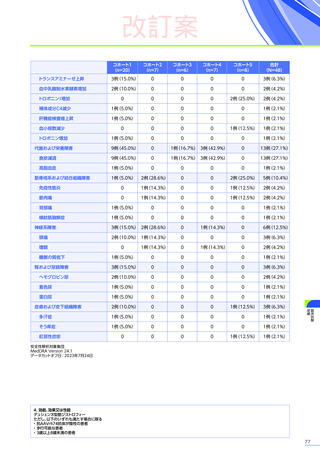
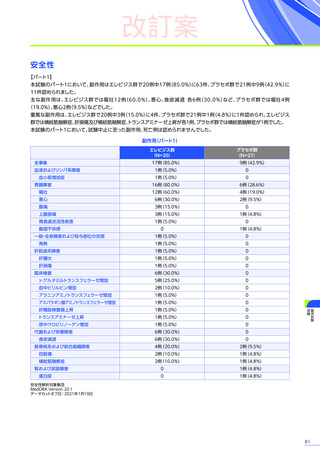
【パート1】
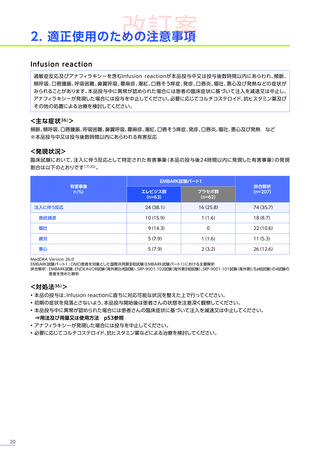
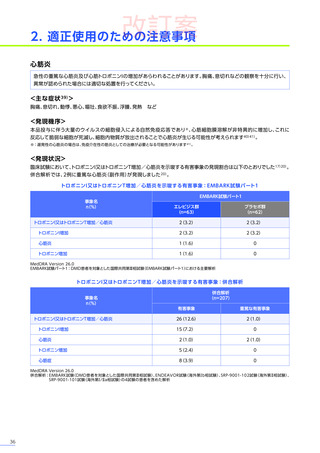
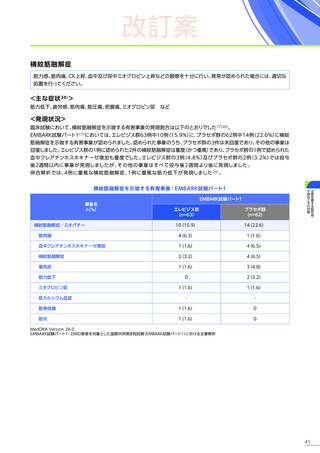
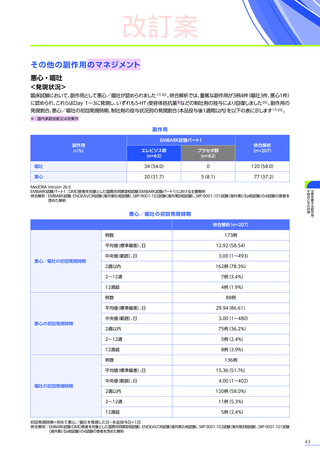
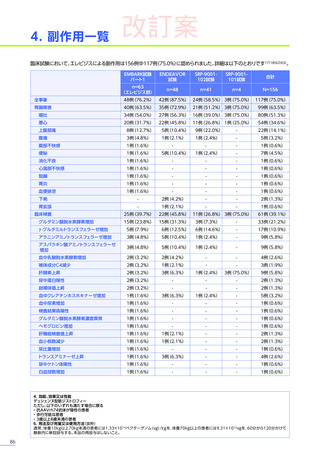
本試験のパート1において、副作用はエレビジス群で20例中17例
(85.0%)
に63件、プラセボ群で21例中9例
(42.9%)
に
11件認められました。
主な副作用は、エレビジス群では嘔吐12例(60.0%)、悪心、食欲減退 各6例(30.0%)など、プラセボ群では嘔吐4例
(19.0%)
、悪心2例
(9.5%)
などでした。
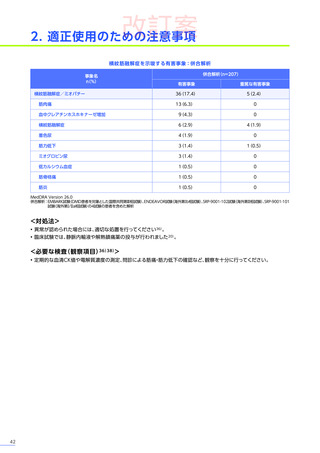
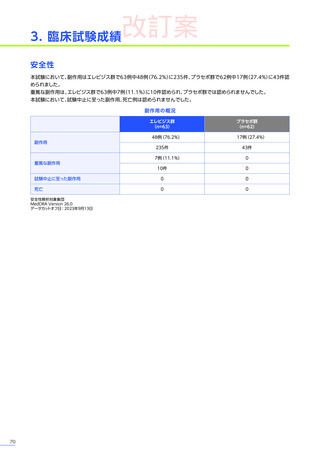
重篤な副作用は、エレビジス群で20例中3例
(15.0%)
に4件、プラセボ群で21例中1例
(4.8%)
に1件認められ、エレビジス
群では横紋筋融解症、
肝損傷及び横紋筋融解症、
トランスアミナーゼ上昇が各1例、
プラセボ群では横紋筋融解症が1例でした。
本試験のパート1において、試験中止に至った副作用、死亡例は認められませんでした。
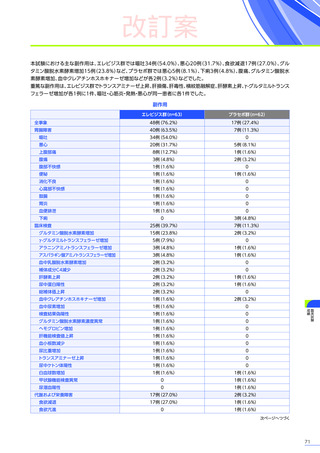
副作用
(パート1)
エレビジス群
(N=20)
全事象
17例(85.0%)
血液およびリンパ系障害
1例(5.0%)
血小板増加症
1例(5.0%)
プラセボ群
(N=21)
9例(42.9%)
0
0
胃腸障害
16例(80.0%)
6例(28.6%)
嘔吐
12例(60.0%)
4例(19.0%)
悪心
6例(30.0%)
2例(9.5%)
腹痛
3例(15.0%)
上腹部痛
3例(15.0%)
胃食道逆流性疾患
1例(5.0%)
腹部不快感
一般・全身障害および投与部位の状態
0
0
1例(4.8%)
0
1例(4.8%)
0
1例(5.0%)
0
肝胆道系障害
1例(5.0%)
0
肝腫大
1例(5.0%)
0
肝損傷
1例(5.0%)
0
臨床検査
6例(30.0%)
0
γ-グルタミルトランスフェラーゼ増加
5例(25.0%)
0
血中ビリルビン増加
2例(10.0%)
0
アラニンアミノトランスフェラーゼ増加
1例(5.0%)
0
アスパラギン酸アミノトランスフェラーゼ増加
1例(5.0%)
0
肝機能検査値上昇
1例(5.0%)
0
トランスアミナーゼ上昇
1例(5.0%)
0
尿中ウロビリノーゲン増加
1例(5.0%)
0
6例(30.0%)
0
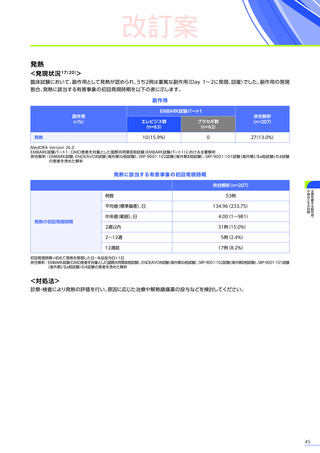
発熱
代謝および栄養障害
食欲減退
筋骨格系および結合組織障害
6例(30.0%)
0
4例(20.0%)
2例(9.5%)
四肢痛
2例(10.0%)
1例(4.8%)
横紋筋融解症
2例(10.0%)
1例(4.8%)
腎および尿路障害
蛋白尿
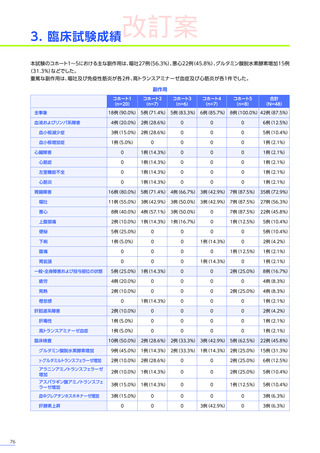
臨床試験
成績
1例(5.0%)
0
1例(4.8%)
0
1例(4.8%)
安全性解析対象集団
MedDRA Version 20.1
データカットオフ日:2021年1月19日
81
安全性
【パート1】
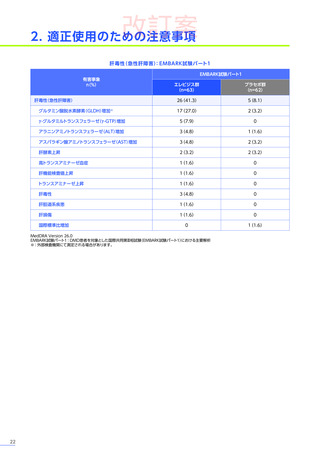
本試験のパート1において、副作用はエレビジス群で20例中17例
(85.0%)
に63件、プラセボ群で21例中9例
(42.9%)
に
11件認められました。
主な副作用は、エレビジス群では嘔吐12例(60.0%)、悪心、食欲減退 各6例(30.0%)など、プラセボ群では嘔吐4例
(19.0%)
、悪心2例
(9.5%)
などでした。
重篤な副作用は、エレビジス群で20例中3例
(15.0%)
に4件、プラセボ群で21例中1例
(4.8%)
に1件認められ、エレビジス
群では横紋筋融解症、
肝損傷及び横紋筋融解症、
トランスアミナーゼ上昇が各1例、
プラセボ群では横紋筋融解症が1例でした。
本試験のパート1において、試験中止に至った副作用、死亡例は認められませんでした。
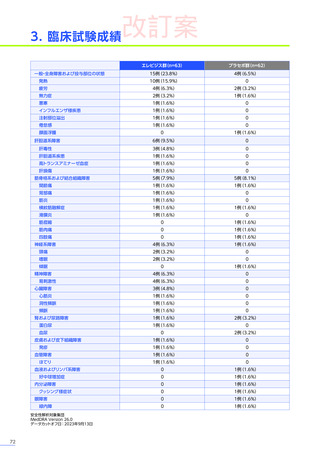
副作用
(パート1)
エレビジス群
(N=20)
全事象
17例(85.0%)
血液およびリンパ系障害
1例(5.0%)
血小板増加症
1例(5.0%)
プラセボ群
(N=21)
9例(42.9%)
0
0
胃腸障害
16例(80.0%)
6例(28.6%)
嘔吐
12例(60.0%)
4例(19.0%)
悪心
6例(30.0%)
2例(9.5%)
腹痛
3例(15.0%)
上腹部痛
3例(15.0%)
胃食道逆流性疾患
1例(5.0%)
腹部不快感
一般・全身障害および投与部位の状態
0
0
1例(4.8%)
0
1例(4.8%)
0
1例(5.0%)
0
肝胆道系障害
1例(5.0%)
0
肝腫大
1例(5.0%)
0
肝損傷
1例(5.0%)
0
臨床検査
6例(30.0%)
0
γ-グルタミルトランスフェラーゼ増加
5例(25.0%)
0
血中ビリルビン増加
2例(10.0%)
0
アラニンアミノトランスフェラーゼ増加
1例(5.0%)
0
アスパラギン酸アミノトランスフェラーゼ増加
1例(5.0%)
0
肝機能検査値上昇
1例(5.0%)
0
トランスアミナーゼ上昇
1例(5.0%)
0
尿中ウロビリノーゲン増加
1例(5.0%)
0
6例(30.0%)
0
発熱
代謝および栄養障害
食欲減退
筋骨格系および結合組織障害
6例(30.0%)
0
4例(20.0%)
2例(9.5%)
四肢痛
2例(10.0%)
1例(4.8%)
横紋筋融解症
2例(10.0%)
1例(4.8%)
腎および尿路障害
蛋白尿
臨床試験
成績
1例(5.0%)
0
1例(4.8%)
0
1例(4.8%)
安全性解析対象集団
MedDRA Version 20.1
データカットオフ日:2021年1月19日
81