よむ、つかう、まなぶ。
総-1参考1 (89 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64319.html |
| 出典情報 | 中央社会保険医療協議会 総会(第619回 10/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
5. Q & A
改訂案
1 投与対象を抗AAVrh74抗体が陰性の患者としているのはなぜですか?
非臨床試験の結果では、既存の抗AAVrh74抗体価が1:400を超えると有効性の低下が認められています19)。本品
の臨床試験では、ELISAにより測定したrAAVrh74抗体価が1:400未満(上昇していない)の患者のみ登録可能
でした17)。抗AAVrh74抗体が陽性の患者における本品の有効性及び安全性は確立していません。
また、Sarepta社はAAVrh74に対する抗体を有する4歳以上9歳以下のDMD患者を対象としたimlifidase ※1
投与後の本品の安全性及び有効性を検討する非盲検試験(SRP-9001-104試験)及びAAVrh74に対する抗体を
有する4歳以上8歳以下のDMD患者を対象とした血漿交換療法後の本品の安全性及び有効性を検討する非盲検試験
(SRP-9001-105試験)
を実施していますが、まだ結果が得られていません。SRP-9001-104試験では重篤な有害
事象として蕁麻疹が1件発現しました。本患者では本品の投与開始8分後に強い潮紅、発疹、浮腫、悪心及び倦怠感など
を伴う重篤で重度の蕁麻疹が発現し、本品の投与を中止しました。抗ヒスタミン薬及びメチルプレドニゾロン ※2
の静脈内投与後に回復しました。持続時間は約5時間でした64)。
2 なぜ2回目の投与ができないのでしょうか?
本品の初回投与時にAAVに対する抗体が産生されるため、再投与はできません。
抗AAVrh74抗体は、本品の筋細胞内への取り込みを阻害することで導入遺伝子の発現を妨げます。
また、過剰な免疫応答を誘発する可能性もあります。
1「投与対象を抗AAVrh74抗体が陰性の患者としているのはなぜですか?」
もご参照ください。
3 血管外漏出してしまった場合の対処法はありますか?
本品投与中の血管外漏出に対する具体的な対処法や治療法は明らかになっていません。血管外漏出が認められた
場合は、速やかに投与を中断し、症状に応じた適切な処置を行ってください。
本品はpH7.7~8.3、浸透圧388~426mOsm/kgの遺伝子治療用製品です36)。局所刺激性試験は実施していません
が、マウスを用いた単回投与毒性試験の評価では、一般状態観察及び病理学的検査において、投与部位に刺激性は
認められませんでした65)。
血管外漏出が発生した際は、弊社担当者にご連絡ください。
4 なぜエレビジスの調製中にフィルター針を使用してはいけないのですか?
副作用
一覧
本品の調製中にフィルター針を使用することで、閉塞のリスクが高まり、
シリンジとフィルターが外れやすくなると考え
られるためです。本品を必要量採取するためには複数のシリンジが必要になります。採取後はシリンジ内の空気を抜き、
注射針を外してシリンジにキャップをしてください。
&
Q
A
※1:国内未承認
※2:国内承認効能又は効果外
89
改訂案
1 投与対象を抗AAVrh74抗体が陰性の患者としているのはなぜですか?
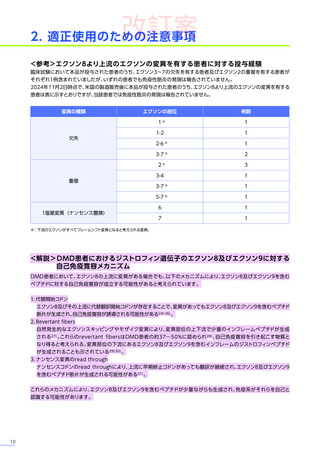
非臨床試験の結果では、既存の抗AAVrh74抗体価が1:400を超えると有効性の低下が認められています19)。本品
の臨床試験では、ELISAにより測定したrAAVrh74抗体価が1:400未満(上昇していない)の患者のみ登録可能
でした17)。抗AAVrh74抗体が陽性の患者における本品の有効性及び安全性は確立していません。
また、Sarepta社はAAVrh74に対する抗体を有する4歳以上9歳以下のDMD患者を対象としたimlifidase ※1
投与後の本品の安全性及び有効性を検討する非盲検試験(SRP-9001-104試験)及びAAVrh74に対する抗体を
有する4歳以上8歳以下のDMD患者を対象とした血漿交換療法後の本品の安全性及び有効性を検討する非盲検試験
(SRP-9001-105試験)
を実施していますが、まだ結果が得られていません。SRP-9001-104試験では重篤な有害
事象として蕁麻疹が1件発現しました。本患者では本品の投与開始8分後に強い潮紅、発疹、浮腫、悪心及び倦怠感など
を伴う重篤で重度の蕁麻疹が発現し、本品の投与を中止しました。抗ヒスタミン薬及びメチルプレドニゾロン ※2
の静脈内投与後に回復しました。持続時間は約5時間でした64)。
2 なぜ2回目の投与ができないのでしょうか?
本品の初回投与時にAAVに対する抗体が産生されるため、再投与はできません。
抗AAVrh74抗体は、本品の筋細胞内への取り込みを阻害することで導入遺伝子の発現を妨げます。
また、過剰な免疫応答を誘発する可能性もあります。
1「投与対象を抗AAVrh74抗体が陰性の患者としているのはなぜですか?」
もご参照ください。
3 血管外漏出してしまった場合の対処法はありますか?
本品投与中の血管外漏出に対する具体的な対処法や治療法は明らかになっていません。血管外漏出が認められた
場合は、速やかに投与を中断し、症状に応じた適切な処置を行ってください。
本品はpH7.7~8.3、浸透圧388~426mOsm/kgの遺伝子治療用製品です36)。局所刺激性試験は実施していません
が、マウスを用いた単回投与毒性試験の評価では、一般状態観察及び病理学的検査において、投与部位に刺激性は
認められませんでした65)。
血管外漏出が発生した際は、弊社担当者にご連絡ください。
4 なぜエレビジスの調製中にフィルター針を使用してはいけないのですか?
副作用
一覧
本品の調製中にフィルター針を使用することで、閉塞のリスクが高まり、
シリンジとフィルターが外れやすくなると考え
られるためです。本品を必要量採取するためには複数のシリンジが必要になります。採取後はシリンジ内の空気を抜き、
注射針を外してシリンジにキャップをしてください。
&
Q
A
※1:国内未承認
※2:国内承認効能又は効果外
89