よむ、つかう、まなぶ。
総-1参考1 (86 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64319.html |
| 出典情報 | 中央社会保険医療協議会 総会(第619回 10/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
4. 副作用一覧
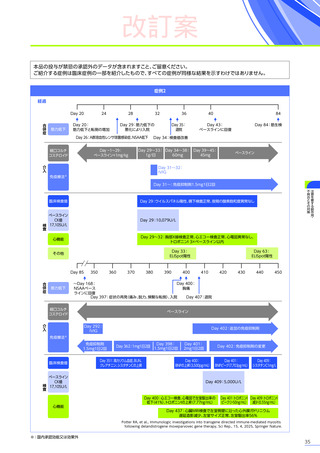
改訂案
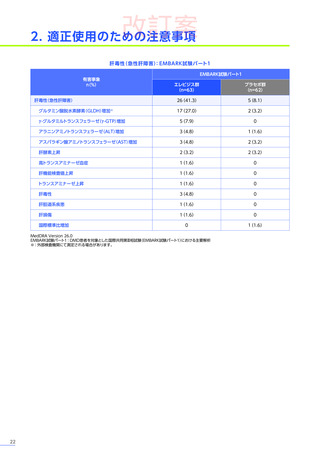
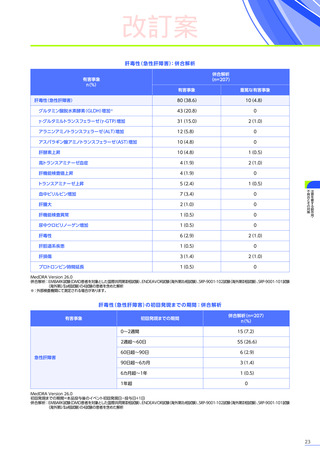
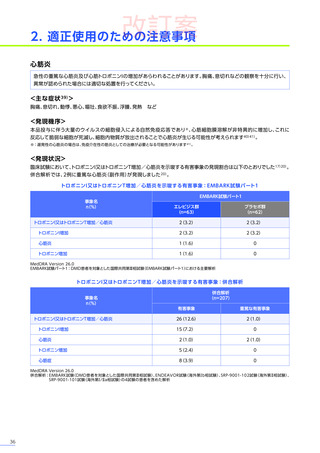
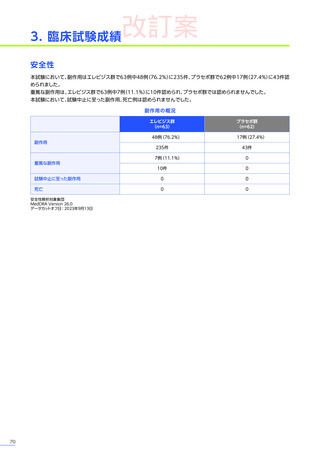
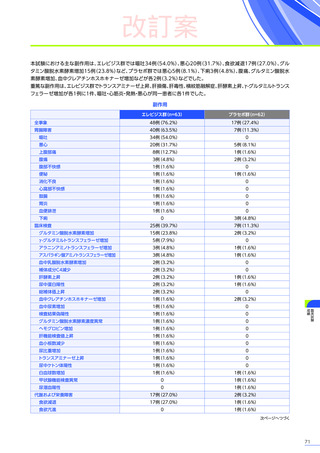
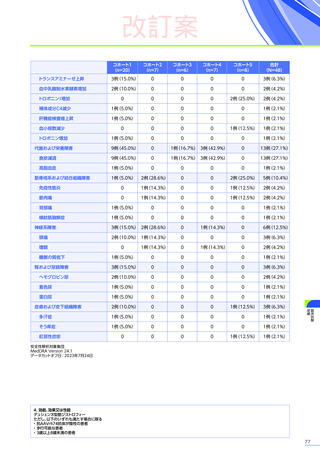
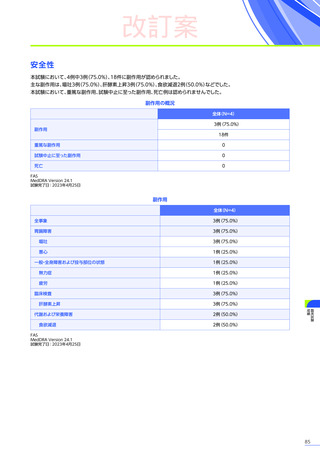
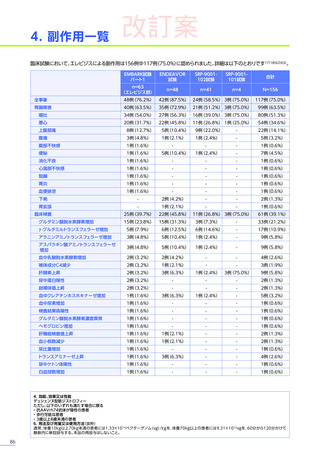
臨床試験において、
エレビジスによる副作用は156例中117例
(75.0%)
に認められました。詳細は以下のとおりです17)18)62)63)。
EMBARK試験
パート1
ENDEAVOR
試験
SRP-9001102試験
SRP-9001101試験
合計
n=63
(エレビジス群)
n=48
n=41
n=4
N=156
全事象
48例(76.2%)
42例(87.5%) 24例(58.5%) 3例(75.0%) 117例(75.0%)
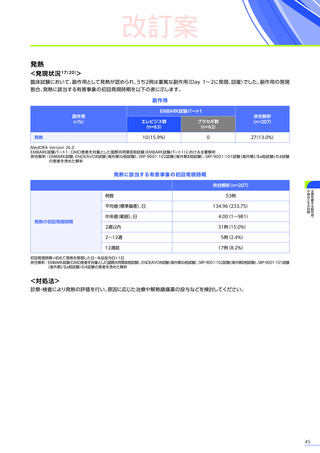
胃腸障害
40例(63.5%)
35例(72.9%) 21例(51.2%) 3例(75.0%)
99例(63.5%)
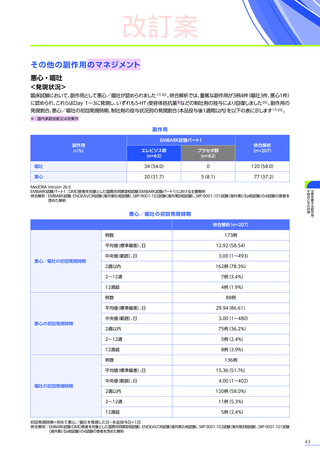
嘔吐
34例(54.0%)
27例(56.3%) 16例(39.0%) 3例(75.0%)
80例(51.3%)
悪心
20例(31.7%)
22例(45.8%) 11例(26.8%) 1例(25.0%)
54例(34.6%)
上腹部痛
8例(12.7%)
5例(10.4%)
9例(22.0%)
-
22例(14.1%)
腹痛
3例(4.8%)
1例(2.1%)
1例(2.4%)
-
5例(3.2%)
腹部不快感
1例(1.6%)
-
-
-
1例(0.6%)
便秘
1例(1.6%)
5例(10.4%)
1例(2.4%)
-
7例(4.5%)
消化不良
1例(1.6%)
-
-
-
1例(0.6%)
心窩部不快感
1例(1.6%)
-
-
-
1例(0.6%)
鼓腸
1例(1.6%)
-
-
-
1例(0.6%)
胃炎
1例(1.6%)
-
-
-
1例(0.6%)
血便排泄
1例(1.6%)
-
-
-
1例(0.6%)
下痢
-
2例(4.2%)
-
-
2例(1.3%)
胃拡張
-
1例(2.1%)
-
-
1例(0.6%)
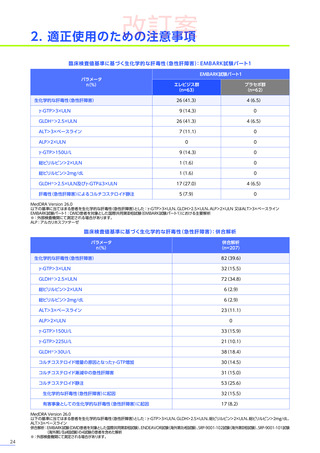
臨床検査
25例(39.7%)
22例(45.8%) 11例(26.8%) 3例(75.0%)
61例(39.1%)
グルタミン酸脱水素酵素増加
15例(23.8%)
15例(31.3%)
3例(7.3%)
-
33例(21.2%)
γ-グルタミルトランスフェラーゼ増加
5例(7.9%)
6例(12.5%)
6例(14.6%)
-
17例(10.9%)
アラニンアミノトランスフェラーゼ増加
3例(4.8%)
5例(10.4%)
1例(2.4%)
-
9例(5.8%)
アスパラギン酸アミノトランスフェラーゼ
増加
3例(4.8%)
5例(10.4%)
1例(2.4%)
-
9例(5.8%)
血中乳酸脱水素酵素増加
2例(3.2%)
2例(4.2%)
-
-
4例(2.6%)
補体成分C4減少
2例(3.2%)
1例(2.1%)
-
-
3例(1.9%)
肝酵素上昇
2例(3.2%)
3例(6.3%)
尿中蛋白陽性
2例(3.2%)
-
-
-
2例(1.3%)
総補体価上昇
2例(3.2%)
-
-
-
2例(1.3%)
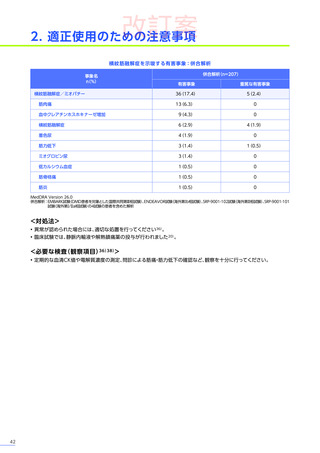
血中クレアチンホスホキナーゼ増加
1例(1.6%)
3例(6.3%)
1例(2.4%)
-
5例(3.2%)
血中尿素増加
1例(1.6%)
-
-
-
1例(0.6%)
1例(2.4%) 3例(75.0%)
9例(5.8%)
検査結果偽陽性
1例(1.6%)
-
-
-
1例(0.6%)
グルタミン酸脱水素酵素濃度異常
1例(1.6%)
-
-
-
1例(0.6%)
ヘモグロビン増加
1例(1.6%)
-
-
-
1例(0.6%)
肝機能検査値上昇
1例(1.6%)
1例(2.1%)
-
-
2例(1.3%)
血小板数減少
1例(1.6%)
1例(2.1%)
-
-
2例(1.3%)
尿比重増加
1例(1.6%)
-
-
-
1例(0.6%)
トランスアミナーゼ上昇
1例(1.6%)
3例(6.3%)
-
-
4例(2.6%)
尿中ケトン体陽性
1例(1.6%)
-
-
-
1例(0.6%)
白血球数増加
1例(1.6%)
-
-
-
1例(0.6%)
4. 効能、効果又は性能
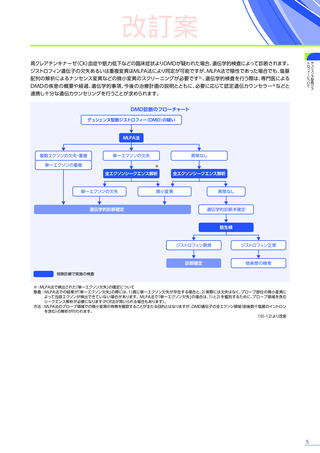
デュシェンヌ型筋ジストロフィー
ただし、以下のいずれも満たす場合に限る
・ 抗AAVrh74抗体が陰性の患者
・ 歩行可能な患者
・ 3歳以上8歳未満の患者
6. 用法及び用量又は使用方法
(抜粋)
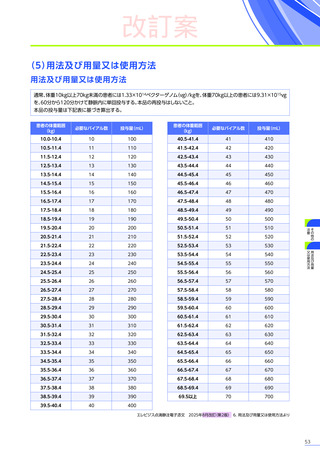
通常、体重10kg以上70kg未満の患者には1.33×10 14ベクターゲノム
(vg)
/kgを、体重70kg以上の患者には9.31×10 15vgを、60分から120分かけて
静脈内に単回投与する。本品の再投与はしないこと。
86
改訂案
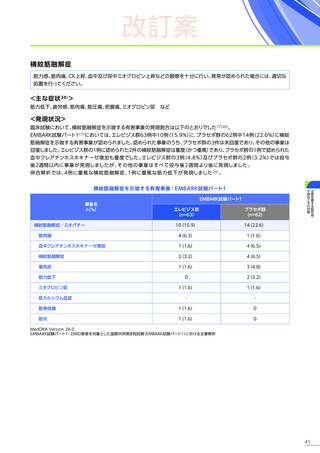
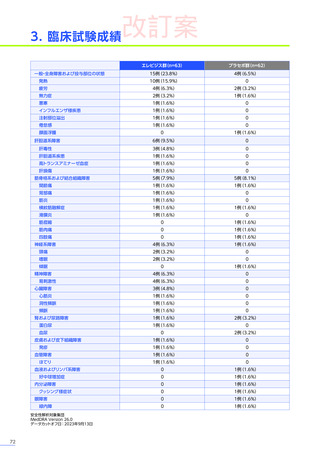
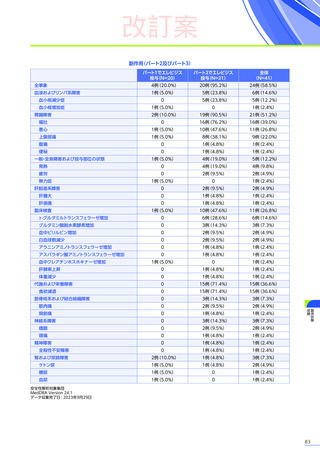
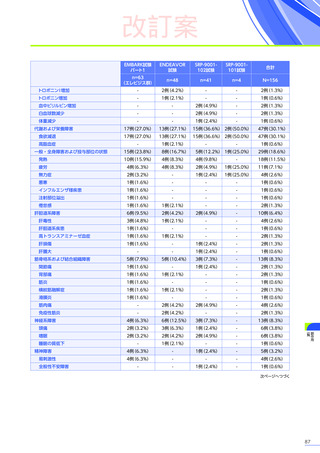
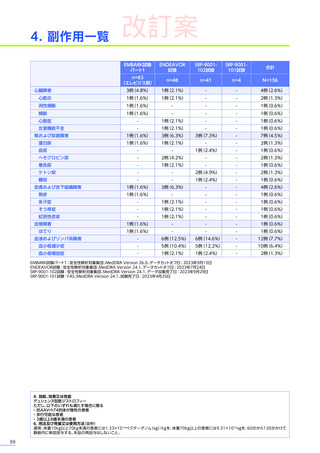
臨床試験において、
エレビジスによる副作用は156例中117例
(75.0%)
に認められました。詳細は以下のとおりです17)18)62)63)。
EMBARK試験
パート1
ENDEAVOR
試験
SRP-9001102試験
SRP-9001101試験
合計
n=63
(エレビジス群)
n=48
n=41
n=4
N=156
全事象
48例(76.2%)
42例(87.5%) 24例(58.5%) 3例(75.0%) 117例(75.0%)
胃腸障害
40例(63.5%)
35例(72.9%) 21例(51.2%) 3例(75.0%)
99例(63.5%)
嘔吐
34例(54.0%)
27例(56.3%) 16例(39.0%) 3例(75.0%)
80例(51.3%)
悪心
20例(31.7%)
22例(45.8%) 11例(26.8%) 1例(25.0%)
54例(34.6%)
上腹部痛
8例(12.7%)
5例(10.4%)
9例(22.0%)
-
22例(14.1%)
腹痛
3例(4.8%)
1例(2.1%)
1例(2.4%)
-
5例(3.2%)
腹部不快感
1例(1.6%)
-
-
-
1例(0.6%)
便秘
1例(1.6%)
5例(10.4%)
1例(2.4%)
-
7例(4.5%)
消化不良
1例(1.6%)
-
-
-
1例(0.6%)
心窩部不快感
1例(1.6%)
-
-
-
1例(0.6%)
鼓腸
1例(1.6%)
-
-
-
1例(0.6%)
胃炎
1例(1.6%)
-
-
-
1例(0.6%)
血便排泄
1例(1.6%)
-
-
-
1例(0.6%)
下痢
-
2例(4.2%)
-
-
2例(1.3%)
胃拡張
-
1例(2.1%)
-
-
1例(0.6%)
臨床検査
25例(39.7%)
22例(45.8%) 11例(26.8%) 3例(75.0%)
61例(39.1%)
グルタミン酸脱水素酵素増加
15例(23.8%)
15例(31.3%)
3例(7.3%)
-
33例(21.2%)
γ-グルタミルトランスフェラーゼ増加
5例(7.9%)
6例(12.5%)
6例(14.6%)
-
17例(10.9%)
アラニンアミノトランスフェラーゼ増加
3例(4.8%)
5例(10.4%)
1例(2.4%)
-
9例(5.8%)
アスパラギン酸アミノトランスフェラーゼ
増加
3例(4.8%)
5例(10.4%)
1例(2.4%)
-
9例(5.8%)
血中乳酸脱水素酵素増加
2例(3.2%)
2例(4.2%)
-
-
4例(2.6%)
補体成分C4減少
2例(3.2%)
1例(2.1%)
-
-
3例(1.9%)
肝酵素上昇
2例(3.2%)
3例(6.3%)
尿中蛋白陽性
2例(3.2%)
-
-
-
2例(1.3%)
総補体価上昇
2例(3.2%)
-
-
-
2例(1.3%)
血中クレアチンホスホキナーゼ増加
1例(1.6%)
3例(6.3%)
1例(2.4%)
-
5例(3.2%)
血中尿素増加
1例(1.6%)
-
-
-
1例(0.6%)
1例(2.4%) 3例(75.0%)
9例(5.8%)
検査結果偽陽性
1例(1.6%)
-
-
-
1例(0.6%)
グルタミン酸脱水素酵素濃度異常
1例(1.6%)
-
-
-
1例(0.6%)
ヘモグロビン増加
1例(1.6%)
-
-
-
1例(0.6%)
肝機能検査値上昇
1例(1.6%)
1例(2.1%)
-
-
2例(1.3%)
血小板数減少
1例(1.6%)
1例(2.1%)
-
-
2例(1.3%)
尿比重増加
1例(1.6%)
-
-
-
1例(0.6%)
トランスアミナーゼ上昇
1例(1.6%)
3例(6.3%)
-
-
4例(2.6%)
尿中ケトン体陽性
1例(1.6%)
-
-
-
1例(0.6%)
白血球数増加
1例(1.6%)
-
-
-
1例(0.6%)
4. 効能、効果又は性能
デュシェンヌ型筋ジストロフィー
ただし、以下のいずれも満たす場合に限る
・ 抗AAVrh74抗体が陰性の患者
・ 歩行可能な患者
・ 3歳以上8歳未満の患者
6. 用法及び用量又は使用方法
(抜粋)
通常、体重10kg以上70kg未満の患者には1.33×10 14ベクターゲノム
(vg)
/kgを、体重70kg以上の患者には9.31×10 15vgを、60分から120分かけて
静脈内に単回投与する。本品の再投与はしないこと。
86