会議資料 (88 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第64回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号;IV-168
「5.要望内容に係る国内外の公表文
小児の AIHA 患者における本剤の使用実態としては、
献・成書等について(1)無作為化比較試験、薬物動態試験等の公表論文としての報告状況」
に記載のとおり、海外において、前方視的試験、後方視的試験、症例報告が報告されており、
その他、メタ・アナリシス/システマティックレビューや総説による報告や国内外教科書に
おける記載も確認されている。
また、
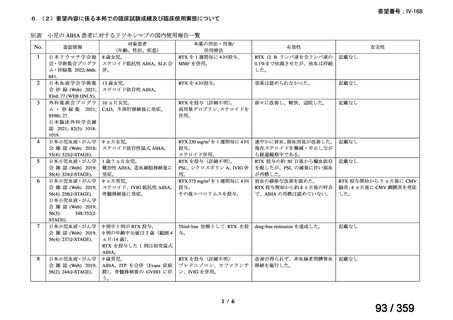
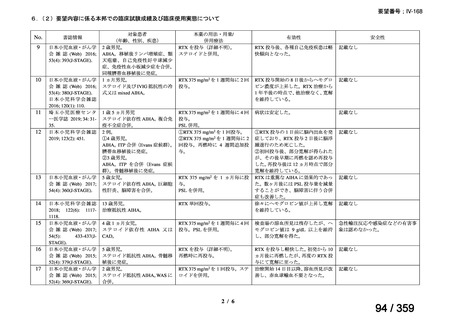
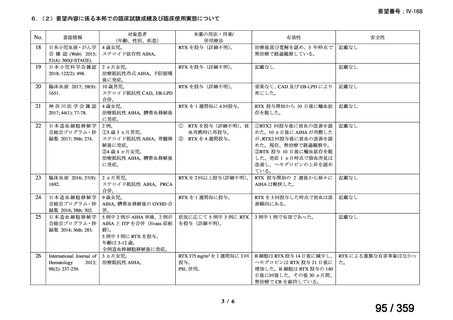
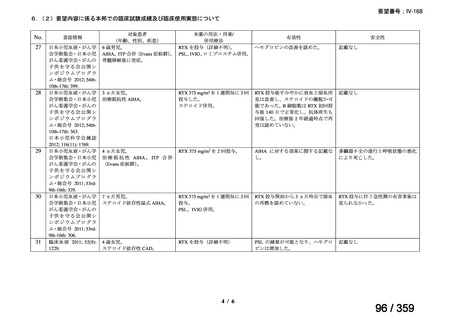
「6.本邦での開発状況(経緯)及び使用実態について(2)要望内容に係る本邦で
の臨床試験成績及び臨床使用実態について」に記載のとおり、国内の使用実態と臨床的有用
性が報告されていることから、臨床使用実態に不足はないと考える。なお、PCH は温式 AIHA
及び CAD と比較して症例数が少なく、国内外の診療ガイドラインにおいてもエビデンスは限
られているが、症例数は限定的であるものの、本剤が副腎皮質ホルモン薬で効果不十分の PCH
に対して有効であったとの報告がある 61)。
(2)上記(1)で臨床使用実態が不足している場合は、必要とされる使用実態調査等の内
容について
国内でも臨床使用実態があり、現時点では、製造販売後調査等により迅速かつ重点的に情
報を収集する必要性はないと考える。承認後は、通常の安全性監視体制にて情報を収集し、
検討を要する問題点が見出された場合には、速やかに適切な製造販売後調査等を実施する必
要があると考える。
(3)その他、製造販売後における留意点について
該当なし
10.備考
該当なし
11.参考文献一覧
1)
厚生労働科学研究費補助金 難治性疾患政策研究事業 特発性造血障害に関する調査研究
班 自己免疫性溶血性貧血の診断基準と診療の参照ガイド改訂版作成のためのワーキン
ググループ作成.自己免疫性溶血性貧血診療の参照ガイド 令和 4 年度改訂版, 2023.
2)
Murphy S, LoBuglio AF. Drug therapy of autoimmune hemolytic anemia. Semin Hematol 1976;
13(4): 323-334.
3)
小峰光博, 自己免疫性溶血性貧血の長期予後:二つの症例集団の追跡調査成績. 平成 8 年
度報告書(血液系疾患調査研究班特発性造血障害分科会), pp64-66.
4)
Berentsen S, Ulvestad E, Langholm R, et al. Primary chronic cold agglutinin disease: a
population based clinical study of 86 patients. Haematologica 2006; 91(4): 460-466.
59
88 / 359