会議資料 (201 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第64回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
国立研究開発法人日本医療研究開発機構の支援を受け、医師主導治験として実施された国内
第Ⅲ相試験 7)、8)において、リンパ管静脈吻合術時における本薬を用いたリンパ管造影に係る
有効性及び安全性が確認された(5.(1)項参照)
。
<本邦における臨床使用実態>
1)リンパ浮腫画像検査の実態について:日本形成外科学会認定施設を対象とした全国アンケ
ート調査から(リンパ学 2018; 41: 81-5)14)
日本形成外科学会認定施設 318 施設を対象にリンパ浮腫診療に関するアンケート調査を実
施した(調査期間:2016 年 8~9 月)。36 施設(11.3%)から回答が得られ、2010~2015 年の
リンパ管静脈吻合術の施行件数上位 20 施設のうち 11 施設が回答に含まれていた。回答を得
た 36 施設のうち、リンパ管静脈吻合術を実施している施設は 28 施設であり、そのうち 27 施
設でリンパ管静脈吻合術時に本薬を用いたリンパ管造影が行われており、その使用実態は以
下のとおりであった。
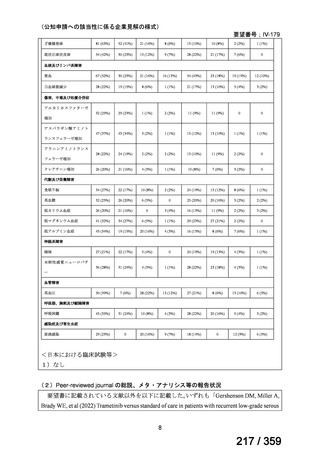
リンパ管造影に用いた本薬の濃度は、2.5 mg/mL が 52%(14/27 施設)、5 mg/mL が 19%
(5/27 施設)、1.25 mg/mL が 7%(2/27 施設)、6.25 mg/mL が 7%(2/27 施設)、不明が 15%
(4/27 施設)であった。
投与経路は、皮内投与が 59%(16/27 施設)、皮下投与が 22%(6/27 施設)、皮内・皮下投
与併用が 19%(5/27 施設)であった。
投与部位について回答が得られた施設は上肢 12 施設、下肢 13 施設であった。上肢では、
1 カ所目に第 1 指間が 58%(7/12 施設)、第 2 指間が 42%(5/12 施設)であり、2 カ所目
に第 4 指間に追加しているのが 58%(7/12 施設)
、さらに 42%(5/12 施設)では 3 カ所目
に手関節掌側に追加していた。下肢では、1 カ所目に第 1 趾間が 85%(11/13 施設)、第 2
趾間が 15%(2/13 施設)であり、2 カ所目に外果 46%(6/13 施設)、内果 15%(2/13 施設)
、
第 4 趾間 23%(3/13 施設)、第 3 趾間 8%(1/13 施設)及び足底部 8%(1/13 施設)に追
加していた。なお、2 施設では手術時に随時追加していた。
濃度と注射総量より総投与量が計算できた施設は上肢 19 施設、下肢 20 施設であり、本
薬の総投与量(平均[範囲])は、上肢で 2.4 mg[0.25~6.25 mg]、下肢で 2.7 mg[0.13
~6.25 mg]であった。
安全性について、副作用として注射部位の発赤等の軽度の局所症状(3 件)、気分不良等の
軽度の全身症状(1 件)が報告されたが、いずれも重篤ではなかった。
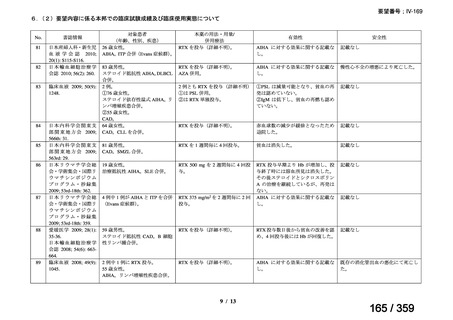
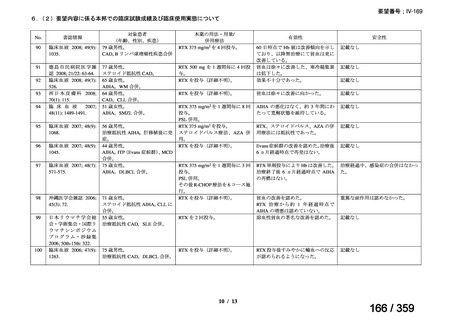
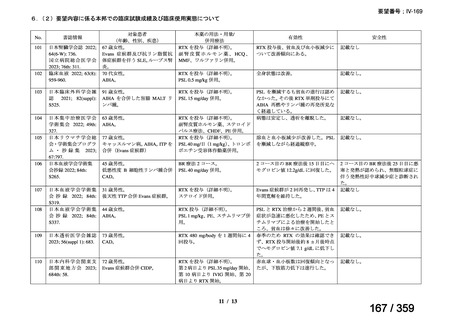
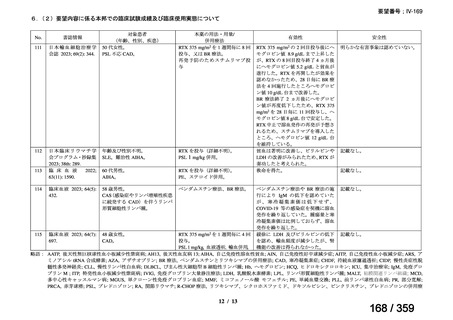
2)本邦における臨床使用実態に関する文献報告 15~21)
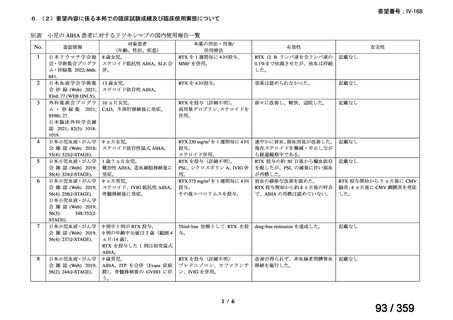
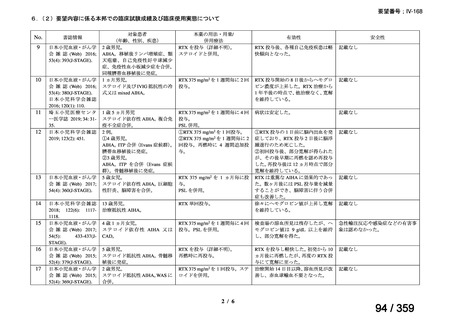
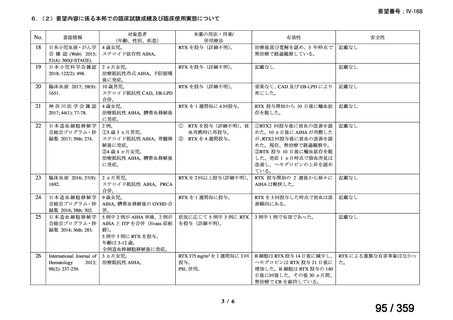
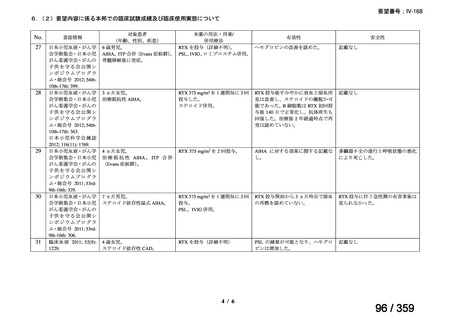
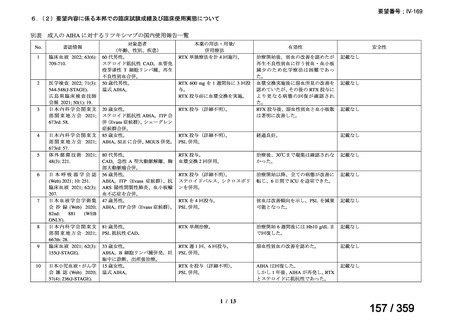
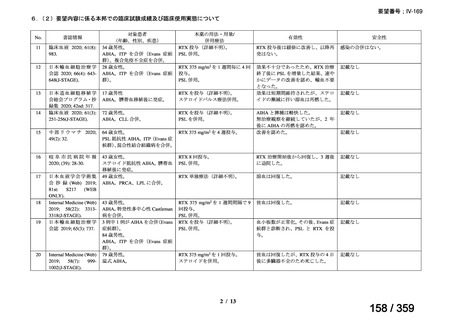
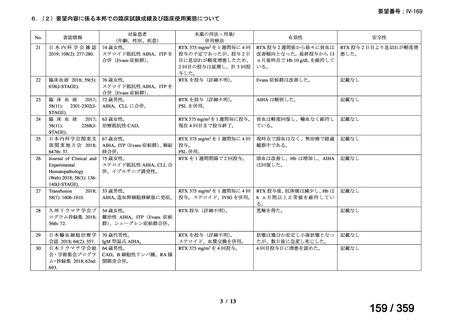
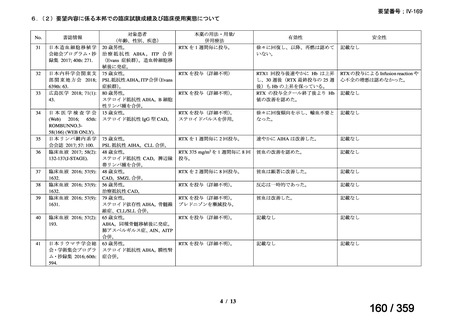
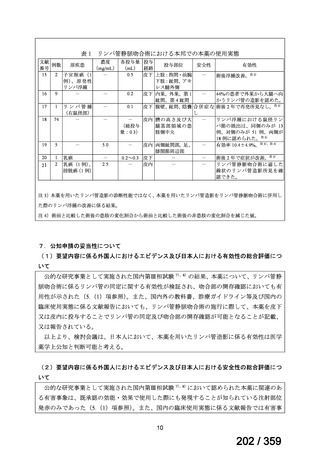
要望内容に係る本邦での臨床使用実態に関する報告のうち、リンパ管静脈吻合術における
リンパ管の同定又は吻合部の開存確認の目的で使用され、本薬の用法・用量に関する情報が
記載された報告は、表 1 のとおりであった。
9
201 / 359