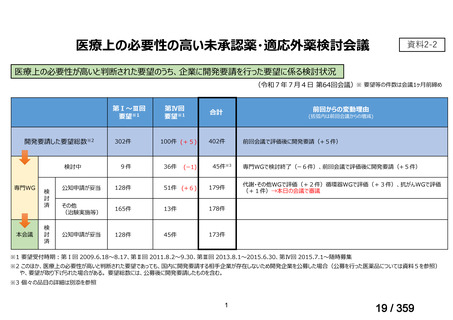
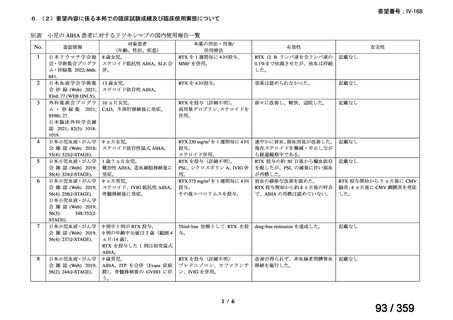
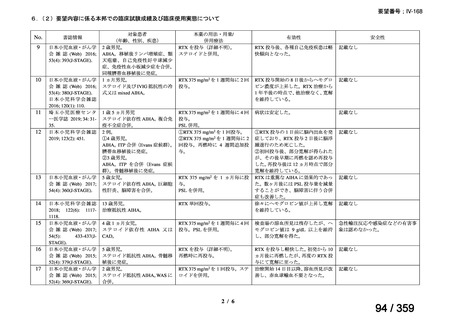
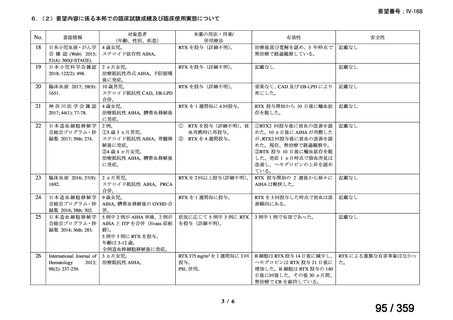
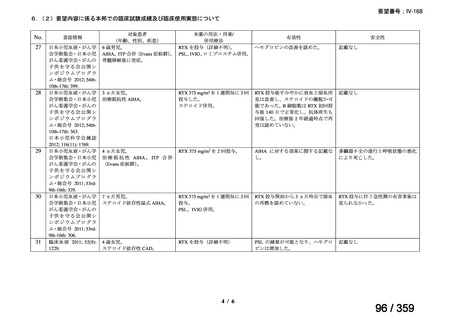
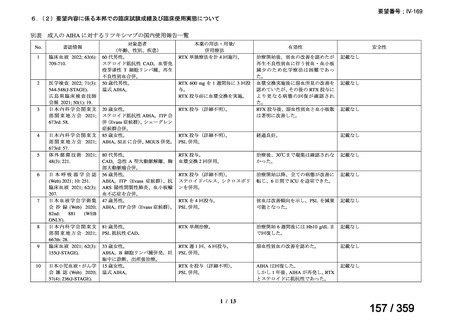
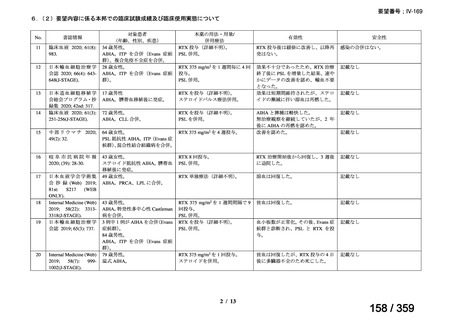
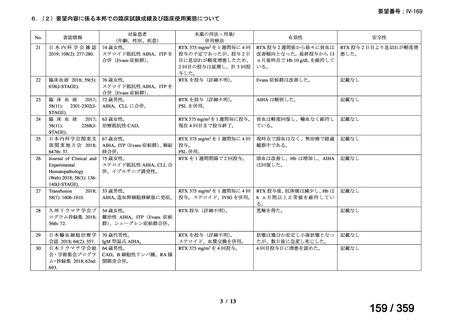
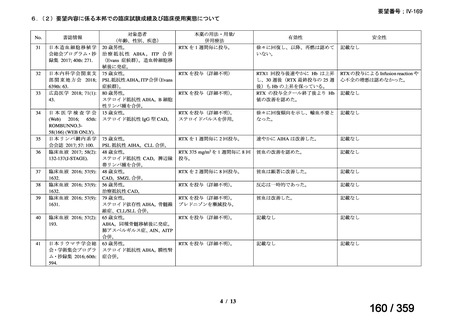
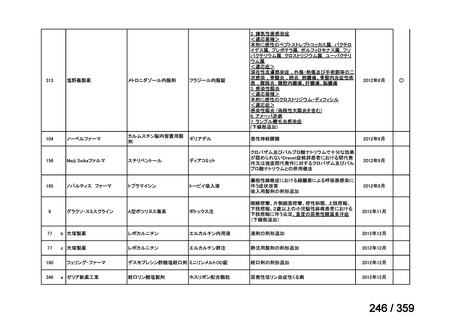
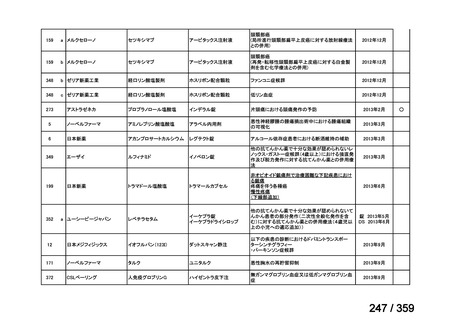
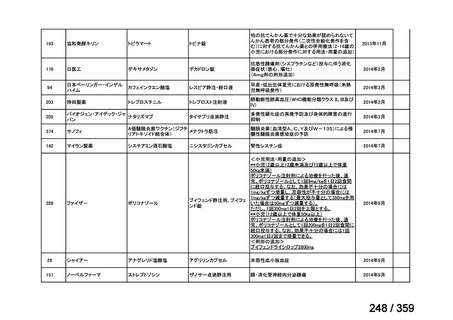
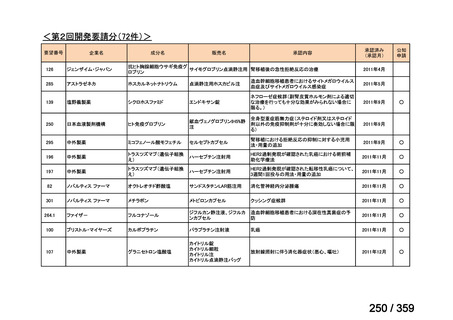
会議資料 (69 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第64回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号;IV-168
ルなリンパ増殖が 6 例、反応性のリンパ球浸潤/非クローナルなリンパ増殖性障害が 2 例
であった。
、効果
27 例中 14 例で本剤のファーストライン治療が奏効し(CR が 1 例、PR が 13 例)
を認めなかった 2 例に対して本剤と IFN の併用治療が行われ、1 例が PR、1 例では効果を
認めなかった。8 例で再発を認め、3 例に本剤と IFN の併用治療が行われ、5 例に対して本
剤単剤治療が行われ、5 例で PR を認め、3 例では効果を認めなかった。2 例では 2 回目の
再発に対して本剤単剤治療を実施し、PR を認めた。本剤治療は合計 37 コース実施され、
CR が 1 コース、PR が 19 コースで認められ、効果を認めるまでの期間中央値は 1.5 ヵ月(範
囲 0.5-4.0 ヵ月)であった。
奏効を認めた 17 例の奏効期間(奏効を認めた後の再発又は 12 ヵ月を超える場合)中央
値は、11 ヵ月(範囲 2-42 ヵ月)であり、1 例(28 ヵ月後に PR を維持)を除きその他の症
例では 12 ヵ月を超えた時期で再発を認めた。CR を認めた症例では 42 ヵ月間、奏効を維持
した。12 例で本剤治療後に骨髄障害の消失を認めた。
重篤な infusion reaction の発現は認められなかったが、1 例で本剤初回投与時に筋肉痛を
認めた。本剤に関連のある血液毒性が 1 例(grade 4 の好中球減少症、grade 2 の発熱、grade
1 の感染症)に認められた。本剤単剤治療が無効であった 2 例が、治療と関係ない疾患に
よりそれぞれ治療後 4 ヵ月、12 ヵ月で死亡したが、その他の症例については治療後 3~43
ヵ月時点で生存を認めている。
(3)AIHA(共通)に関する報告
1)AIHA を対象としたリツキシマブの有効性及び安全性に関する後方視的解析 35)
AIHA 患者又は ITP 患者に対する本剤治療に関する多施設共同の後方視的解析がベルギ
ーで実施され、17 施設から AIHA 患者 53 例の解析結果が報告された。
対象患者は、特発性又は続発性の AIHA で、1 種類以上の前治療が奏効せず本剤治療が 1
コース以上実施された患者とした。女性が 28 例(53%)、本剤投与開始時の年齢中央値は
65 歳(範囲 1-87 歳)
、18 例(34%)で基礎疾患を認めず、温式 AIHA が 36 例(68%)、CAD
が 14 例(26%)、不明が 3 例(6%)
、前治療数中央値は 2(範囲 1-4)、脾摘実施例が 10 例
(19%)
、診断から初回本剤投与までの期間中央値は 10 ヵ月(範囲 0.5-132 ヵ月)
、本剤投
与前に輸血が必要だった症例が 26 例
(49%)
、ヘモグロビン値中央値が 8.8 g/dL
(範囲 4.0-14.2
g/dL)であった。
92.7%の症例に対して本剤 375 mg/m2 の週 1 回、4 回投与が行われ、本剤単剤投与が 12
例(22.6%)でそれ以外の症例では副腎皮質ステロイド薬を含む併用治療が行われた。
CR は免疫抑制療法が実施されない状態でヘモグロビン値が正常化及び溶血の徴候を認
めない場合とし、PR は輸血を実施していた症例では輸血が不要となった場合、及び/又は
ヘモグロビン値が 2 g/dL 上昇とし、それら以外は非奏効とした。
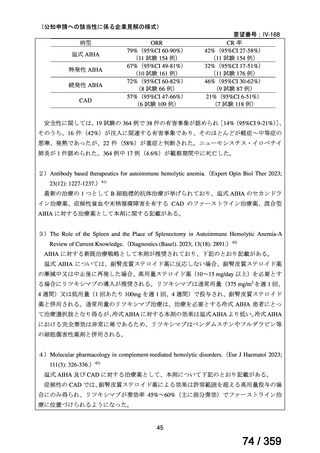
本剤初回投与時の ORR は 79%(42/53 例、CR:47%、PR:32%)
、本剤単剤治療の 12 例
においても、ORR が 75%、CR が 42%、PR が 33%であった。本剤初回投与からの追跡期間
40
69 / 359