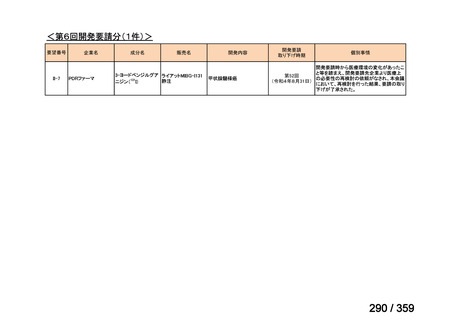
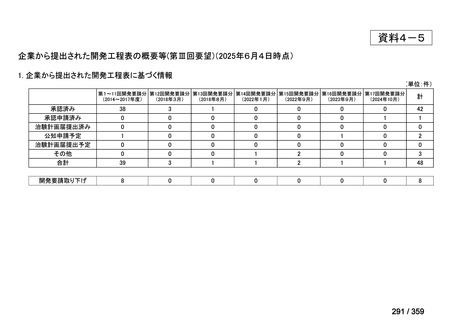
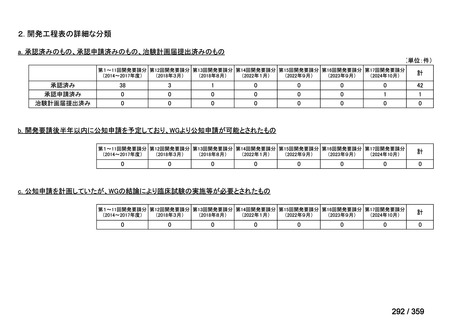
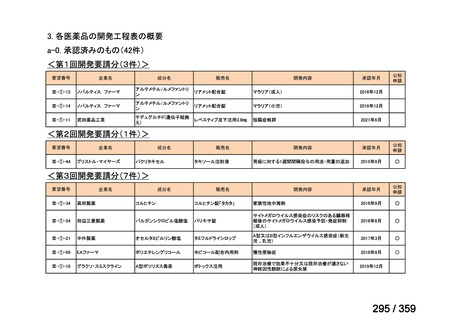
会議資料 (216 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第64回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
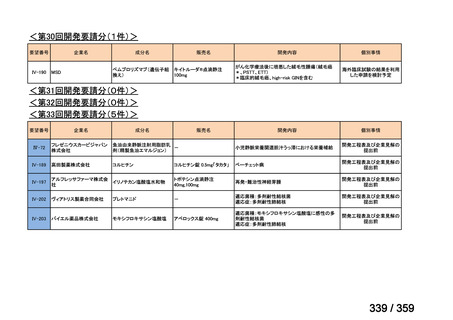
要望番号;IV-179
0.36-0.64],p<0.0001)[Log-rank 検定(片側有意水準 2.5%)]。全生存期間(OS)中央値
は,追跡不十分のデータであるが,トラメチニブ群 37.6 カ月,標準治療群 29.2 カ月(ハザー
ド比 0.76[95%CI 0.51-1.12],p<0.056)と,トラメチニブ群で良好な成績であった。
KRAS,BRAF 又は NRAS 変異陽性患者及び変異陰性患者における PFS はともにトラメ
チニブ群の方が優れていた[それぞれ,ハザード比 0.55(95% CI 0.28-1.07),ハザード比
0.64[95%CI 0.39-1.03])。変異状態が PFS の予測因子になることは示されなかった(交
互作用の検定,多重比較調整済 p 値=0.72)。
また,変異陰性患者における ORR[トラメチニブ群 8.3%(48 例中 4 例),
標準治療群 7.1%
(42 例中 3 例)]より変異陽性患者における ORR[トラメチニブ群 50.0%(22 例中 11 例),
標準治療群 9.1%(22 例中 2 例)]は,トラメチニブ群では標準治療群に比べ顕著に良好で
あったが,統計学的有意差は認められなかった(交互作用の検定,多重比較調整済 p 値
=0.11)。
安全性評価:
安全性解析対象集団におけるトラメチニブ群
(128 例)
で高頻度に発現した Grade 3 又は 4
の有害事象(AE)は,発疹(ざ瘡様発疹,斑状丘疹状皮疹)(17 例,13%),貧血(16 例,
13%),高血圧(15 例,12%),下痢(13 例,10%),悪心(12 例,9%),疲労(10 例,8%)
であった。標準治療群(127 例)で高頻度に発現した Grade 3 又は 4 の AE は,腹痛(22 例,
17%),悪心(14 例,11%),貧血(12 例,10%),嘔吐(10 例,8%)であった(Table 1)。
治療関連の死亡はなかった。新たな安全性シグナルは認められなかった。
解釈:トラメチニブは,再発 LGSOC 及び LGSPC に対する新たな標準治療の選択肢となる。
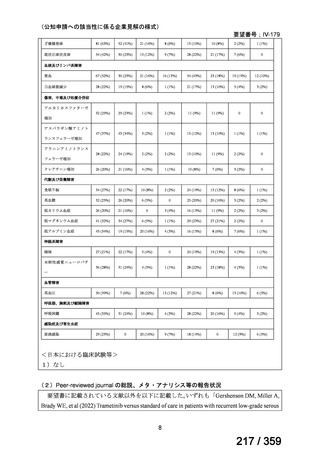
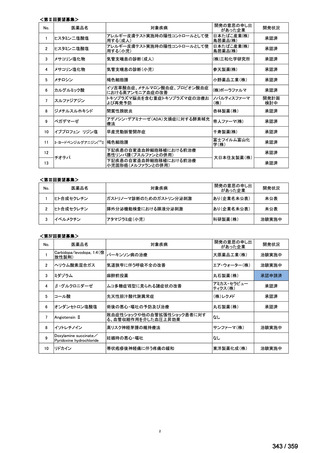
Table 1 安全性解析対象集団における AE の発現状況(20%以上の患者に発現した AE)
トラメチニブ群 (N=128)
標準治療群(N=127)
Any grade
Grade 1
Grade 2
Grade >3
Any grade
Grade 1
Grade 2
Grade >3
疲労
93 (73%)
47 (37%)
36 (28%)
10 (8%)
74 (58%)
44 (35%)
25 (20%)
5 (4%)
末梢性浮腫
62 (49%)
44 (34%)
18 (14%)
0
15 (12%)
9 (7%)
5 (4%)
1 (1%)
腹痛
57 (45%)
37 (29%)
13 (10%)
7 (6%)
60 (47%)
27 (21%)
11 (9%)
22 (17%)
便秘
54 (42%)
43 (34%)
8 (6%)
3 (2%)
49 (39%)
38 (30%)
8 (6%)
3 (2%)
下痢
93 (73%)
57 (45%)
23 (18%)
13 (10%)
43 (34%)
29 (23%)
10 (8%)
4 (3%)
口腔粘膜炎
45 (35%)
34 (27%)
8 (6%)
3 (2%)
23 (18%)
13 (10%)
8 (6%)
2 (2%)
悪心
78 (61%)
43 (34%)
23 (18%)
12 (9%)
65 (51%)
39 (31%)
12 (9%)
14 (11%)
嘔吐
59 (46%)
40 (31%)
10 (8%)
10 (7%)
44 (35%)
24 (19%)
10 (8%)
10 (8%)
56 (44%)
46 (36%)
9 (7%)
1 (1%)
17 (13%)
16 (13%)
1 (1%)
0
一般・全身障害
胃腸障害
皮膚及び皮下組織障害
皮膚乾燥
7
216 / 359