会議資料 (130 ページ)
出典
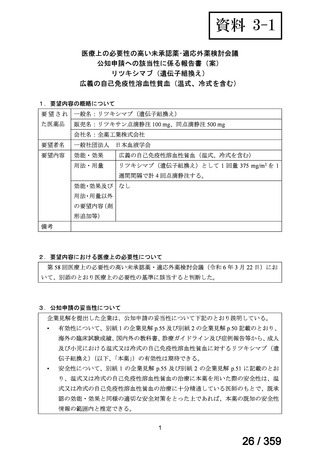
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第64回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
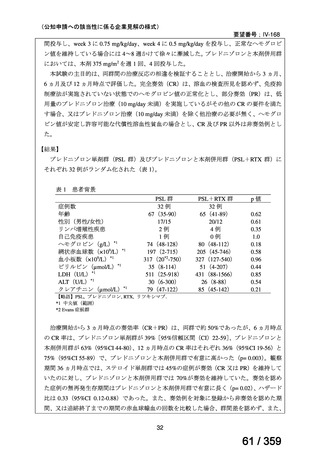
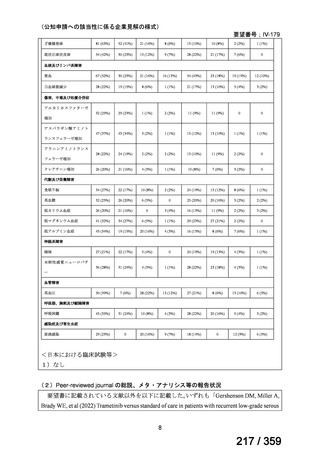
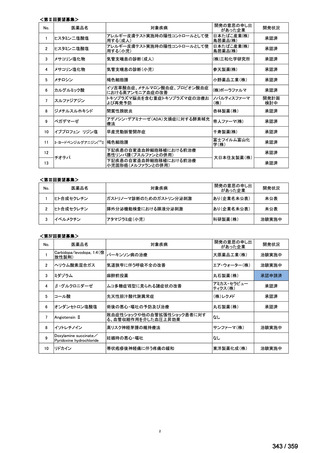
症例数
年齢
性別(男性/女性)
リンパ増殖性疾患
自己免疫疾患
ヘモグロビン(g/L)*1
網状赤血球数(×109/L)*1
血小板数(×109/L)*1
ビリルビン(µmol/L)*1
LDH(U/L)*1
ALT(U/L)*1
クレアチニン(µmol/L)*1
PSL 群
32 例
67(35-90)
17/15
2例
1例
74(48-128)
197(2-715)
317(20*2-750)
35(8-114)
511(25-918)
30(6-300)
79(47-122)
要望番号;IV-169
PSL+RTX 群
p値
32 例
65(41-89)
0.62
20/12
0.61
4例
0.35
0例
1.0
80(48-112)
0.18
205(45-746)
0.58
327(127-540)
0.96
51(4-207)
0.44
431(88-1566)
0.85
26(8-88)
0.54
85(45-142)
0.21
【略語】PSL, プレドニゾロン, RTX, リツキシマブ.
*1 中央値(範囲)
*2 Evans 症候群
治療開始から 3 ヵ月時点の奏効率(CR+PR)は、両群で約 50%であったが、6 ヵ月時点
の CR 率は、プレドニゾロン単剤群が 39%[95%信頼区間(CI)22-59]
、プレドニゾロンと
本剤併用群が 63%(95%CI 44-80)
、12 ヵ月時点の CR 率はそれぞれ 36%(95%CI 19-56)と
75%(95%CI 55-89)で、プレドニゾロンと本剤併用群で有意に高かった(p= 0.003)
。観察
期間 36 ヵ月時点では、ステロイド単剤群では 45%の症例が奏効(CR 又は PR)を維持して
いたのに対し、プレドニゾロンと本剤併用群では 70%が奏効を維持していた。奏効を認め
た症例の無再発生存期間はプレドニゾロンと本剤併用群で有意に長く(p= 0.02)
、ハザード
比は 0.33(95%CI 0.12-0.88)であった。また、奏効例を対象に登録から非奏効を認めた期
間、又は追跡終了までの期間の赤血球輸血の回数を比較した場合、群間差を認めず、また、
再発や非奏効の場合の脾摘実施例数は、両群で同様であった。
有害事象及び重篤な有害事象(SAE、致死的又は致死的ではない事象)の発現状況は両
群で差を認めず、主な事象は呼吸困難、消化不良、不眠症、頭痛、疲労であり、それらの
多くはプレドニゾロンとの関連性が考えられた。
死亡に至った SAE はプレドニゾロンと本剤併用群で 4 例[肺炎、虚血性脳卒中(2 例)
、
心不全]
、プレドニゾロン単剤群で 3 例(虚血性脳卒中、心不全、殺人犠牲者)であった。
プレドニゾロンと本剤併用群の 1 例で発現した肺炎は、免疫抑制治療による合併症であり
関連性が否定されなかった。他の 6 例の死亡に至った SAE については免疫抑制治療に関連
する事象とは判断されなかった。プレドニゾロンと本剤投与例でアレルギー反応は認めら
れなかった。
2)温式 AIHA を対象としたリツキシマブのランダム化臨床第 III 相試験(RAIHA study)
34)
本試験は、新規に温式 AIHA と診断された 18 歳以上の患者のうち、プレドニゾン治療が
6 週未満の 32 例を対象とした、多施設共同二重盲検プラセボ対照ランダム化臨床第 III 相
32
130 / 359