よむ、つかう、まなぶ。
資料4-2 令和5年度医療機器・再生医療等製品の自主回収一覧[1.6MB] (3 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59564.html |
| 出典情報 | 薬事審議会 医療機器・再生医療等製品安全対策部会(令和7年度第1回 7/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
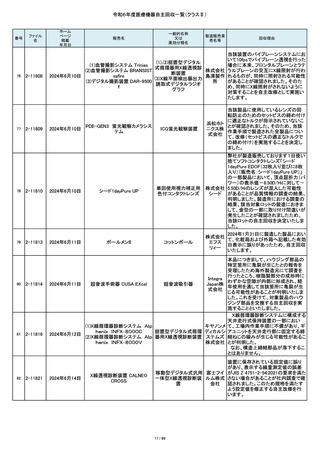
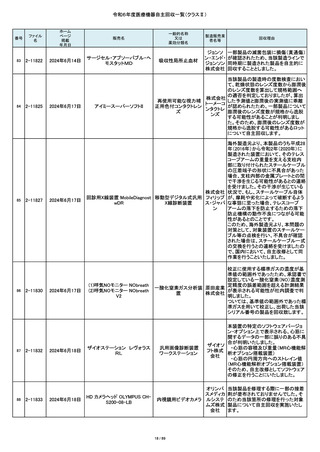
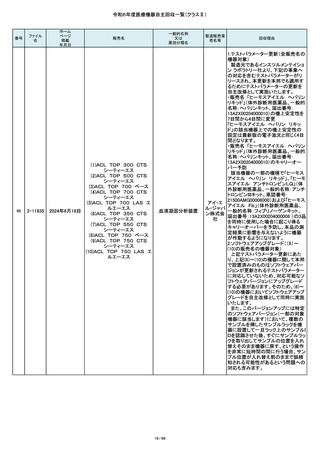
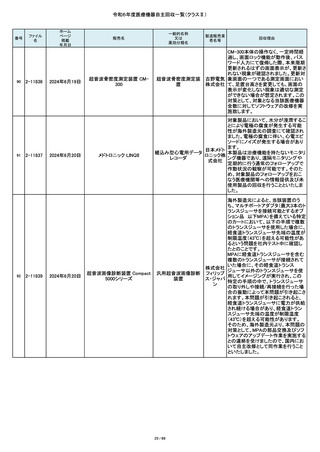
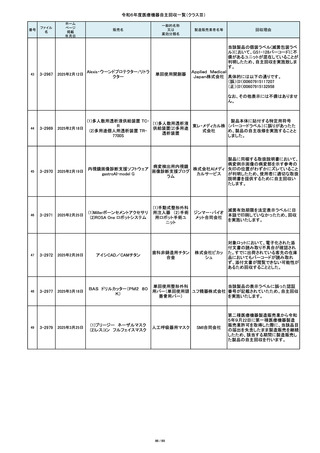
令和6年度医療機器自主回収一覧(クラスⅡ)
番号
7
8
9
10
11
ファイル
名
2-11678
2-11679
2-11681
2-11682
2-11683
ホーム
ページ
掲載
年月日
2024年4月3日
2024年4月4日
一般的名称
又は
薬効分類名
販売名
製造販売業
者名等
回収理由
Epix ユニバーサル クリップアプ
体内用結さつクリップ
ライヤー
外国製造業者であるApplied medical
resources社より、Epix ユニバーサル
オリンパ クリップアプライヤーの特定のロット番
スメディカ 号において、トリガーをハンドル側へ
ルシステ 引いてもクリップが装填されないという
ムズ株式 現象が発生する可能性があるとして、
会社
自主回収を行うとの連絡を受けまし
た。弊社はこの決定を受けて本製品
の自主回収を行うことにいたしました。
三次元動作分析装置 ローカス
3D MAシリーズ
独立行政法人医薬品医療機器総合機
構によるQMS調査において、出荷し
ている製品が承認内容と異なるという
指摘を受けました。実際には、型名
MA-3000において、アイソレーショント
アニマ株
ランスを付属して出荷しておりました。
式会社
このため、お客様に情報提供を行うと
ともに、製品の一部変更承認申請手
続きが完了しましたので、承認事項に
基づく安全性の確認を行うため改修作
業を実施いたします。
生理学的神経筋機能
分析装置(17929000)
アヴェイル LP
海外製造元からの連絡より、市販後
調査のプロセスにおいて、本製品にお
ける、電磁干渉(EMI)によって
Emergency VVI(EVVI)設定またはMRI
設定に移行する可能性があることが
確認されたことから、EMIの影響を軽
減させるためのファームウェア
(FWVer.19.12.00)を提供するとの情報
アボットメ
を入手しました。海外製造元の調査の
植込み型リードレス心 ディカル
結果、当該製品は出荷前に全ての製
臓ペースメーカ
ジャパン
造要件を満たしており、EMIの影響に
合同会社
対する国際・国内規格に適合している
ことを確認しており、本事象は植込み
後の環境との相互作用の結果として
発生していることが確認されました。こ
れらのことから、EMIの影響を軽減させ
るための改善として最新のファーム
ウェア(FW Ver.19.12.00)へのアップ
デートを実施することといたしました。
2024年4月5日
ヘモクロン テストカートリッジ
国内取引先施設よりアクリバ社製「ヘ
モクロン テストカートリッジ(型式:
JACT-LR)の1ロット(J3JLR204)にお
いて、外箱および個包装の表示と異な
る型式(JACT+)のロット(J3JAC247)
凝固測定用経過時間タ 平和物産 が混在していたとの報告を受けまし
イマ
株式会社 た。製造元である米国アクリバ社の原
因究明の結果、製造工程において、
当該ロット製品の一部に異なる製品を
誤って混入したことが判明しました。弊
社では当該ロットの自主回収を決定い
たしました。
2024年4月5日
NexGen CR-FLEX ポーラス
フェモラル
ジンマー・
ファイバーメタルパッドが本品に適切
人工膝関節大腿骨コン バイオメッ
に溶接できていない恐れがあるため、
ポーネント
ト合同会
回収を実施します。
社
2024年4月4日
3 / 89
番号
7
8
9
10
11
ファイル
名
2-11678
2-11679
2-11681
2-11682
2-11683
ホーム
ページ
掲載
年月日
2024年4月3日
2024年4月4日
一般的名称
又は
薬効分類名
販売名
製造販売業
者名等
回収理由
Epix ユニバーサル クリップアプ
体内用結さつクリップ
ライヤー
外国製造業者であるApplied medical
resources社より、Epix ユニバーサル
オリンパ クリップアプライヤーの特定のロット番
スメディカ 号において、トリガーをハンドル側へ
ルシステ 引いてもクリップが装填されないという
ムズ株式 現象が発生する可能性があるとして、
会社
自主回収を行うとの連絡を受けまし
た。弊社はこの決定を受けて本製品
の自主回収を行うことにいたしました。
三次元動作分析装置 ローカス
3D MAシリーズ
独立行政法人医薬品医療機器総合機
構によるQMS調査において、出荷し
ている製品が承認内容と異なるという
指摘を受けました。実際には、型名
MA-3000において、アイソレーショント
アニマ株
ランスを付属して出荷しておりました。
式会社
このため、お客様に情報提供を行うと
ともに、製品の一部変更承認申請手
続きが完了しましたので、承認事項に
基づく安全性の確認を行うため改修作
業を実施いたします。
生理学的神経筋機能
分析装置(17929000)
アヴェイル LP
海外製造元からの連絡より、市販後
調査のプロセスにおいて、本製品にお
ける、電磁干渉(EMI)によって
Emergency VVI(EVVI)設定またはMRI
設定に移行する可能性があることが
確認されたことから、EMIの影響を軽
減させるためのファームウェア
(FWVer.19.12.00)を提供するとの情報
アボットメ
を入手しました。海外製造元の調査の
植込み型リードレス心 ディカル
結果、当該製品は出荷前に全ての製
臓ペースメーカ
ジャパン
造要件を満たしており、EMIの影響に
合同会社
対する国際・国内規格に適合している
ことを確認しており、本事象は植込み
後の環境との相互作用の結果として
発生していることが確認されました。こ
れらのことから、EMIの影響を軽減させ
るための改善として最新のファーム
ウェア(FW Ver.19.12.00)へのアップ
デートを実施することといたしました。
2024年4月5日
ヘモクロン テストカートリッジ
国内取引先施設よりアクリバ社製「ヘ
モクロン テストカートリッジ(型式:
JACT-LR)の1ロット(J3JLR204)にお
いて、外箱および個包装の表示と異な
る型式(JACT+)のロット(J3JAC247)
凝固測定用経過時間タ 平和物産 が混在していたとの報告を受けまし
イマ
株式会社 た。製造元である米国アクリバ社の原
因究明の結果、製造工程において、
当該ロット製品の一部に異なる製品を
誤って混入したことが判明しました。弊
社では当該ロットの自主回収を決定い
たしました。
2024年4月5日
NexGen CR-FLEX ポーラス
フェモラル
ジンマー・
ファイバーメタルパッドが本品に適切
人工膝関節大腿骨コン バイオメッ
に溶接できていない恐れがあるため、
ポーネント
ト合同会
回収を実施します。
社
2024年4月4日
3 / 89