よむ、つかう、まなぶ。
資料4-3 外国での新たな措置の報告状況[1.6MB] (57 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64439.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
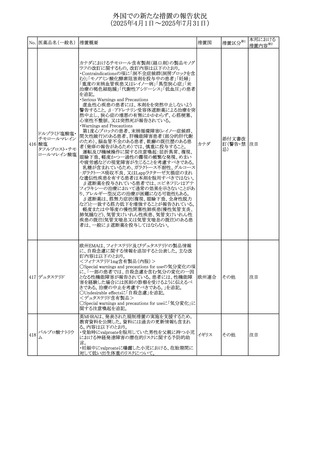
外国での新たな措置の報告状況
(2025年4月1日~2025年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
カナダにおけるチモロール含有製剤(経口剤)の製品モノグ
ラフの改訂に関するもの。改訂内容は以下のとおり。
・Contraindicationsの項に「洞不全症候群(洞房ブロックを含
む)」「モノアミン酸化酵素阻害剤を投与中の患者」「妊婦」
「重度の末梢血管疾患又はレイノー病」「異型狭心症」「未
治療の褐色細胞腫」「代謝性アシドーシス」「低血圧」の患者
を追記。
・Serious Warnings and Precautions
虚血性心疾患の患者には、本剤をを突然中止しないよう
警告すること。β-アドレナリン受容体遮断薬による治療を突
然中止し、狭心症の増悪の有無にかかわらず、心筋梗塞、
心室性不整脈、又は突然死が報告されている。
・Warnings and Precautions
第1度心ブロックの患者、末梢循環障害(レイノー症候群、
ドルゾラミド塩酸塩・
間欠性跛行)のある患者、肝機能障害患者(部分的肝代謝
チモロールマレイン
のため)、脳血管不全のある患者、乾癬の既往歴のある患
416 酸塩
カナダ
者(発疹の報告があるため)では、慎重に投与すること。
タフルプロスト・チモ
運転及び機械操作に関する注意喚起:屈折異常、複視、
ロールマレイン酸塩
眼瞼下垂、軽度かつ一過性の霧視の頻繁な発現、めまい
や疲労感などの視覚障害が生じることを考慮すべきである。
乳糖が含まれているため、ガラクトース不耐性、グルコース
-ガラクトース吸収不良、又はLappラクターゼ欠損症のまれ
な遺伝性疾患を有する患者は本剤を服用すべきではない。
β遮断薬を投与されている患者では、エピネフリンはアナ
フィラキシーの治療において通常の効果を示さないことがあ
り、アレルギー型反応の治療が困難になる可能性もある。
β遮断薬は、筋無力症状(複視、眼瞼下垂、全身性脱力
など)と一致する筋力低下を増強することが報告されている。
軽度または中等度の慢性閉塞性肺疾患(慢性気管支炎、
肺気腫など)、気管支けいれん性疾患、気管支けいれん性
疾患の既往(気管支喘息又は気管支喘息の既往)のある患
者は、一般にβ遮断薬を投与してはならない。
417 デュタステリド
418
バルプロ酸ナトリウ
ム
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
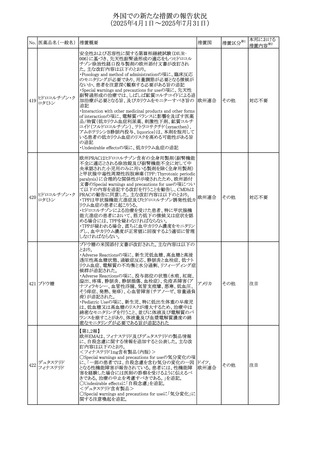
欧州EMAは、フィナステリド及びデュタステリドの製品情報
に、自殺念慮に関する情報を追加すると公表した。主な改
訂内容は以下のとおり。
<フィナステリド1mg含有製品(内服)>
〇Special warnings and precautions for useの気分変化の項
に、「一部の患者では、自殺念慮を含む気分の変化の一因
となる性機能障害が報告されている。患者には、性機能障 欧州連合
害を経験した場合には医師の診察を受けるように伝えるべ
きである。治療の中止を考慮すべきである。」を追記。
〇Undesirable effectsに「自殺念慮」を追記。
<デュタステリド含有製品>
〇Special warnings and precautions for useに「気分変化」に
関する注意喚起を追記。
その他
注目
英MHRAは、発表された規制措置の実施を支援するため,
教育資料を公開した。資料には過去の更新情報も含まれ
る。内容は以下のとおり。
・受胎時にvalproateを服用していた男性を父親に持つ小児
イギリス
における神経発達障害の潜在的リスクに関する予防的助
言。
・妊娠中にvalproateに曝露した小児における、在胎期間に
対して低い出生体重のリスクについて。
その他
注目
57
(2025年4月1日~2025年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
カナダにおけるチモロール含有製剤(経口剤)の製品モノグ
ラフの改訂に関するもの。改訂内容は以下のとおり。
・Contraindicationsの項に「洞不全症候群(洞房ブロックを含
む)」「モノアミン酸化酵素阻害剤を投与中の患者」「妊婦」
「重度の末梢血管疾患又はレイノー病」「異型狭心症」「未
治療の褐色細胞腫」「代謝性アシドーシス」「低血圧」の患者
を追記。
・Serious Warnings and Precautions
虚血性心疾患の患者には、本剤をを突然中止しないよう
警告すること。β-アドレナリン受容体遮断薬による治療を突
然中止し、狭心症の増悪の有無にかかわらず、心筋梗塞、
心室性不整脈、又は突然死が報告されている。
・Warnings and Precautions
第1度心ブロックの患者、末梢循環障害(レイノー症候群、
ドルゾラミド塩酸塩・
間欠性跛行)のある患者、肝機能障害患者(部分的肝代謝
チモロールマレイン
のため)、脳血管不全のある患者、乾癬の既往歴のある患
416 酸塩
カナダ
者(発疹の報告があるため)では、慎重に投与すること。
タフルプロスト・チモ
運転及び機械操作に関する注意喚起:屈折異常、複視、
ロールマレイン酸塩
眼瞼下垂、軽度かつ一過性の霧視の頻繁な発現、めまい
や疲労感などの視覚障害が生じることを考慮すべきである。
乳糖が含まれているため、ガラクトース不耐性、グルコース
-ガラクトース吸収不良、又はLappラクターゼ欠損症のまれ
な遺伝性疾患を有する患者は本剤を服用すべきではない。
β遮断薬を投与されている患者では、エピネフリンはアナ
フィラキシーの治療において通常の効果を示さないことがあ
り、アレルギー型反応の治療が困難になる可能性もある。
β遮断薬は、筋無力症状(複視、眼瞼下垂、全身性脱力
など)と一致する筋力低下を増強することが報告されている。
軽度または中等度の慢性閉塞性肺疾患(慢性気管支炎、
肺気腫など)、気管支けいれん性疾患、気管支けいれん性
疾患の既往(気管支喘息又は気管支喘息の既往)のある患
者は、一般にβ遮断薬を投与してはならない。
417 デュタステリド
418
バルプロ酸ナトリウ
ム
措置区分※1
本邦における
措置内容※2
添付文書改
訂(警告・禁 注目
忌)
欧州EMAは、フィナステリド及びデュタステリドの製品情報
に、自殺念慮に関する情報を追加すると公表した。主な改
訂内容は以下のとおり。
<フィナステリド1mg含有製品(内服)>
〇Special warnings and precautions for useの気分変化の項
に、「一部の患者では、自殺念慮を含む気分の変化の一因
となる性機能障害が報告されている。患者には、性機能障 欧州連合
害を経験した場合には医師の診察を受けるように伝えるべ
きである。治療の中止を考慮すべきである。」を追記。
〇Undesirable effectsに「自殺念慮」を追記。
<デュタステリド含有製品>
〇Special warnings and precautions for useに「気分変化」に
関する注意喚起を追記。
その他
注目
英MHRAは、発表された規制措置の実施を支援するため,
教育資料を公開した。資料には過去の更新情報も含まれ
る。内容は以下のとおり。
・受胎時にvalproateを服用していた男性を父親に持つ小児
イギリス
における神経発達障害の潜在的リスクに関する予防的助
言。
・妊娠中にvalproateに曝露した小児における、在胎期間に
対して低い出生体重のリスクについて。
その他
注目
57