よむ、つかう、まなぶ。
資料4-3 外国での新たな措置の報告状況[1.6MB] (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64439.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
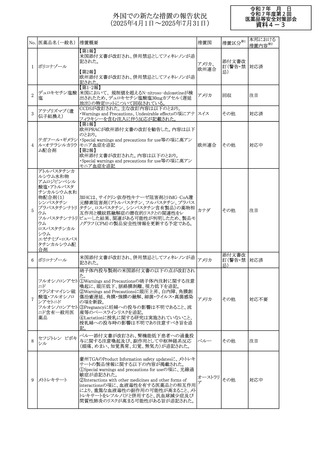
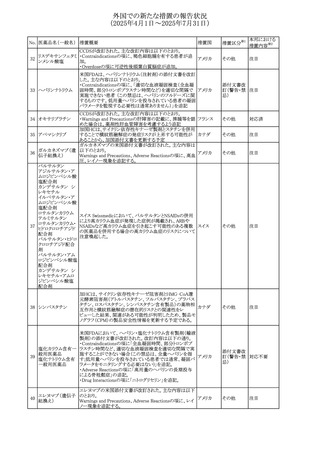
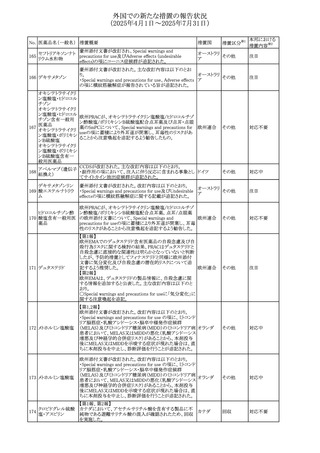
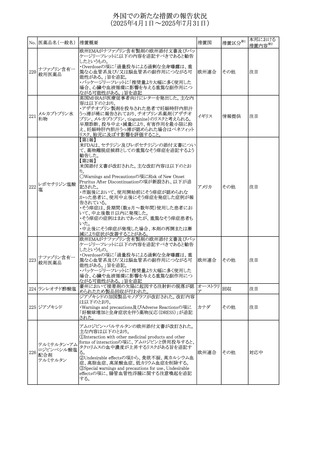
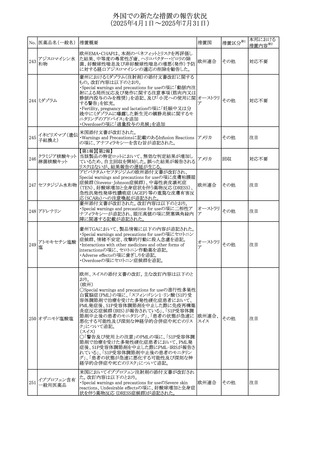
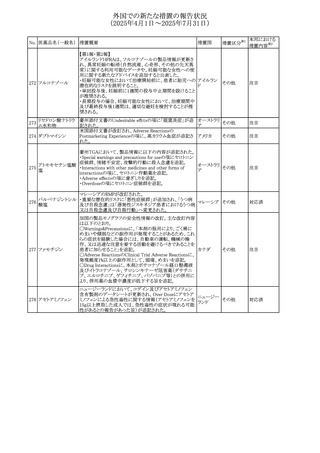
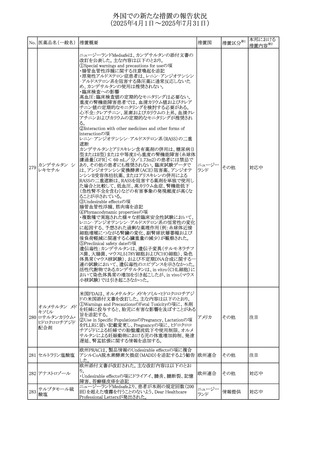
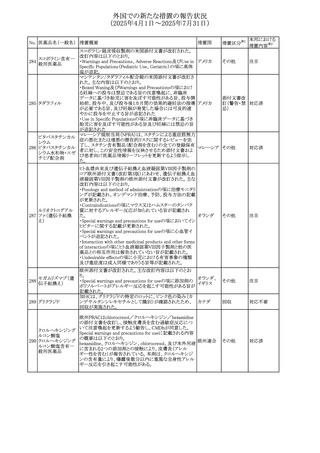
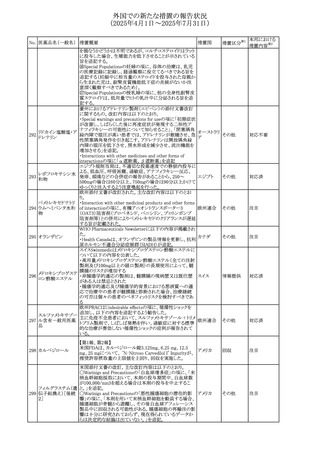
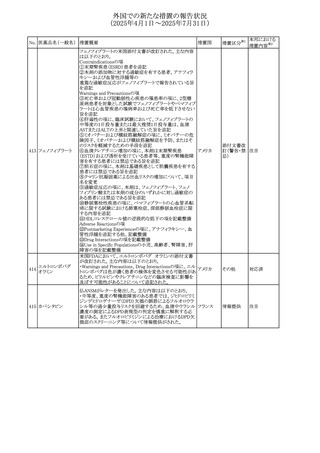
外国での新たな措置の報告状況
(2025年4月1日~2025年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
欧州PRACは、PSURの評価に基づき、サクビトビルバルサル
タンナトリウムの欧州添付文書の改訂を勧告した。主な内容
は以下のとおり。
101 バルサルタン
欧州連合 その他
①母乳中への排泄に関する限られたデータを反映させるた
めに授乳に関する表現を修正する。
②Undesirable effectsの項に、ミオクローヌスを追加する。
欧州EMAにおいて、経鼻弱毒生インフルエンザワクチンの
欧州添付文書及びパッケージリーフレットが改訂された。欧
州添付文書の改訂内容は以下のとおり。
・Special warnings and precautions for use
<過敏症・アナフィラキシー>
他のワクチンと同様に、本剤接種後のアナフィラキシー事象
又は重篤な過敏症事象を管理するために適切な治療管理
が常に実施できるようにしなければならない。
<合併症>
重度の喘息又は現在喘鳴を呈している小児及び青年に本
経鼻弱毒生インフ
102
剤を接種すべきではない。これらの患者は臨床試験で十分 欧州連合 その他
ルエンザワクチン
に研究されていない。
重度の急性熱性疾患又は急性感染症にかかっている者で
は本剤の接種を延期すべきである。
<免疫不全患者>
ワクチン接種者には本剤は弱毒生ワクチンであり、免疫不全
の接触者に伝播する可能性があることを知らせるべきであ
る。
ワクチン接種者は可能な限りワクチン接種後1~2週間は重
度の免疫不全患者との密接な関係を避けるように努めるべ
きである。
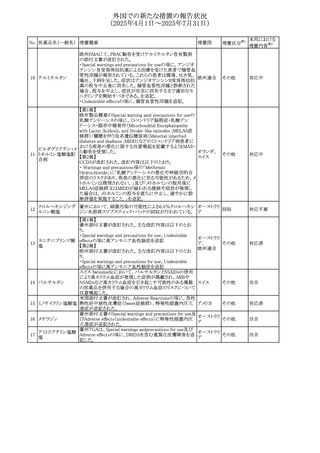
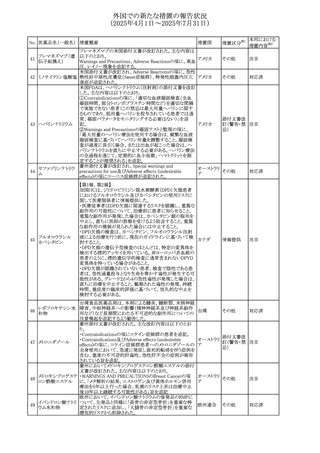
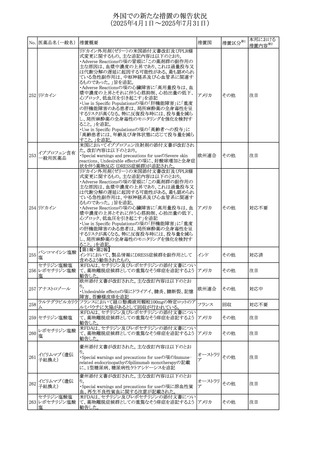
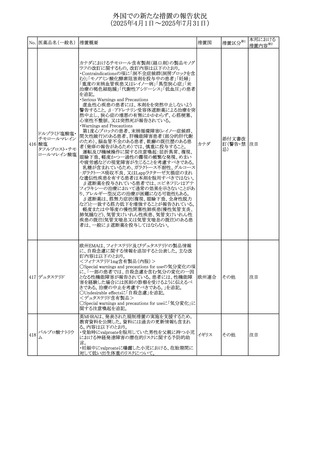
豪州において、特定のロットから検出されたNDMAの濃度
オーストラリ
103 メトホルミン塩酸塩 が、TGAで設定された規制値を超えるか、それに近い値で
回収
ア
あることが確認されたため、回収を開始した。
ガラス粒子が含まれるバイアルが認められたため、回収が行
104 シタラビン
フランス
回収
われている。
カナダで、ボトルを振っても溶解せず、粉砕しにくい大きな
バルプロ酸ナトリウ
105
固体結晶(ショ糖)についての苦情が複数寄せられたことを カナダ
回収
ム
受け、バルプロ酸経口液剤がリコールされている。
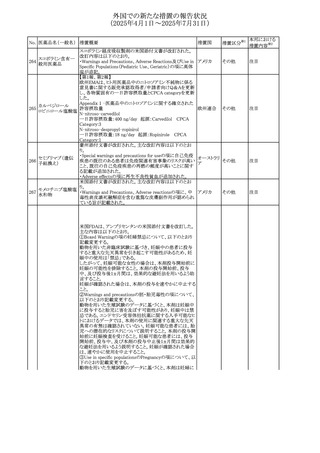
【第1-2報】
クエチアピンフマル 加HCにて、許容限度値を超えるN-nitroso-desalkyl106
カナダ
回収
酸塩
quetiapine (NDAQ)が検出されたため、クエチアピン
XR50mgの2ロットが回収されている。
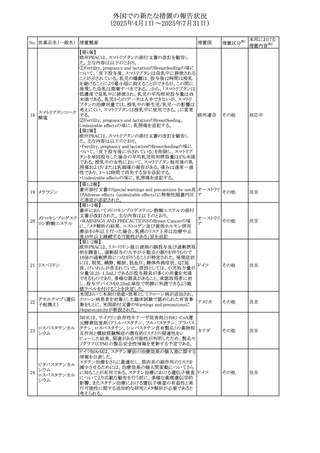
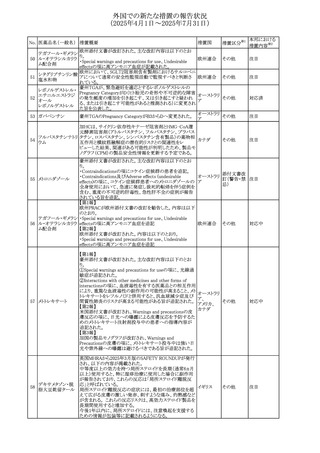
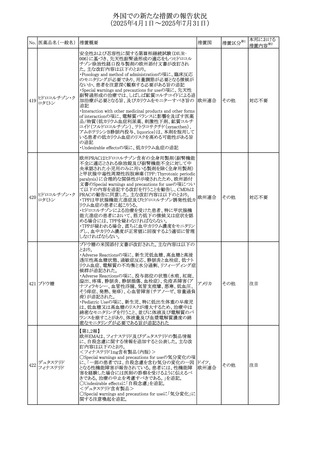
【第1報】
米国添付文書が改訂され、Warnings and Precautions及び
Adverse Reactionsの項に固定薬疹が追加され、汎発性水
テトラサイクリン塩酸 疱性固定薬疹を含む次回投与時の重症度の悪化と関連す アメリカ、
107
その他
塩
る旨追記された。
インド
【第2報】
インドにおいて、製品情報に固定薬疹を副作用として含める
よう勧告された。
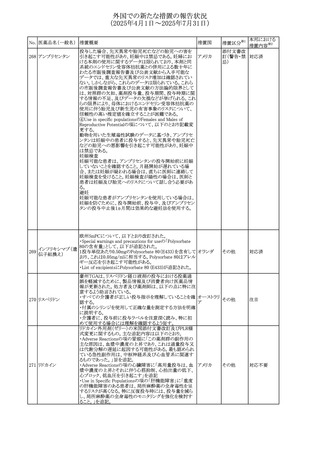
【第1報】
PRACはジクロフェナクを含有する製品(全身投与製剤)の
SmPCを改訂し、Special Warnings and Precautions for Use
の皮膚反応の項に固定薬疹を追記すること、及び、Adverse
Effectsに頻度不明の副作用として固定薬疹を追記すること
を推奨した。
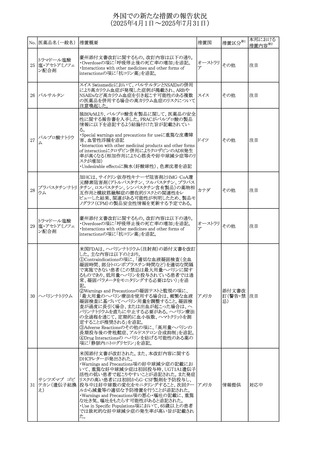
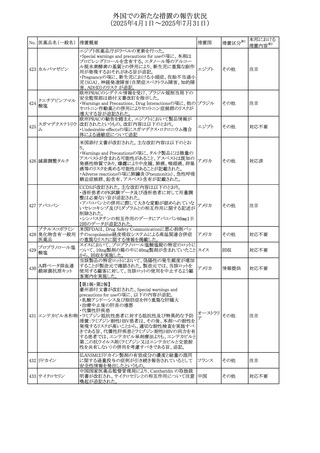
【第2報】
PRACは、2021年10月1日から2024年9月30日までの期間を
対象としたジクロフェナク(全身投与用製剤)のPSURの最終
評価報告書を以て、以下の内容に関して、SmPCを更新する
よう勧告した。
ジクロフェナクナトリ
108
・Special Warnings and Precautions for Useの皮膚反応の項 スイス
その他
ウム
に「汎発性水疱性固定薬疹」を追記。
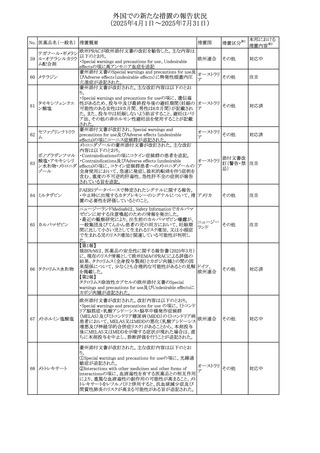
・Adverse Effectに頻度不明の副作用として SOC「皮膚及び
皮下組織障害」に「固定薬疹」及び「汎発性水疱性固定薬
疹」を追記。
【第3報】
CDSが改訂されることが決定した。主な変更内容は以下のと
おり。
・Warnings and Precautionsの項に「汎発性水疱性固定薬
疹」を追記。
・Adverse Drug Reactionsの項に「固定薬疹」及び「汎発性
水疱性固定薬疹」を追記。
13
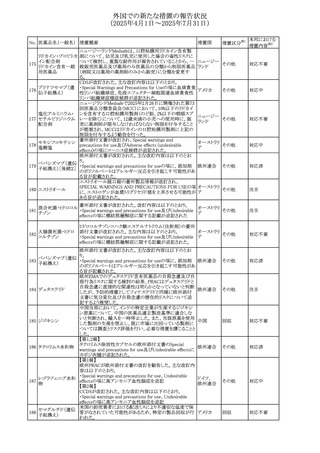
本邦における
措置内容※2
注目
対応済
対応不要
対応不要
対応不要
注目
注目
注目
(2025年4月1日~2025年7月31日)
No. 医薬品名(一般名) 措置概要
措置国
措置区分※1
欧州PRACは、PSURの評価に基づき、サクビトビルバルサル
タンナトリウムの欧州添付文書の改訂を勧告した。主な内容
は以下のとおり。
101 バルサルタン
欧州連合 その他
①母乳中への排泄に関する限られたデータを反映させるた
めに授乳に関する表現を修正する。
②Undesirable effectsの項に、ミオクローヌスを追加する。
欧州EMAにおいて、経鼻弱毒生インフルエンザワクチンの
欧州添付文書及びパッケージリーフレットが改訂された。欧
州添付文書の改訂内容は以下のとおり。
・Special warnings and precautions for use
<過敏症・アナフィラキシー>
他のワクチンと同様に、本剤接種後のアナフィラキシー事象
又は重篤な過敏症事象を管理するために適切な治療管理
が常に実施できるようにしなければならない。
<合併症>
重度の喘息又は現在喘鳴を呈している小児及び青年に本
経鼻弱毒生インフ
102
剤を接種すべきではない。これらの患者は臨床試験で十分 欧州連合 その他
ルエンザワクチン
に研究されていない。
重度の急性熱性疾患又は急性感染症にかかっている者で
は本剤の接種を延期すべきである。
<免疫不全患者>
ワクチン接種者には本剤は弱毒生ワクチンであり、免疫不全
の接触者に伝播する可能性があることを知らせるべきであ
る。
ワクチン接種者は可能な限りワクチン接種後1~2週間は重
度の免疫不全患者との密接な関係を避けるように努めるべ
きである。
豪州において、特定のロットから検出されたNDMAの濃度
オーストラリ
103 メトホルミン塩酸塩 が、TGAで設定された規制値を超えるか、それに近い値で
回収
ア
あることが確認されたため、回収を開始した。
ガラス粒子が含まれるバイアルが認められたため、回収が行
104 シタラビン
フランス
回収
われている。
カナダで、ボトルを振っても溶解せず、粉砕しにくい大きな
バルプロ酸ナトリウ
105
固体結晶(ショ糖)についての苦情が複数寄せられたことを カナダ
回収
ム
受け、バルプロ酸経口液剤がリコールされている。
【第1-2報】
クエチアピンフマル 加HCにて、許容限度値を超えるN-nitroso-desalkyl106
カナダ
回収
酸塩
quetiapine (NDAQ)が検出されたため、クエチアピン
XR50mgの2ロットが回収されている。
【第1報】
米国添付文書が改訂され、Warnings and Precautions及び
Adverse Reactionsの項に固定薬疹が追加され、汎発性水
テトラサイクリン塩酸 疱性固定薬疹を含む次回投与時の重症度の悪化と関連す アメリカ、
107
その他
塩
る旨追記された。
インド
【第2報】
インドにおいて、製品情報に固定薬疹を副作用として含める
よう勧告された。
【第1報】
PRACはジクロフェナクを含有する製品(全身投与製剤)の
SmPCを改訂し、Special Warnings and Precautions for Use
の皮膚反応の項に固定薬疹を追記すること、及び、Adverse
Effectsに頻度不明の副作用として固定薬疹を追記すること
を推奨した。
【第2報】
PRACは、2021年10月1日から2024年9月30日までの期間を
対象としたジクロフェナク(全身投与用製剤)のPSURの最終
評価報告書を以て、以下の内容に関して、SmPCを更新する
よう勧告した。
ジクロフェナクナトリ
108
・Special Warnings and Precautions for Useの皮膚反応の項 スイス
その他
ウム
に「汎発性水疱性固定薬疹」を追記。
・Adverse Effectに頻度不明の副作用として SOC「皮膚及び
皮下組織障害」に「固定薬疹」及び「汎発性水疱性固定薬
疹」を追記。
【第3報】
CDSが改訂されることが決定した。主な変更内容は以下のと
おり。
・Warnings and Precautionsの項に「汎発性水疱性固定薬
疹」を追記。
・Adverse Drug Reactionsの項に「固定薬疹」及び「汎発性
水疱性固定薬疹」を追記。
13
本邦における
措置内容※2
注目
対応済
対応不要
対応不要
対応不要
注目
注目
注目