よむ、つかう、まなぶ。
資料4-3 外国での新たな措置の報告状況[1.6MB] (26 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64439.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第2回 10/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
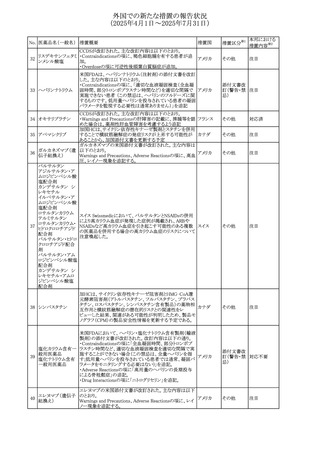
外国での新たな措置の報告状況
(2025年4月1日~2025年7月31日)
措置区分※1
本邦における
措置内容※2
その他
注目
その他
対応不要
その他
注目
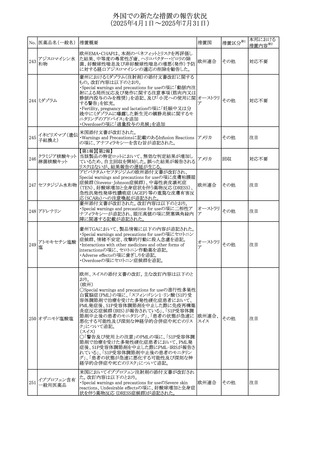
【第1-2報】
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項にセロトニン
アトモキセチン塩酸 症候群、情緒不安定、攻撃的行動に殺人念慮を追記。
オーストラリ
230
その他
塩
・Interactions with other medicines and other forms of
ア
interactionsの項に、セロトニン作動薬を追記。
・Adverse effectsの項に歯ぎしりを追記。
・Overdoseの項にセロトニン症候群を追記。
注目
セチリジン塩酸塩 米FDAは、セチリジン及びレボセチリジンの添付文書につい
231 レボセチリジン塩酸 て、薬物離脱症候群としての重篤なそう痒症を追記するよう アメリカ
塩
勧告した。
注目
No. 医薬品名(一般名) 措置概要
措置国
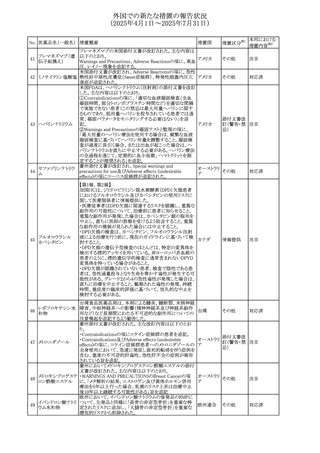
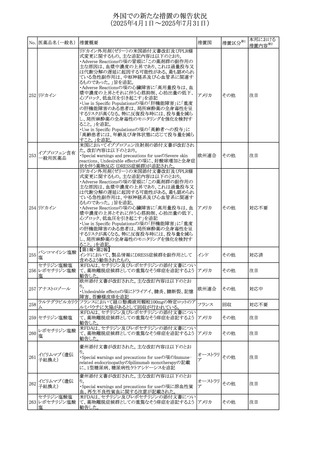
欧州EMAがナファゾリン含有製剤の欧州添付文書及びパッ
ケージリーフレットに以下の内容を追記したというもの。
・Overdoseの項に「過量投与による過剰な全身曝露は、重
篤な心血管系及び/又は脳血管系の副作用につながる可
227 ナファゾリン硝酸塩
欧州連合
能性がある。」旨を追記。
・パッケージリーフレットに「推奨量より大幅に多く使用した
場合、心臓や血液循環に影響を与える重篤な副作用につ
ながる可能性がある。」旨を追記
リドカイン外用剤(ゼリー)の米国添付文書改訂及びPLR様
式変更に関するもの。主な追記内容は以下のとおり。
・Adverse Reactionsの項の冒頭に「この薬剤群の副作用の
主な原因は、血漿中濃度の上昇であり、これは過量投与又
は代謝分解の遅延に起因する可能性がある。最も認められ
ている急性副作用は、中枢神経系及び心血管系に関連す
るものであった。」旨を追記。
228 リドカイン塩酸塩
・Adverse Reactionsの項の心臓障害に「高用量投与は、血 アメリカ
漿中濃度の上昇とそれに伴う心筋抑制、心拍出量の低下、
心ブロック、低血圧を引き起こす」を追記
・Use in Specific Populationsの項の「肝機能障害」に「重度
の肝機能障害のある患者は、局所麻酔薬の全身毒性を呈
するリスクが高くなる。特に反復投与時には、投与量を減ら
し、局所麻酔薬の全身毒性のモニタリングを強化を検討す
ること。」を追記。
セチリジン塩酸塩 米FDAは、セチリジン及びレボセチリジンの添付文書につい
229 レボセチリジン塩酸 て、薬物離脱症候群としての重篤なそう痒症を追記するよう アメリカ
塩
勧告した。
232 アザチオプリン
233 ドラビリン
234 ドラビリン
235
組換えRSウイルス
ワクチン
その他
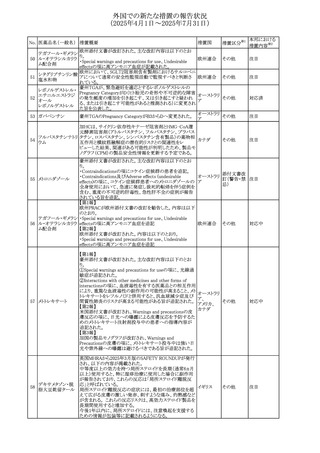
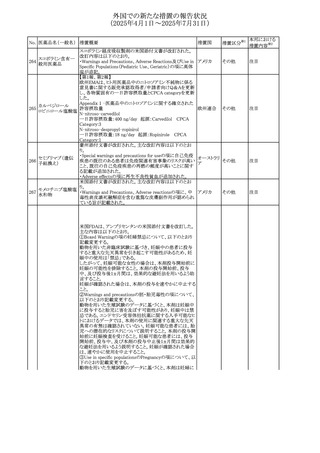
【第1報】
英国MHRAは、チオプリン製剤による妊娠中肝内胆汁うっ滞
の稀なリスクについて医療従事者に注意喚起を行った。
サウジアラ
【第2報】
ビア、
情報提供
サウジアラビアSFDAは、チオプリン製剤による妊娠中肝内 イギリス
胆汁うっ滞に対する注意喚起を含めるために、添付文書を
改訂するよう要請した。
【第1報・第2報・第3報】
米国添付文書が改訂され、Warnings and Precautionsに重
アメリカ
その他
度の皮膚障害として、スティーブンス・ジョンソン症候群(SJS)
及び中毒性表皮壊死融解症(TEN)が追記された。
【第1報・第2報】
ドラビリン/ラミブジ/テノホビル ジソプロキシル配合剤の,
米国添付文書が改訂され、Warnings and Precautionsにドラ
アメリカ
その他
ビリンによる重度の皮膚障害として、スティーブンス・ジョンソ
ン症候群(SJS)及び中毒性表皮壊死融解症(TEN)が追記さ
れた。
豪州TGAのホームページより、RSウイルスワクチンの安全性
情報が更新され、ワクチン接種後のギラン・バレー症候群の
リスク(低リスク)について反映された。
製品情報の改訂内容は以下のとおり。
オーストラリ
その他
・Special warnings and precautions for useの項にギラン・バ ア
レー症候群が追記された。
・Adverse effectsの項にギラン・バレー症候群が追記され
た。
26
注目
注目
注目
注目
(2025年4月1日~2025年7月31日)
措置区分※1
本邦における
措置内容※2
その他
注目
その他
対応不要
その他
注目
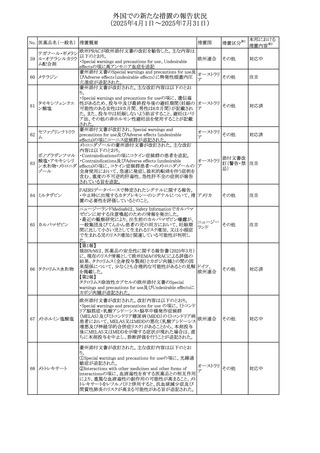
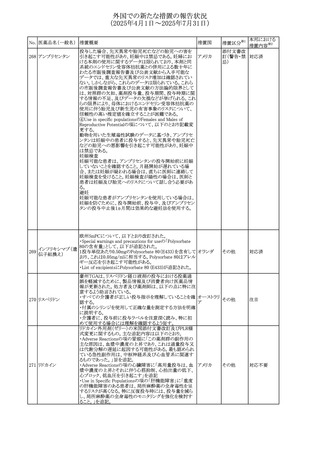
【第1-2報】
豪州TGAにおいて、製品情報に以下の内容が追記された。
・Special warnings and precautions for useの項にセロトニン
アトモキセチン塩酸 症候群、情緒不安定、攻撃的行動に殺人念慮を追記。
オーストラリ
230
その他
塩
・Interactions with other medicines and other forms of
ア
interactionsの項に、セロトニン作動薬を追記。
・Adverse effectsの項に歯ぎしりを追記。
・Overdoseの項にセロトニン症候群を追記。
注目
セチリジン塩酸塩 米FDAは、セチリジン及びレボセチリジンの添付文書につい
231 レボセチリジン塩酸 て、薬物離脱症候群としての重篤なそう痒症を追記するよう アメリカ
塩
勧告した。
注目
No. 医薬品名(一般名) 措置概要
措置国
欧州EMAがナファゾリン含有製剤の欧州添付文書及びパッ
ケージリーフレットに以下の内容を追記したというもの。
・Overdoseの項に「過量投与による過剰な全身曝露は、重
篤な心血管系及び/又は脳血管系の副作用につながる可
227 ナファゾリン硝酸塩
欧州連合
能性がある。」旨を追記。
・パッケージリーフレットに「推奨量より大幅に多く使用した
場合、心臓や血液循環に影響を与える重篤な副作用につ
ながる可能性がある。」旨を追記
リドカイン外用剤(ゼリー)の米国添付文書改訂及びPLR様
式変更に関するもの。主な追記内容は以下のとおり。
・Adverse Reactionsの項の冒頭に「この薬剤群の副作用の
主な原因は、血漿中濃度の上昇であり、これは過量投与又
は代謝分解の遅延に起因する可能性がある。最も認められ
ている急性副作用は、中枢神経系及び心血管系に関連す
るものであった。」旨を追記。
228 リドカイン塩酸塩
・Adverse Reactionsの項の心臓障害に「高用量投与は、血 アメリカ
漿中濃度の上昇とそれに伴う心筋抑制、心拍出量の低下、
心ブロック、低血圧を引き起こす」を追記
・Use in Specific Populationsの項の「肝機能障害」に「重度
の肝機能障害のある患者は、局所麻酔薬の全身毒性を呈
するリスクが高くなる。特に反復投与時には、投与量を減ら
し、局所麻酔薬の全身毒性のモニタリングを強化を検討す
ること。」を追記。
セチリジン塩酸塩 米FDAは、セチリジン及びレボセチリジンの添付文書につい
229 レボセチリジン塩酸 て、薬物離脱症候群としての重篤なそう痒症を追記するよう アメリカ
塩
勧告した。
232 アザチオプリン
233 ドラビリン
234 ドラビリン
235
組換えRSウイルス
ワクチン
その他
【第1報】
英国MHRAは、チオプリン製剤による妊娠中肝内胆汁うっ滞
の稀なリスクについて医療従事者に注意喚起を行った。
サウジアラ
【第2報】
ビア、
情報提供
サウジアラビアSFDAは、チオプリン製剤による妊娠中肝内 イギリス
胆汁うっ滞に対する注意喚起を含めるために、添付文書を
改訂するよう要請した。
【第1報・第2報・第3報】
米国添付文書が改訂され、Warnings and Precautionsに重
アメリカ
その他
度の皮膚障害として、スティーブンス・ジョンソン症候群(SJS)
及び中毒性表皮壊死融解症(TEN)が追記された。
【第1報・第2報】
ドラビリン/ラミブジ/テノホビル ジソプロキシル配合剤の,
米国添付文書が改訂され、Warnings and Precautionsにドラ
アメリカ
その他
ビリンによる重度の皮膚障害として、スティーブンス・ジョンソ
ン症候群(SJS)及び中毒性表皮壊死融解症(TEN)が追記さ
れた。
豪州TGAのホームページより、RSウイルスワクチンの安全性
情報が更新され、ワクチン接種後のギラン・バレー症候群の
リスク(低リスク)について反映された。
製品情報の改訂内容は以下のとおり。
オーストラリ
その他
・Special warnings and precautions for useの項にギラン・バ ア
レー症候群が追記された。
・Adverse effectsの項にギラン・バレー症候群が追記され
た。
26
注目
注目
注目
注目