資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (96 ページ)
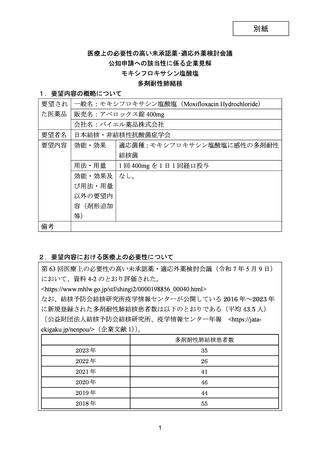
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
6.2.2 Medicines used in longer MDR-TB treatment regimens
(注)これら 2 項では、WHO ガイドライン(2025)の推奨内容と同様の記
述がなされているので、本項では記載を省略する。
なお、6 ヵ月レジメン及び 9 ヵ月レジメンにおいて、MFLX を含む各薬剤
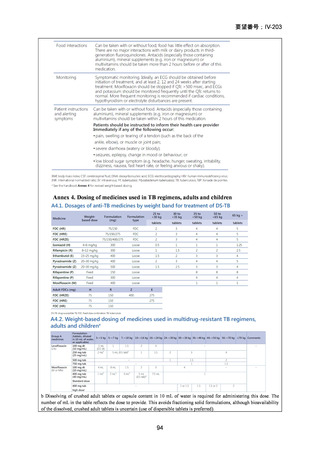
の用法・用量は Annex 4 の“Dosing of medicines used in TB regimens, adults
and children”参照としているので、Annex 4 の MFLX で該当する記載(A4.2)
を、Annex 1. Tuberculosis medicine information sheets の MFLX の項と共に示
す。いずれにおいても、成人結核患者における MFLX の推奨用量として、
400mg/日が示されている。
Annex 1. Tuberculosis medicine information sheets
92