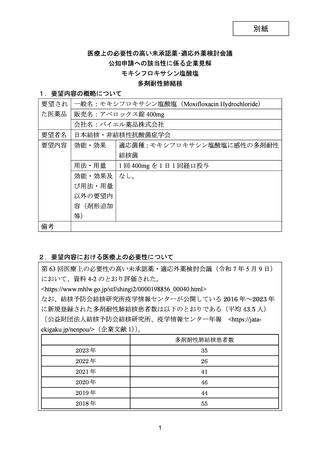
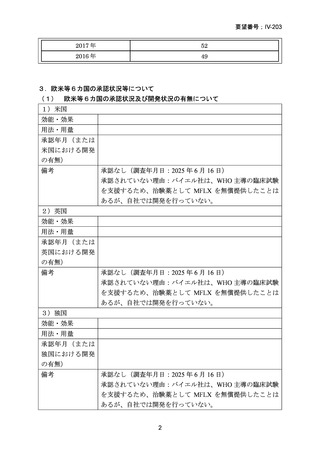
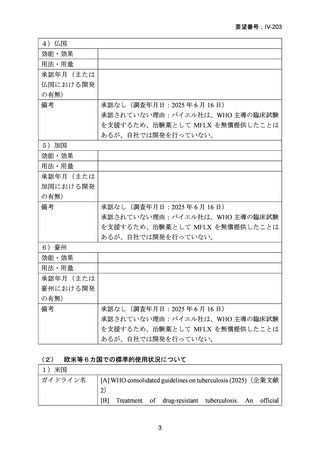
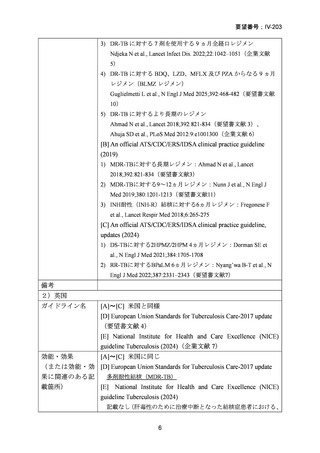
資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (18 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
公表時期: 2020 年 1 月 1 日以降
検索実施日:2025 年 10 月 9 日
上記の手法で抽出された 29 件から 5 件の国外報告(企業文献 16、18~21)、前
項の薬物動態に関する文献検索結果で抽出された 2 件の国外報告(企業文献
11、17)及び別途抽出した 1 件の国内報告(企業文献 22)を選択した(本企業
見解 60~63 頁)。
<海外における臨床試験等>
薬剤耐性結核(DR-TB)に関する MFLX の海外臨床試験については、WHO ガイド
ライン update(2025)及び ATS/CDC/ERS/IDS 合同ガイドライン update(2024)での
BPaLM レジメン〔ベダキリン(BDQ)、プレトマニド、リネゾリド(LZD)及び MFLX〕
推奨の根拠となった、リファンピン(以後、リファンピシンと共に「RFP」と表示す
る)耐性結核(RR-TB)患者を対象とした第Ⅱ/Ⅲ相 TB-PRACTECAL 試験(要望
書文献 7)、RR-TB でフルオロキノロン(FQ)感受性の患者を対象として、MFLX を
含む BLMZ レジメン(BDQ、LZD、MFLX 及び PZA)等 5 つのレジメンと標準治療
を比較した第Ⅲ相 endTB 試験(要望書文献 10)、RR-TB 患者を対象として MFLX を
含む 7 剤併用療法を検討した第Ⅲ相 STREAM 試験(要望書文献 11)が、RR-TB 及
び MDR-TB に対する MFLX の有用性を示す臨床試験成績として、学会要望書に記載
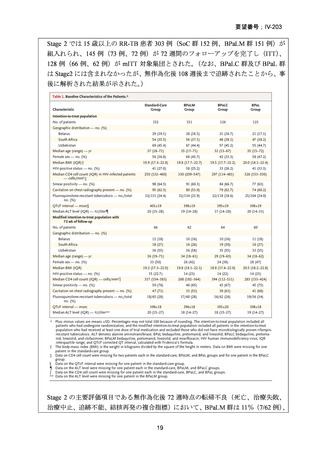
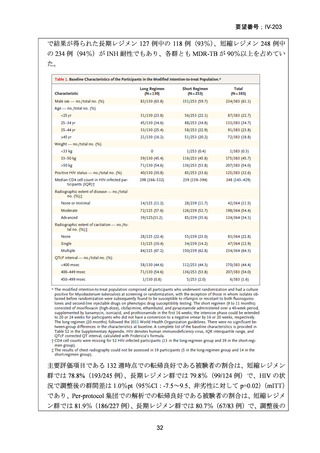
されている。TB-PRACTECAL 試験、endTB 試験及び STREAM 試験はいずれも RRTB 患者を対象としているが、各試験における INH 耐性の被験者割合は 80%を超え
ており、MDR-TB に対する治療レジメンの評価に資するエビデンスと考えられる。
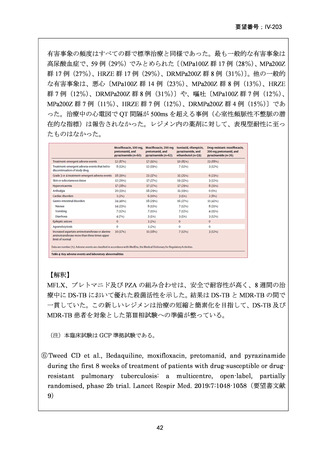
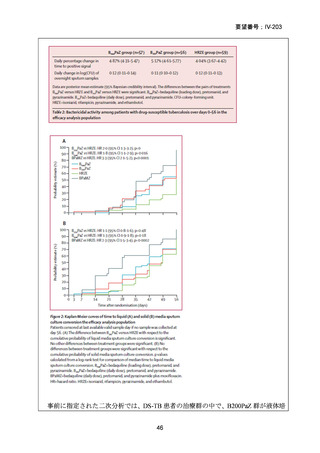
TB-PRACTECAL 試験は RR-TB 患者を対象として実施され、Stage 1 では BPaLM、
BPaLC(BDQ、プレトマニド、LZD、CFZ)及び BPaL(BDQ、プレトマニド、LZD)
の 3 レジメンが比較された。Stage 2 ではその結果に基づいて選択された BPaLM レ
ジメンが標準治療(9 ヵ月短縮レジメン又は 18 ヵ月長期レジメン)と比較され、有効
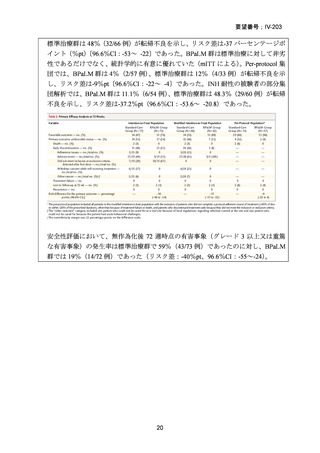
性主要評価項目の無作為化後 72 週時点での転帰不良に関して、BPaLM レジメンの
標準治療に対する非劣性と統計学的に有意なリスク低減効果が示されている〔11%
vs 48%、リスク差:-37 パーセンテージポイント(%pt)(96.6%信頼区間(CI):-53
~-22)〕。安全性についても、無作為化後 72 週時点の有害事象(AE)
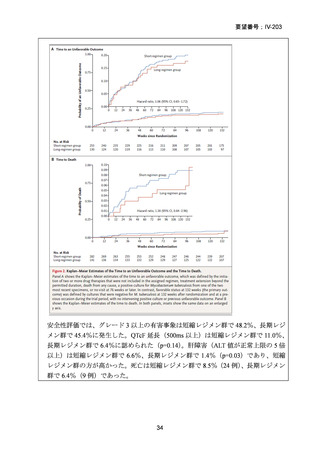
〔グレード 3 以
上又は重篤な AE
(SAE)〕の発現割合は BPaLM 群で標準治療群よりも低かった〔19%
vs 59%、リスク差:-40%pt(96.6%CI:-55~-24)〕。
endTB 試験は RR-TB 患者を対象として実施され、BLMZ、BCLLfxZ(BDQ、CFZ、
LZD、LVFX 及び PZA)、BDLLfxZ〔BDQ、デラマニド(DLM)、LZD、LVFX 及び
PZA〕、DCLLfxZ(DLM、CFZ、LZD、LVFX 及び PZA)及び DCMZ(DLM、CFZ、
MFLX 及び PZA)の 5 つの 9 ヵ月レジメンが 18~24 ヵ月の標準治療と比較された。
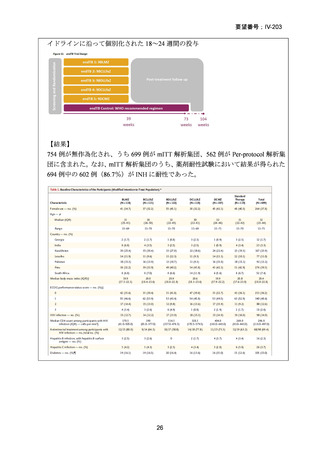
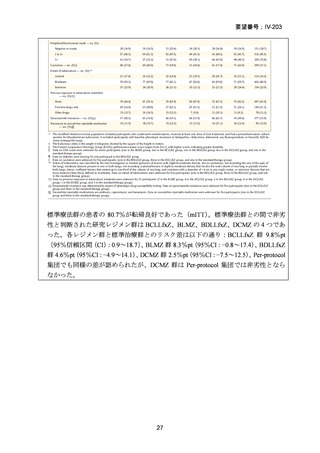
有効性主要評価項目とされた、無作為化後 73 週時点で良好な治療転帰を示した被験
14