資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (139 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
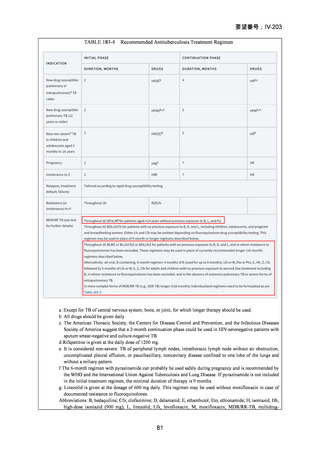
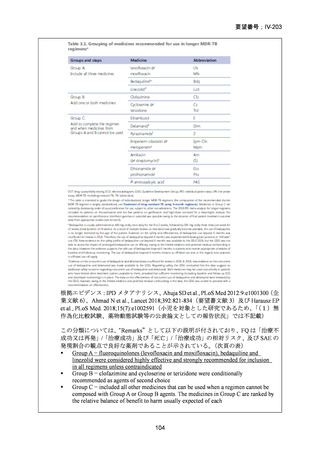
4 ヵ月目以降も陽性)には、治療失敗や薬剤抵抗性の獲得の可能性について調査を
行う必要がある。6 ヵ月目以降も改善がみられない場合(臨床的に、又は喀痰培養
が陽性)には、レジメンを中止する。
レジメン開始後に、FQ 抵抗性、又は、BDQ もしくは LZD に抵抗性が発生した場
合は治療失敗とみなされ、レジメンは中止される。
有害事象により投与量が修正できるのは LZD のみである。他の構成薬剤では投
与量の修正はできずに中止となる。LZD の用量 600mg は、投与開始から 16 週間ま
でであれば、有害事象により 300mg に減量できる。投与開始から 9 週間までは減量
や中止をしないことが望ましく、喀痰培養の陰性化、臨床症状の解消、又は X 線検
査による悪化がないことを示す良好な臨床反応がある場合に限る。
有害事象により PZA 又は LZD の中止が考慮される場合、残りの薬剤でレジメン
を継続することはできるが、複数薬剤を中止する必要は、レジメンを中止する。
許容されるレジメンの中断期間
有害事象や臨床検査値異常により、レジメンが中断される場合、患者の状態が許
容できる限り、できるだけ早く治療を再開すべきとされている。レジメンの中断が
7 日間を超えて 1 ヵ月未満である場合は、中断期間を補完するために延長する必要
がある。延長した場合には治療期間全体として 11 ヵ月で完了する必要があるが、
ケースバイケースで評価されるべきであるとしている。レジメン後半の中断は、治
療の結果に対してより大きな悪影響がある。一方、レジメン初期の中断は、30 日未
満であっても、レジメン構成薬剤のすべてに対して即座に再度 DST を行い、潜在的
な抵抗性を評価して、新しい治療レジメンへ切り替えの必要性を判断しなければな
らない。
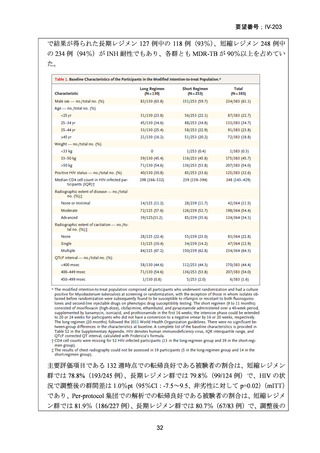
BLMZ レジメンの endTB 試験における有効性
endTB 試験では、WHO ガイドライン(2016、2019 及び 2022)に従った地域の標
準治療(18~24 ヵ月長期レジメン又は 9 ヵ月短縮レジメン)が対照群に設定され
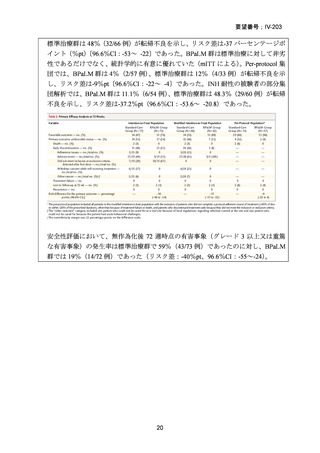
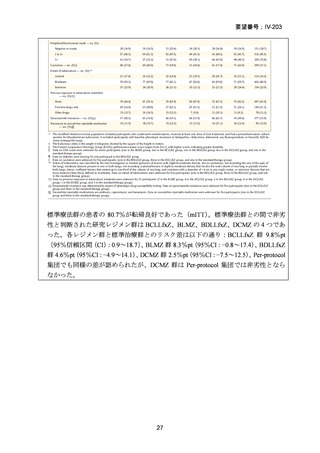
た。標準治療群の患者では 80.7%が転帰良好を示し、BLMZ 群は標準治療群に対し
て非劣性と判断され、BLMZ レジメン群と標準治療群とのリスク差は 8.3%pt(95%
CI:−0.8~17.4)であった(mITT)。
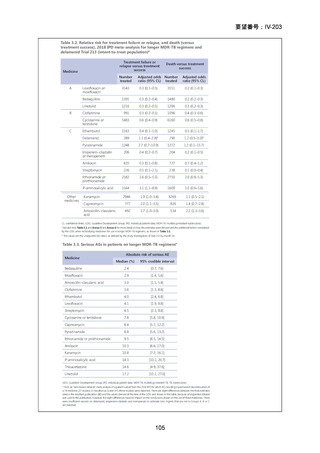
また、9 ヵ月 BLMZ レジメンは標準治療に比べて、治療成功率が高く(89.0% vs.
80.7%)、転帰不良の割合が低く(11.0% vs. 19.3%)、治療失敗又は追跡不能の割合が
低い(2.5% vs. 6.7%)ことが示された。対照群であった標準治療群での主な処方薬
は、LVFX(95.0%)、BDQ(80.7%)、CFZ(79.0%)、LZD(72.3%)、CS/テリジド
ン(71.4%)であった。また、処方薬の中で抗結核薬として日本で使用できない(販
売されていない)のはカプレオマイシン(10.9%)のみであり、処方された割合に
ついても大きくなかった。
よって、対照群とされた標準治療は、日本で MDR-TB の治療薬として処方される
薬剤と概ね一致していると考えられ、本試験で認められた BLMZ 群の標準治療群に
135