資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (60 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
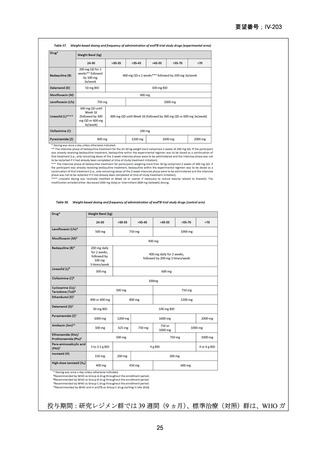
は、FQ、BDQ、LZD、CFZ 及び CS の 6 ヵ月間投与後に FQ、LZD、CFZ 及び CS を
18 ヵ月間投与するレジメンで治療された〔WHO ガイドライン(2019)及び中国の
推奨レジメン〕。AE は治療期間を通してモニタリングされ、薬剤曝露量(AUC0-24
等)との関係を評価した。AE 発現に係る薬物動態予測因子の閾値は、Classification
and Regression Tree (CART)解析で特定した。閾値の validation を、BDQ、MFLX、
LZD、CFZ 及び CS を含むレジメンで 6 ヵ月間の治療を受けた別のコホートで行っ
た。
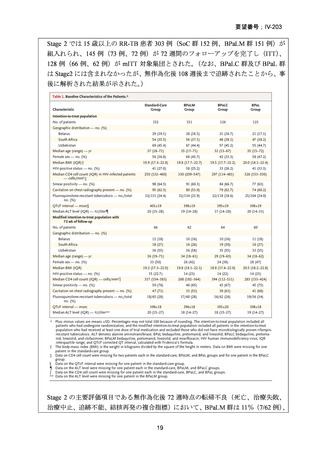
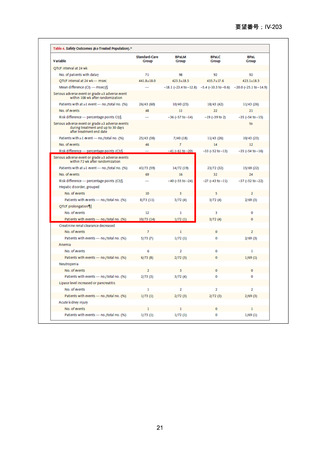
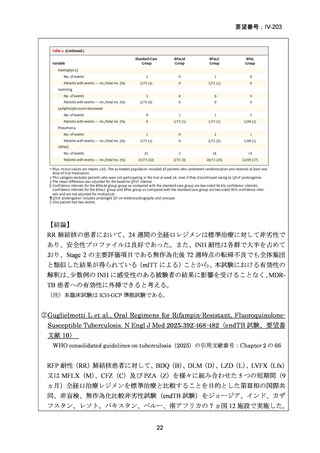
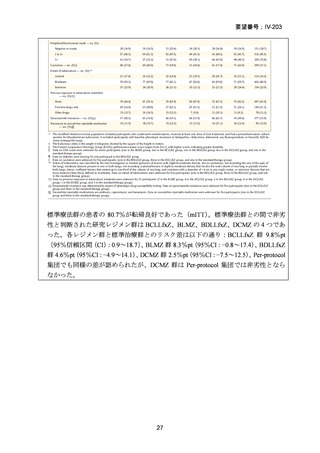
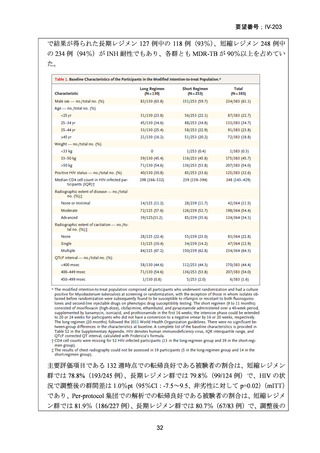
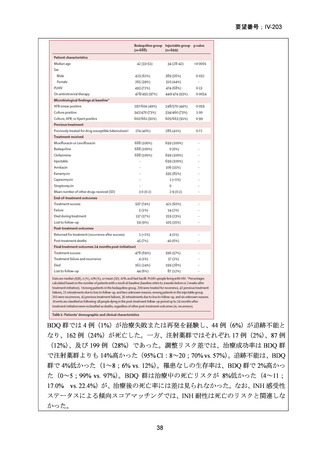
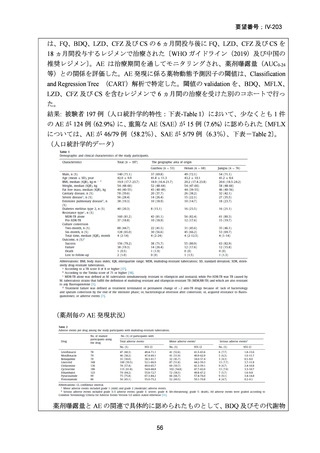
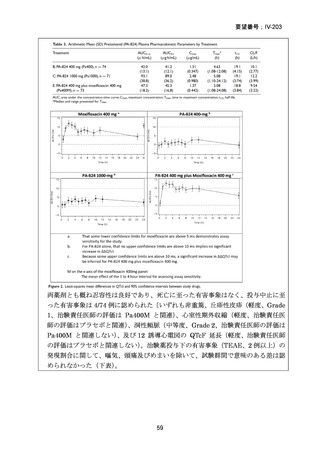
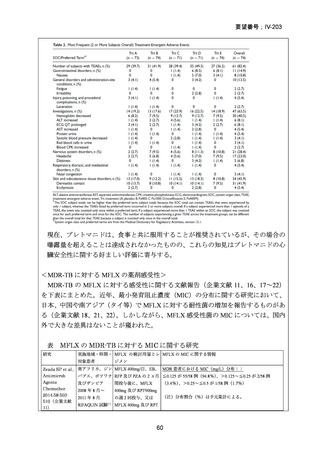
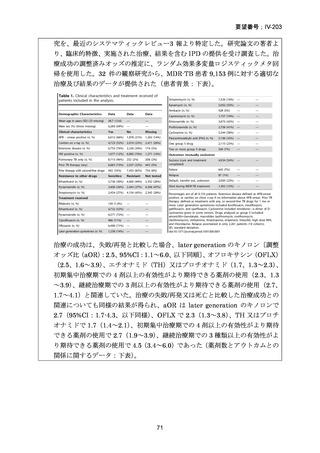
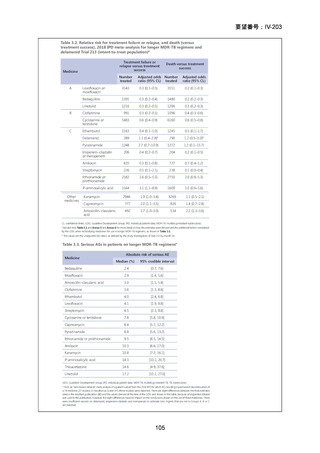
結果: 被験者 197 例(人口統計学的特性:下表-Table 1)において、少なくとも 1 件
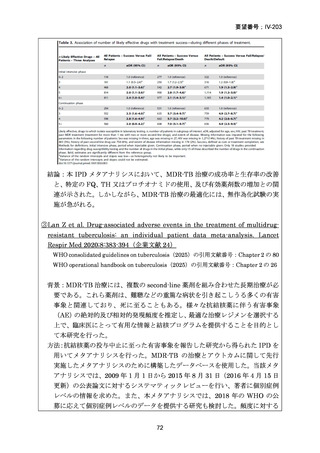
の AE が 124 例(62.9%)に、重篤な AE(SAE)が 15 例(7.6%)に認められた〔MFLX
については、AE が 46/79 例(58.2%)、SAE が 5/79 例(6.3%)、下表-Table 2〕。
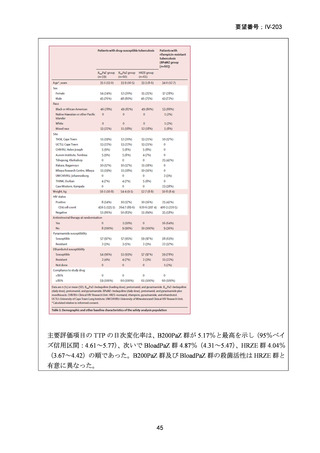
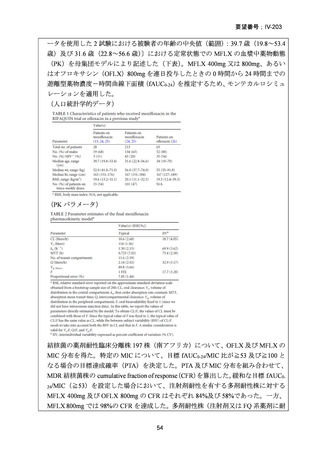
(人口統計学的データ)
(薬剤毎の AE 発現状況)
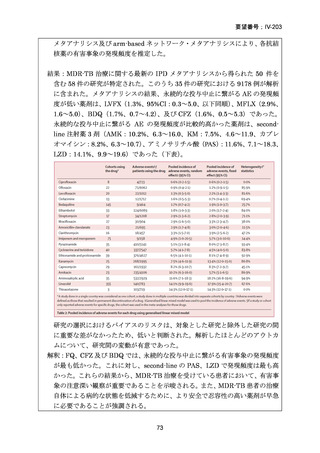
薬剤曝露量と AE の関連で具体的に認められたものとして、BDQ 及びその代謝物
56