資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (12 ページ)
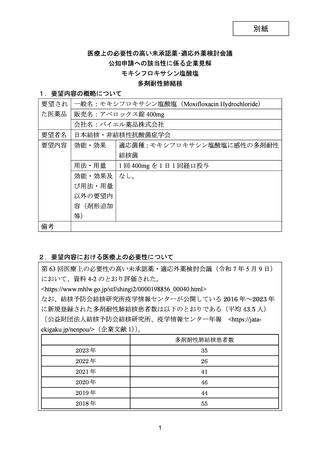
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
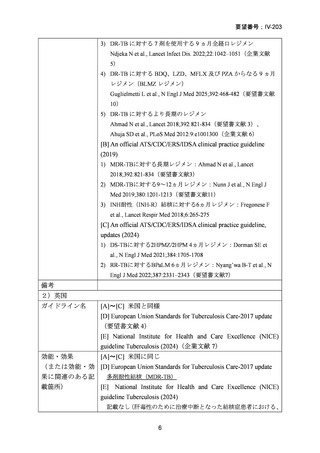
では MFLX の具体的な用法・用量は示されていない。
[E] National Institute for Health and Care Excellence (NICE)
guideline Tuberculosis (2024)
記載なし
ガイドラインの根 [A]~[C] 米国と同じ
拠論文
[D] European Union Standards for Tuberculosis Care-2017 update
以下のガイドラインが参照されているが、個別の臨床試験やメタア
ナリシスの成績は引用されていない。
1) 20~24ヵ月レジメン
World Health Organization. Compendium of WHO guidelines and
associated standards: ensuring optimum delivery of the cascade of
care for patients with tuberculosis. Geneva: World Health
Organization; 2017
World Health Organization. WHO treatment guidelines for drugresistant tuberculosis: 2016 update. Geneva: World Health
Organization; 2016.
2) 9~12ヵ月短縮レジメン
World Health Organization. Compendium of WHO guidelines and
associated standards: ensuring optimum delivery of the cascade of
care for patients with tuberculosis. Geneva: World Health
Organization; 2017.
Falzon D et al., World Health Organization treatment guidelines for
drug-resistant tuberculosis, 2016 update. Eur Respir J. 2017; 49:
1602308
Caminero JA et al., Proposal for a standardised treatment regimen
to manage pre- and extensively drug-resistant tuberculosis cases. Eur
Respir J. 2017;50:1700648
備考
3)独国
ガイドライン名
英国と同じ(NICE ガイドライン以外)
効能・効果
(または効能・効
果に関連のある記
載箇所)
用法・用量
(または用法・用
量に関連のある記
8