資料5-1 Ⅳ-203 モキシフロキサシン塩酸塩[15.1MB] (86 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00044.html |
| 出典情報 | 医療上の必要性の高い未承認薬・適応外薬検討会議(第66回 12/12)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
resistant and rifampin-resistant
tuberculosis; Pa, pretomanid; Pto, prothionamide; R, rifampin; WHO, World Health Organization; XDR-TB,
extensively drug-resistant tuberculosis; Z, pyrazinamide.
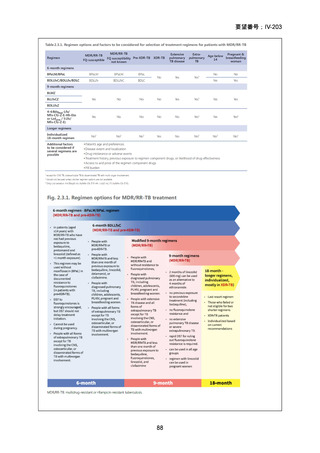
Six-month, All-Oral, Bedaquiline, Pretomanid, Linezolid, and Moxifloxacin
(BPaLM) Regimen
最近の臨床試験 3 件(Nix-TB、Ze-Nix、TB-PRACTECAL)の新たな
エビデンスに基づき、2022 年に WHO は、MDR/RR-TB に対して従
来の推奨療法よりも、BDQ、新規ニトロイミダゾール化合物プレト
マニド、LZD 600 mg/日及び MFLX(BPaLM)の 4 剤で構成されるレ
ジメンを優先すべきであると勧告した。
このレジメンによる治療成功率はおよそ 90%であり、LZD の用量が
600mg/日と、先行した Nix-TB 試験の 1200mg/日より低く、有害事象
の発現も減少している。治療レジメンに MFLX を含めるか、他の 3
剤のみとするかを判断すべきために、FQ に対する DST は治療開始
時に実施すべきである。本レジメンは以下の患者に推奨される。
(1) MDR/RR-TB又は超多剤耐性TBの前段階(pre-XDR-TB)で
14歳以上の患者、HIV合併状況によらない
(2) 粟粒結核、中枢神経結核及び骨関節結核を除くすべての疾
患
(3) BDQ、プレトマニド及びLZDの治療歴がない、若しくは1ヵ
月以上の曝露歴がない患者(感受性が確認できる限り、治
療歴の可能性があっても許容する)
なお、妊娠中又は授乳中の女性においては、プレトマニドの安全性
に関するエビデンスは不完全であるため、投与すべきでない。
Six-Month regimen, all-oral (BDLLfxCfz)
(LVFX に関する記載のみのため、本文書では省略する)
9-Month, All-Oral MDR-TB Regimens
上記の 6 ヵ月レジメンが第一・第二選択肢となるべきであるが、FQ 耐性
がなく、BDQ、DLM 及び LZD の曝露歴がない(又は曝露期間が 1 ヵ月未
満の)MDR/RR-TB 患者では、BDQ を含む 9 ヵ月全経口レジメンの、より
長期の 18 ヵ月レジメンに対する非劣性が示されている。9 ヵ月レジメンの
構成に関する優先順位は以下のとおりである。
(1) BDQ、LZD、MFLX及びPZA(BLMZ)
(2) BDQ、LZD、LVFX、CFZ及びPZA(BLLfxCfzZ)
(3) BDQ、DLM、LZD、LVFX及びPZA(BDLLfxZ)
また、超耐性肺結核又は重篤な肺外結核のいずれでもなく、second-line 薬
剤(BDQ、FQ、TH、LZD 及び CFZ)の曝露歴がない又は 1 ヵ月未満の患
82