よむ、つかう、まなぶ。
【資料1-2】令和8年度研究事業実施方針(AMED研究)(案)の概要 (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59644.html |
| 出典情報 | 厚生科学審議会 科学技術部会(第145回 7/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
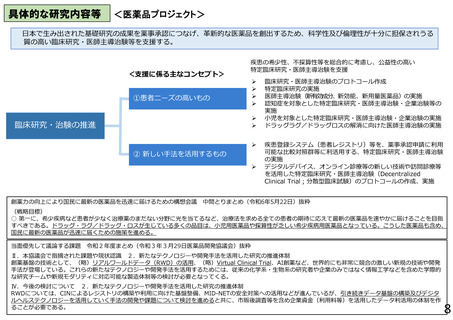
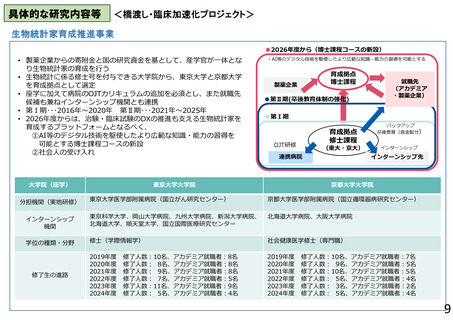
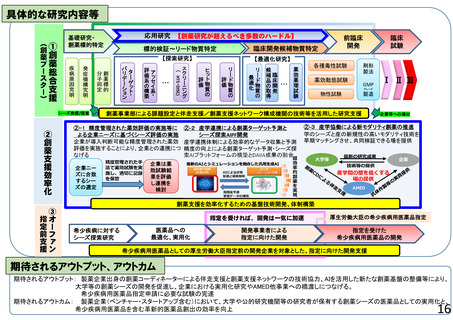
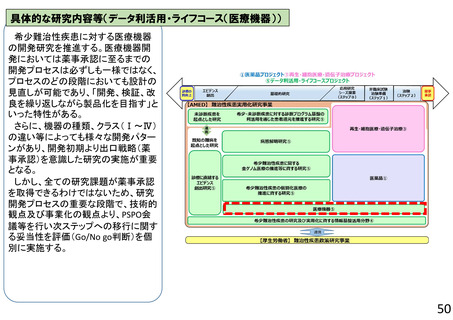
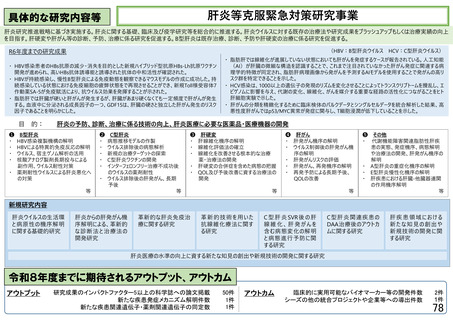
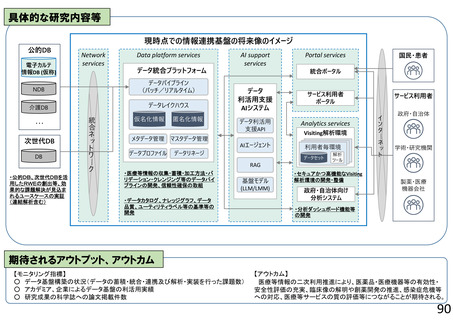
具体的な研究内容等
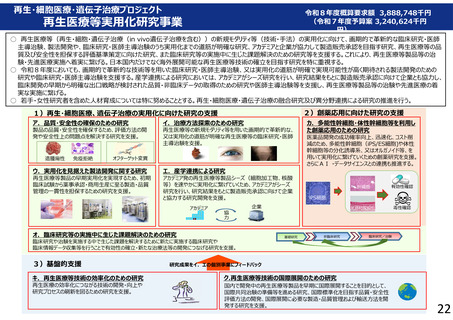
プロジェクト③(再生・細胞医療・遺伝子治療)
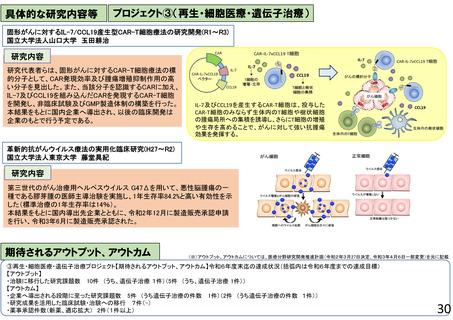
固形がんに対するIL-7/CCL19産生型CAR-T細胞療法の研究開発(R1~R3)
国立大学法人山口大学 玉田耕治
研究内容
研究代表者らは、固形がんに対するCAR-T細胞療法の標
的分子として、CAR発現効率及び腫瘍増殖抑制作用の高
い分子を見出した。また、当該分子を認識するCARに加え、
IL-7及びCCL19を組み込んだCARを発現するCAR-T細胞
を開発し、非臨床試験及びGMP製造体制の構築を行った。
本結果をもとに国内企業へ導出され、以後の臨床開発は
企業のもとで行う予定である。
IL-7及びCCL19を産生するCAR-T細胞は、投与した
CAR-T細胞のみならず生体内のT細胞や樹状細胞
の腫瘍局所への集積を誘導し、さらにT細胞の増殖
や生存を高めることで、がんに対して強い抗腫瘍
効果を発揮する。
革新的抗がんウイルス療法の実用化臨床研究(H27~R2)
国立大学法人東京大学 藤堂具紀
研究内容
第三世代のがん治療用ヘルペスウイルス G47Δを用いて、悪性脳腫瘍の一
種である膠芽腫の医師主導治験を実施し、1年生存率84.2%と高い有効性を示
した(標準治療の1年生存率は14%)。
本結果をもとに国内導出先企業とともに、令和2年12月に製造販売承認申請
を行い、令和3年6月に製造販売承認された。
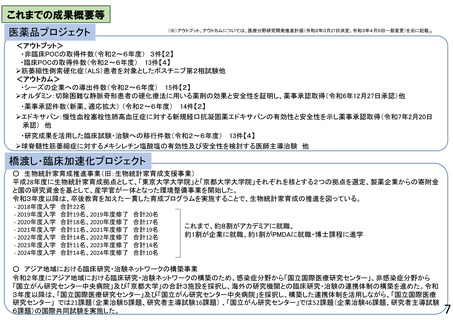
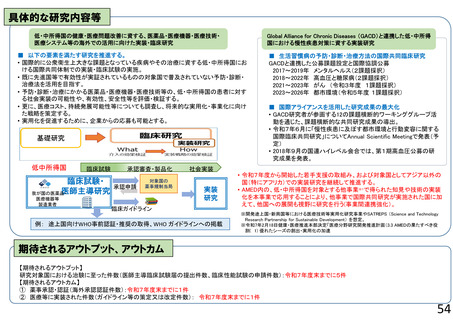
期待されるアウトプット、アウトカム
(※)アウトプット、アウトカムについては、医療分野研究開発推進計画(令和2年3月27日決定、令和3年4月6日一部変更)を元に記載
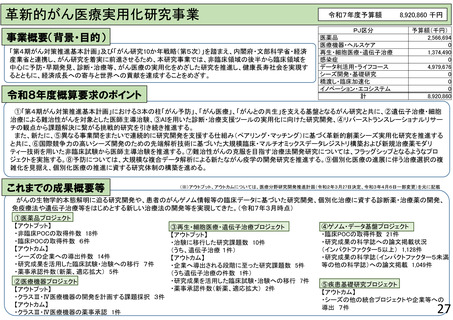
③再生・細胞医療・遺伝子治療プロジェクト【期待されるアウトプット、アウトカム】令和6年度末迄の達成状況(括弧内は令和6年度までの達成目標)
【アウトプット】
・治験に移行した研究課題数 10件 (うち、遺伝子治療 1件)(5件 (うち、遺伝子治療 1件))
【アウトカム】
・企業へ導出される段階に至った研究課題数 5件 (うち遺伝子治療の件数 1件)(2件 (うち遺伝子治療の件数 1件))
・研究成果を活用した臨床試験・治験への移行 7件(-)
・薬事承認件数(新薬、適応拡大) 2件(1件以上)
30
プロジェクト③(再生・細胞医療・遺伝子治療)
固形がんに対するIL-7/CCL19産生型CAR-T細胞療法の研究開発(R1~R3)
国立大学法人山口大学 玉田耕治
研究内容
研究代表者らは、固形がんに対するCAR-T細胞療法の標
的分子として、CAR発現効率及び腫瘍増殖抑制作用の高
い分子を見出した。また、当該分子を認識するCARに加え、
IL-7及びCCL19を組み込んだCARを発現するCAR-T細胞
を開発し、非臨床試験及びGMP製造体制の構築を行った。
本結果をもとに国内企業へ導出され、以後の臨床開発は
企業のもとで行う予定である。
IL-7及びCCL19を産生するCAR-T細胞は、投与した
CAR-T細胞のみならず生体内のT細胞や樹状細胞
の腫瘍局所への集積を誘導し、さらにT細胞の増殖
や生存を高めることで、がんに対して強い抗腫瘍
効果を発揮する。
革新的抗がんウイルス療法の実用化臨床研究(H27~R2)
国立大学法人東京大学 藤堂具紀
研究内容
第三世代のがん治療用ヘルペスウイルス G47Δを用いて、悪性脳腫瘍の一
種である膠芽腫の医師主導治験を実施し、1年生存率84.2%と高い有効性を示
した(標準治療の1年生存率は14%)。
本結果をもとに国内導出先企業とともに、令和2年12月に製造販売承認申請
を行い、令和3年6月に製造販売承認された。
期待されるアウトプット、アウトカム
(※)アウトプット、アウトカムについては、医療分野研究開発推進計画(令和2年3月27日決定、令和3年4月6日一部変更)を元に記載
③再生・細胞医療・遺伝子治療プロジェクト【期待されるアウトプット、アウトカム】令和6年度末迄の達成状況(括弧内は令和6年度までの達成目標)
【アウトプット】
・治験に移行した研究課題数 10件 (うち、遺伝子治療 1件)(5件 (うち、遺伝子治療 1件))
【アウトカム】
・企業へ導出される段階に至った研究課題数 5件 (うち遺伝子治療の件数 1件)(2件 (うち遺伝子治療の件数 1件))
・研究成果を活用した臨床試験・治験への移行 7件(-)
・薬事承認件数(新薬、適応拡大) 2件(1件以上)
30