よむ、つかう、まなぶ。
【資料1-2】令和8年度研究事業実施方針(AMED研究)(案)の概要 (22 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59644.html |
| 出典情報 | 厚生科学審議会 科学技術部会(第145回 7/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
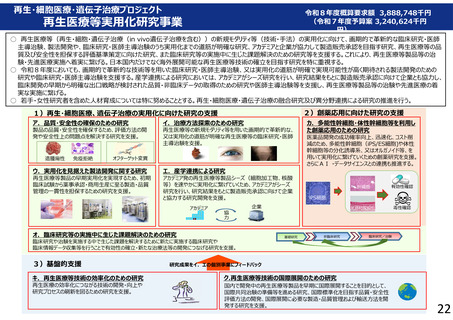
再生医療等実用化研究事業
令和7年度予算額
事業概要(背景・目的)
再生医療等は、これまでの治療では対応困難であった疾患に対す
る新たな治療法となり得るものであり、最新の再生医療を世界に先
駆けて実用化することを目的として、倫理性及び科学性が十分に担
保された臨床研究や医師主導治験等を支援する必要がある。
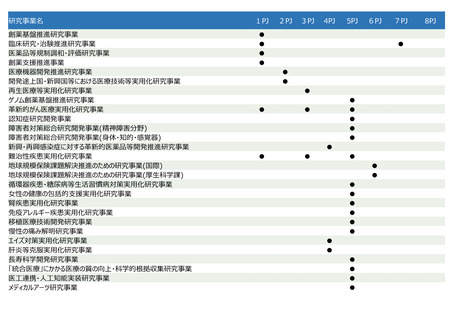
PJ区分
医薬品
医療機器・ヘルスケア
再生・細胞医療・遺伝子治療
感染症
データ利活用・ライフコース
シーズ開発・基礎研究
橋渡し・臨床加速化
イノベーション・エコシステム
計
3,240,624千円
予算額(千円)
0
0
3,240,624
0
0
0
0
0
3,240,624
令和8年度概算要求のポイント
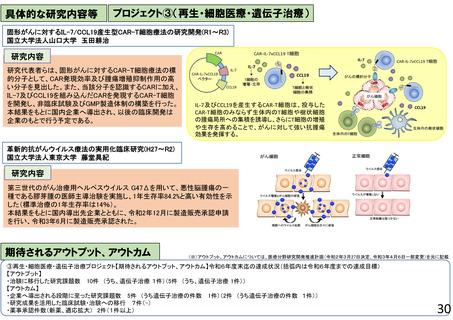
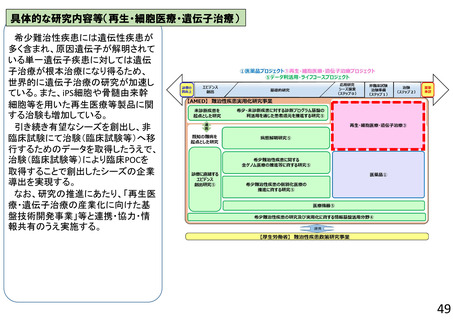
○ 再生医療等(再生・細胞・遺伝子治療(in vivo遺伝子治療を含む))の新規モダリティ等(技術・手法)の実用化に向けて、画期的で革新的な臨床研究・医
師主導治験、製法開発や、臨床研究・医師主導治験のうち実用化までの道筋が明確な研究、アカデミアと企業が協力して製造販売承認を目指す研究、再生医療等
の品質及び安全性を担保する評価基準策定に向けた研究、また臨床研究等の実施中に生じた課題解決のための研究等を支援する。これにより、再生医療等製品等
の治験・先進医療実施へ着実に繋げる。日本国内だけでなく海外展開可能な再生医療等技術の確立を目指す研究を特に重視する。
○ 令和7年度においても、画期的で革新的な技術等を用いた臨床研究・医師主導治験、又は実用化の道筋が明確で実現可能性が高く期待される製法開発のための
研究や臨床研究・医師主導治験を支援する。産学連携による研究においては、アカデミアがシーズ研究を行い、研究結果をもとに製造販売承認に向けて企業とも協力
し、臨床開発の早期から明確な出口戦略が検討された品質・非臨床データの取得のための研究や医師主導治験等を支援し、再生医療等製品等の治験や先進医療
の着実な実施に繋げる。
○ 若手・女性研究者を含めた人材育成については特に努めることとする。再生・細胞医療・遺伝子治療の融合研究及び異分野連携による研究の推進を行う。
これまでの成果概要等
。
(※)アウトプット、アウトカムについては、医療分野研究開発推進計画(令和2年3月27日決定、令和3年4月6日一部変更)を元に記載
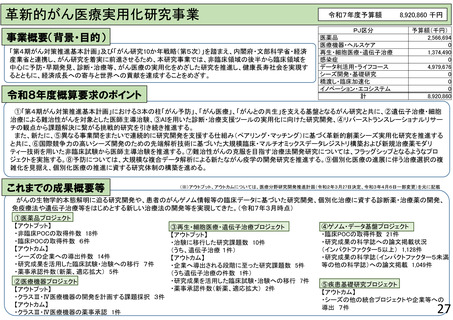
令和2年度から令和6年度までの研究において、パーキンソン病に対するiPS細胞由来分化細胞を用いた医師主導治験など、97件の臨床研究や
医師主導治験が実施された。引き続き、臨床研究又は治験に移行する研究課題を支援することで再生医療等の実用化を推進する。
【再生・細胞医療・遺伝子治療(令和2年度から令和6年度まで)】
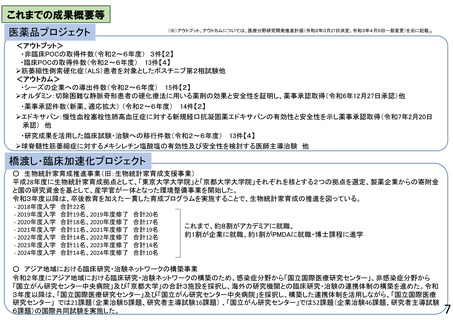
<アウトプット>
・研究成果の科学誌(インパクトファクター5以上)への論文掲載件数 128件
・研究成果の科学誌(インパクトファクター5未満等の他の科学誌)への論文掲載状況 153件
・治験に移行した研究課題数 17件
・臨床研究に移行した研究課題数 13件
<アウトカム>
・企業へ導出される段階に至った研究課題数 1件
・研究成果を活用した臨床試験・治験への移行状況 26件
・薬事承認件数 3件
21
令和7年度予算額
事業概要(背景・目的)
再生医療等は、これまでの治療では対応困難であった疾患に対す
る新たな治療法となり得るものであり、最新の再生医療を世界に先
駆けて実用化することを目的として、倫理性及び科学性が十分に担
保された臨床研究や医師主導治験等を支援する必要がある。
PJ区分
医薬品
医療機器・ヘルスケア
再生・細胞医療・遺伝子治療
感染症
データ利活用・ライフコース
シーズ開発・基礎研究
橋渡し・臨床加速化
イノベーション・エコシステム
計
3,240,624千円
予算額(千円)
0
0
3,240,624
0
0
0
0
0
3,240,624
令和8年度概算要求のポイント
○ 再生医療等(再生・細胞・遺伝子治療(in vivo遺伝子治療を含む))の新規モダリティ等(技術・手法)の実用化に向けて、画期的で革新的な臨床研究・医
師主導治験、製法開発や、臨床研究・医師主導治験のうち実用化までの道筋が明確な研究、アカデミアと企業が協力して製造販売承認を目指す研究、再生医療等
の品質及び安全性を担保する評価基準策定に向けた研究、また臨床研究等の実施中に生じた課題解決のための研究等を支援する。これにより、再生医療等製品等
の治験・先進医療実施へ着実に繋げる。日本国内だけでなく海外展開可能な再生医療等技術の確立を目指す研究を特に重視する。
○ 令和7年度においても、画期的で革新的な技術等を用いた臨床研究・医師主導治験、又は実用化の道筋が明確で実現可能性が高く期待される製法開発のための
研究や臨床研究・医師主導治験を支援する。産学連携による研究においては、アカデミアがシーズ研究を行い、研究結果をもとに製造販売承認に向けて企業とも協力
し、臨床開発の早期から明確な出口戦略が検討された品質・非臨床データの取得のための研究や医師主導治験等を支援し、再生医療等製品等の治験や先進医療
の着実な実施に繋げる。
○ 若手・女性研究者を含めた人材育成については特に努めることとする。再生・細胞医療・遺伝子治療の融合研究及び異分野連携による研究の推進を行う。
これまでの成果概要等
。
(※)アウトプット、アウトカムについては、医療分野研究開発推進計画(令和2年3月27日決定、令和3年4月6日一部変更)を元に記載
令和2年度から令和6年度までの研究において、パーキンソン病に対するiPS細胞由来分化細胞を用いた医師主導治験など、97件の臨床研究や
医師主導治験が実施された。引き続き、臨床研究又は治験に移行する研究課題を支援することで再生医療等の実用化を推進する。
【再生・細胞医療・遺伝子治療(令和2年度から令和6年度まで)】
<アウトプット>
・研究成果の科学誌(インパクトファクター5以上)への論文掲載件数 128件
・研究成果の科学誌(インパクトファクター5未満等の他の科学誌)への論文掲載状況 153件
・治験に移行した研究課題数 17件
・臨床研究に移行した研究課題数 13件
<アウトカム>
・企業へ導出される段階に至った研究課題数 1件
・研究成果を活用した臨床試験・治験への移行状況 26件
・薬事承認件数 3件
21