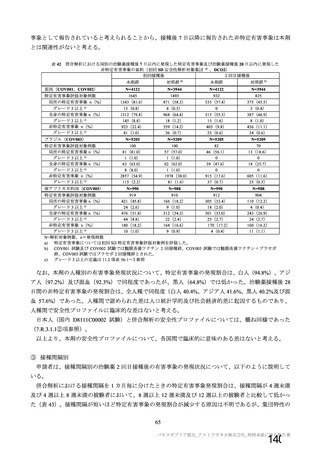
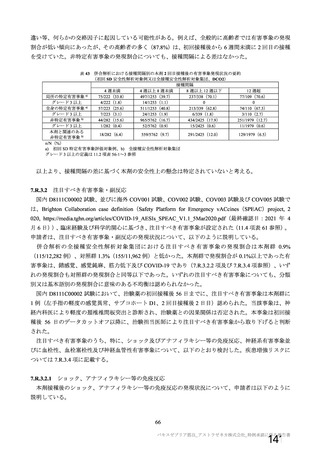
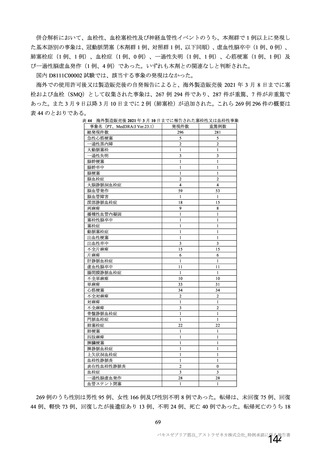
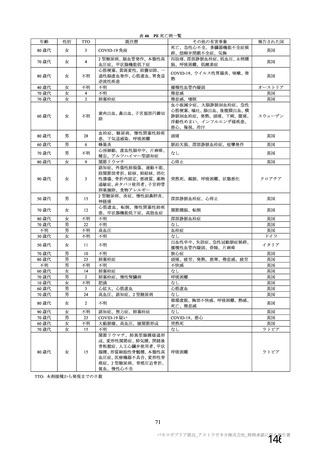
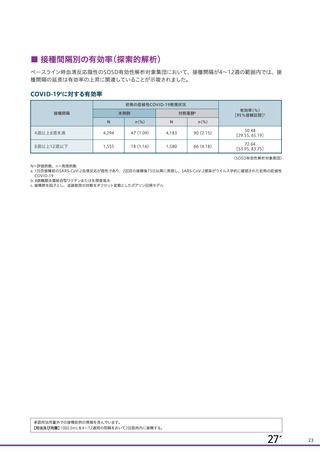
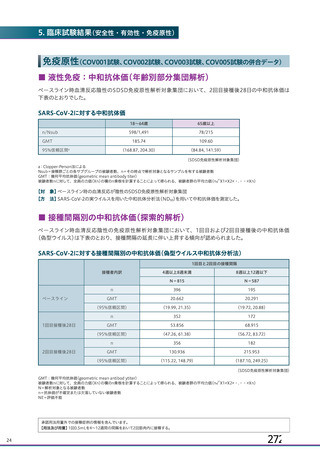
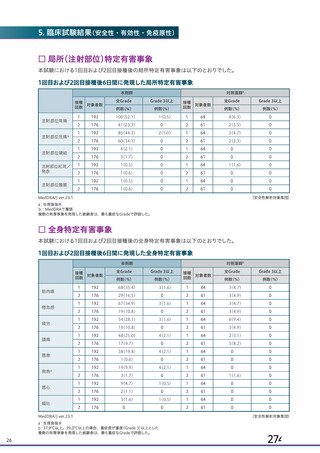
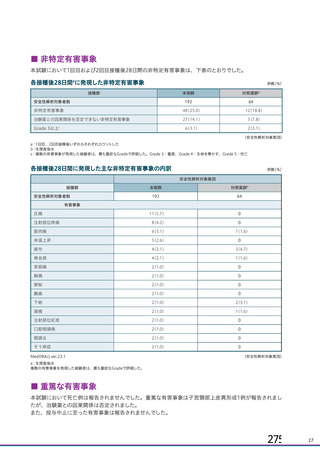
資 料4-1 令和3年度第6回安全技術調査会の審議結果について (94 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
ウスにおける反復筋肉内投与毒性試験(CTD 4.2.3.2.1)の初回投与後の結果から評価された。本剤投与
による死亡はなく、本剤投与部位における浮腫、体温上昇(+0.47℃)等が認められている。
反復投与毒性試験
5.2
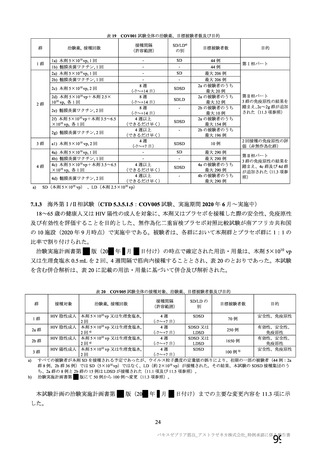
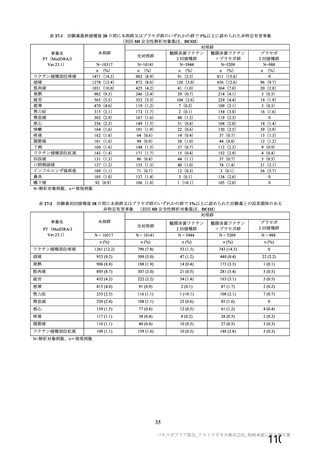
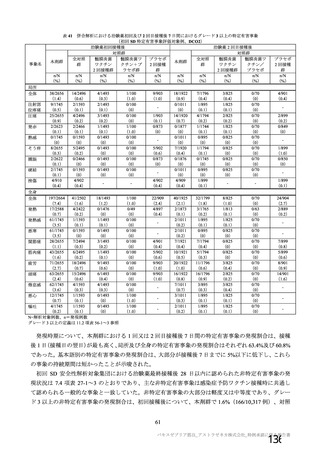
本剤を用いて、マウスにおける反復筋肉内投与毒性試験が実施された(表 13)。主な所見は、投与部
位における炎症性変化であった。
試験系
投与
経路
投与期間
表 13 反復投与毒性試験
用量
(μL/body)
主な所見
無毒性量
(μL/body)
添付資料
CTD
6 週間
70 d):体温上昇、投与部位の浮腫・炎症 e)
(1 回/3 週:計 3 回 a))
70
4.2.3.2.1
0 b)、70 c)
筋肉内
+
回復性:あり
休薬 28 日間
試験開始後 1、22 及び 43 日に、35 μL/site で左右の大腿四頭筋に投与
10 mM ヒスチジン、7.5% [v/w] スクロース、35 mM 塩化ナトリウム、1 mM 塩化マグネシウム、0.1% ポリソルベート 80、0.1 mM
EDTA 及び 0.5% [v/w] エタノール含有水溶液(pH 6.6)
本剤(3.7×1010 vp /70 μL)
試験開始後 22、43 及び 74 日に S タンパク質に対する抗体産生が確認されている
投与部近傍の坐骨神経周辺に炎症が認められたが、公表文献(Toxicol Pathol. 2020; 48: 257-76)等を踏まえ、投与部位の炎症が伸展し
た所見であり、投与手技に起因したげっ歯類に特有と判断されている
雌雄マウス
(CD-1)
a)
b)
c)
d)
e)
遺伝毒性試験
5.3
本剤に用いられる ChAdOx1 ベクターは染色体への組込み能を持たないことから、本剤を用いた遺伝
毒性試験は実施されていない。
がん原性試験
5.4
本剤は臨床での使用が 6 カ月以上継続される医薬品ではないことから、本剤を用いたがん原性試験は
実施されていない。
生殖発生毒性試験
5.5
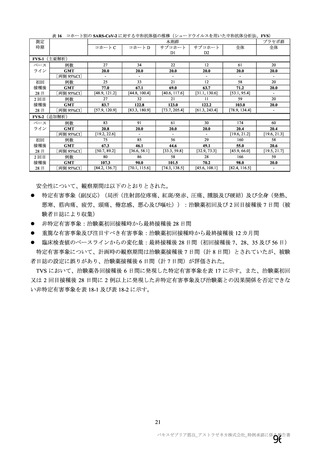
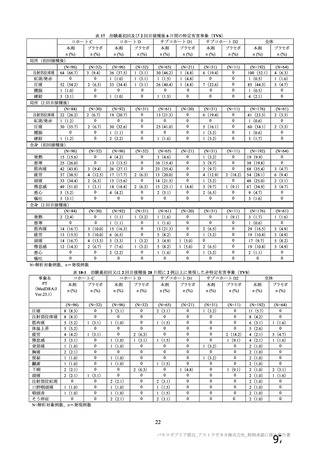
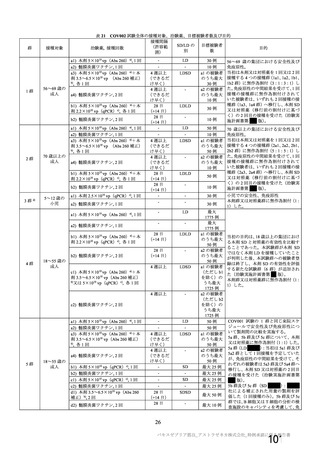
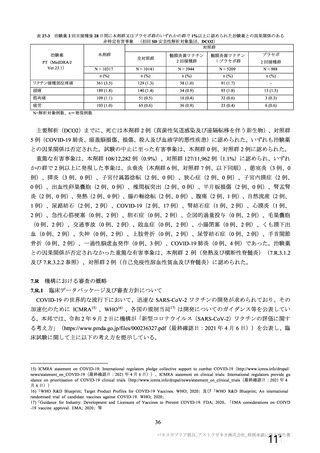
マウスにおける生殖発生毒性試験が実施された(表 14)。本剤投与により、親動物及び次世代への影
響は認められなかった。
表 14
試験の種類
受胎能及び着床ま
での初期胚発生、
胚・胎児発生、出
生前及び出生後の
発生並びに母体の
機能試験
a)
b)
c)
d)
5.6
試験系
投与
経路
投与期間
生殖発生毒性試験
用量
(μL/body)
主な所見
母動物
70 d):なし
雌
マウス
(CD-1)
筋肉内
雌:交配前 13
日~妊娠 15 日
(3 回 a))
0 b)、70 c)
胚・胎児
70 d):なし
F1 出生児
70 d):なし
無毒性量
(μL/body)
添付資料
CTD
母動物(一般毒
性、生殖能):70
胚・胎児:70
4.2.3.5.2.2
F1 出生児:70
交配前 13 日、妊娠 6 及び 15 日に、35 μL/site で左右の大腿四頭筋に投与
10 mM ヒスチジン、7.5% [v/w] スクロース、35 mM 塩化ナトリウム、1 mM 塩化マグネシウム、0.1% ポリソルベート 80、
0.1 mM EDTA 及び 0.5% [v/w] エタノール含有水溶液(pH 6.6)
本剤(3.71×1010 vp /70 μL)
試験開始後 14 日、交配後 7、15 及び 17.5 日(帝王切開時)及び分娩後 7 及び 21 日における母動物、妊娠 17.5 日(帝王切
開時)の胎児、及び分娩後 21 日の F1 出生児において S タンパク質に対する抗体産生が確認されている
局所刺激性試験
17
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
92