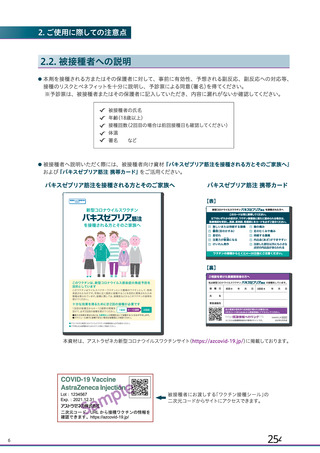
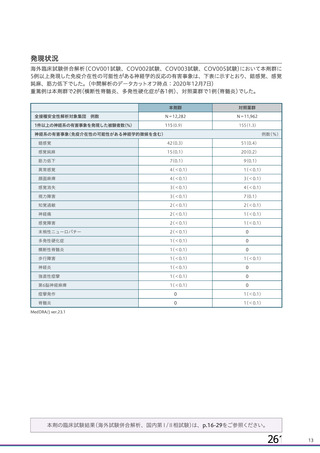
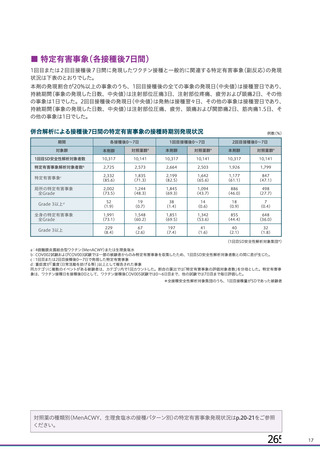
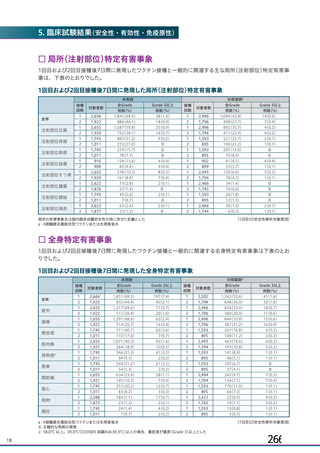
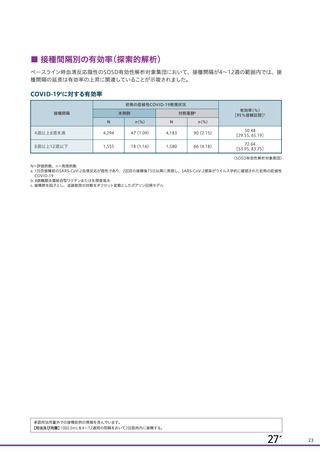
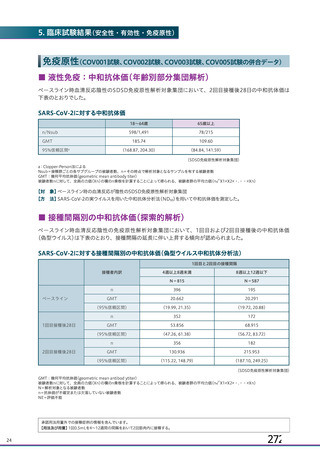
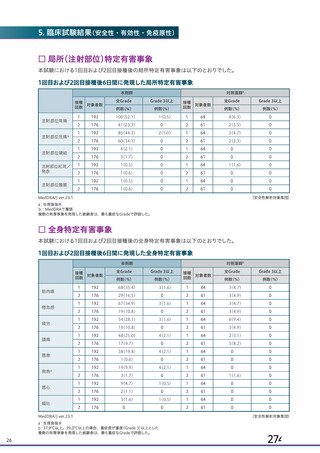
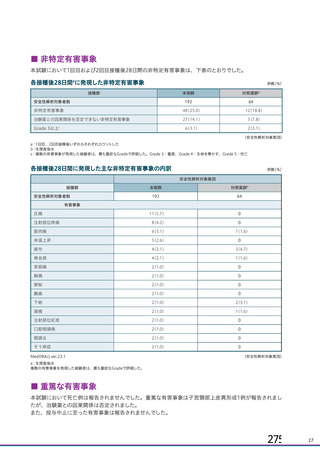
資 料4-1 令和3年度第6回安全技術調査会の審議結果について (141 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
至った重篤な有害事象は治験薬接種との因果関係なしと判断された。
国内 D8111C00002 試験では、治験薬の初回接種後 56 日までに、死亡は報告されなかった。重篤な有
害事象はプラセボ群に 1 例(サブコホート D1、初回接種後、重度の子宮頚部上皮異形成)認められ、治
験薬との因果関係は否定された。
7.R.3.1.3
①
部分集団別の有害事象の発現状況
年齢別
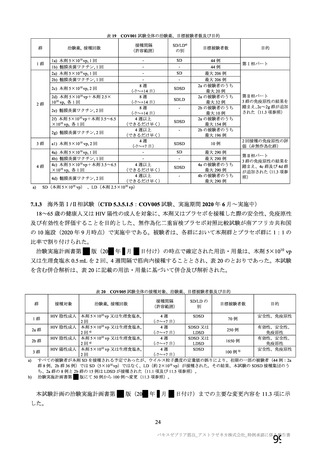
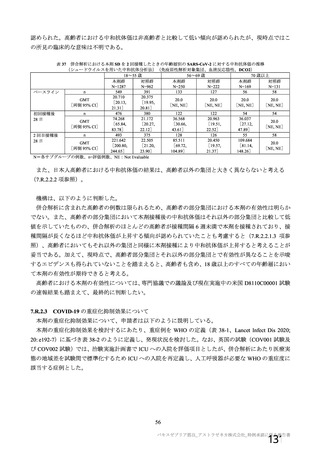
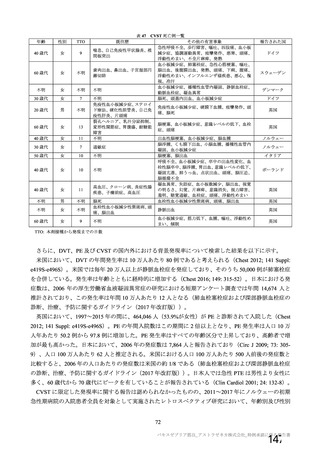
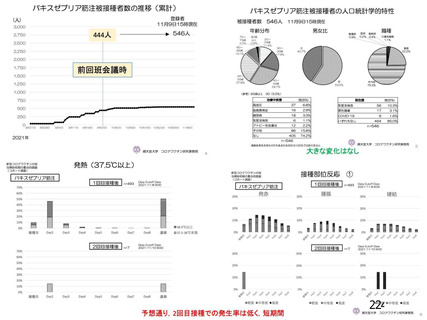
年齢別の本剤の安全性について、申請者は以下のように説明している。
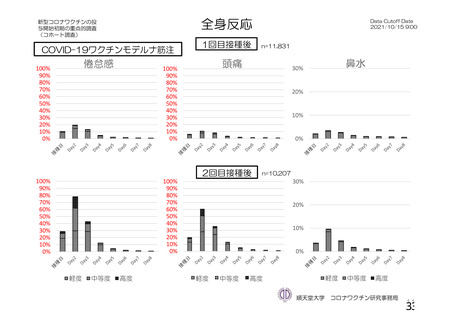
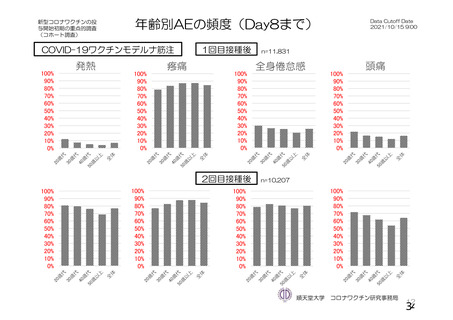
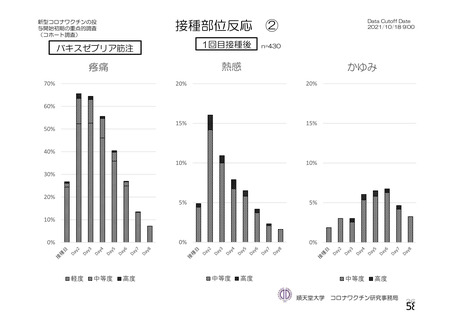
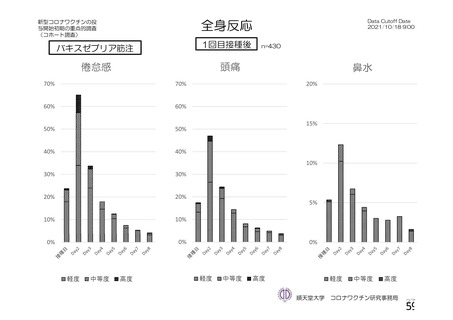
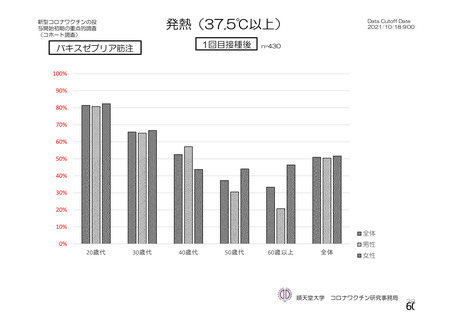
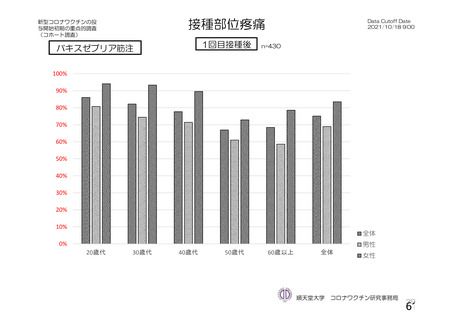
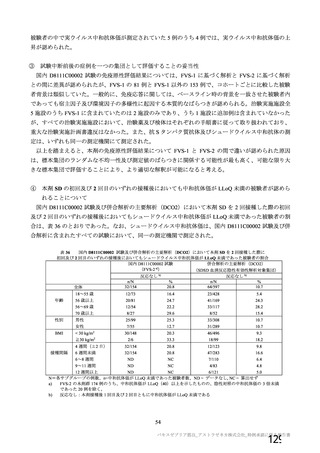
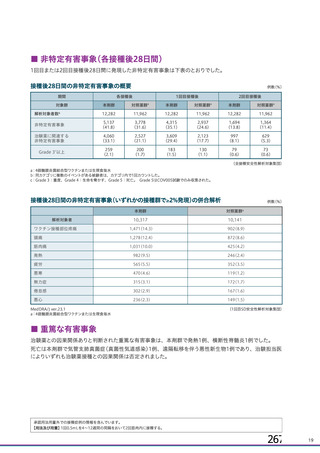
併合解析の初回 SD 特定有害事象評価対象例において、局所及び全身の特定有害事象の重症度及び発
現割合は、18~64 歳と比較して 65 歳以上で低く、いずれの年齢の部分集団でも特定有害事象の重症度
及び発現割合は、初回接種後と比較して 2 回目接種後で低かった。また、初回 SD 安全性解析対象集団
において、接種回数を問わない本剤接種後 28 日間の非特定有害事象の発現割合も 18~64 歳(46.7%)と
比較して 65 歳以上(29.7%)で低かった。非特定有害事象の大部分は軽度又は中等度であり、グレード
3 以上の非特定有害事象の発現割合は 65 歳以上(1.7%)と 18~64 歳(2.3%)のいずれでも低かった。
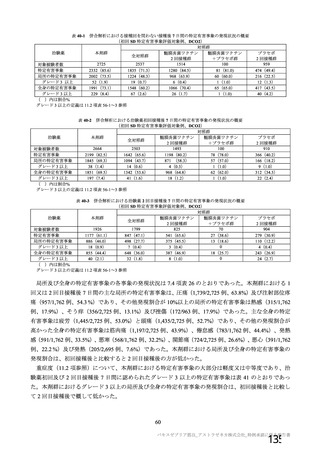
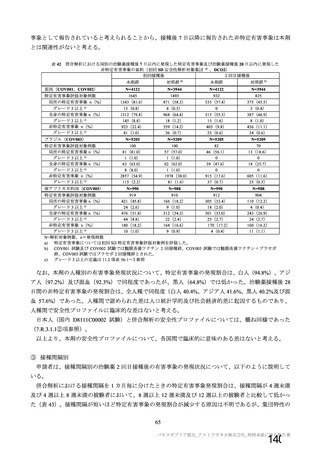
併合解析の全接種安全性解析対象集団における重篤な有害事象の発現割合は、18~64 歳では本剤群
0.8%(90 例)及び対照群 1.0%(114 例)であり、65 歳以上では本剤群 1.4%(18 例)及び対照群 1.3%
(13 例)であった。
以上のように、本剤の安全性プロファイルは、65 歳以上と 18~64 歳で類似していた。また、日本人
についても高齢の被験者では、他の年齢層の被験者と比較して有害事象の重症度及び発現割合が低かっ
た(7.R.3.1.1②項参照)。
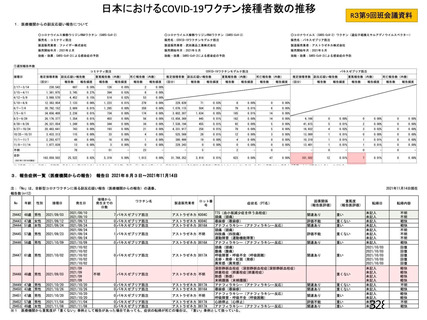
② 国別
国別の安全性プロファイルについて、申請者は以下のように説明している。
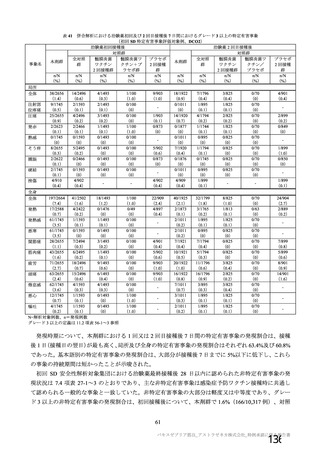
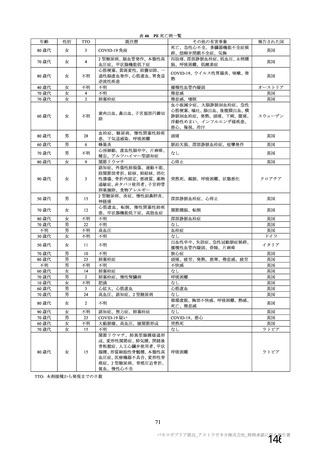
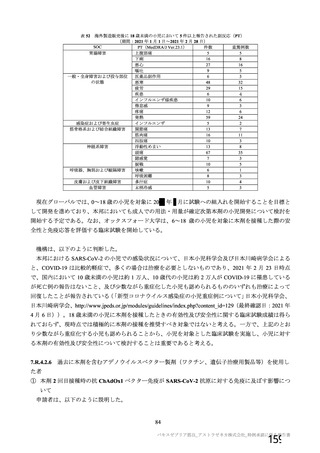
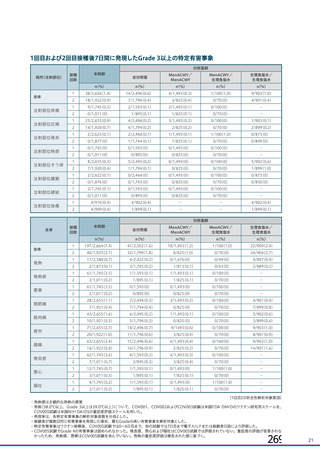
併合解析において、特定有害事象について国別の結果で臨床的に意味のある不均衡は認められなかっ
た(表 42)。非特定有害事象の発現割合は、英国及び南アフリカ共和国と比較してブラジルで高い傾向
が認められた(表 42)。
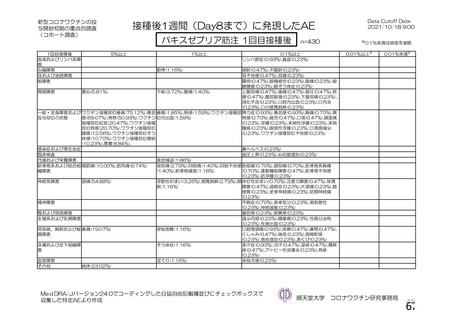
併合解析に含めた 4 試験では、一部の被験者のみが日誌を用いて各接種後 1 週間の特定有害事象を記
録したが、英国(COV001 及び COV002 試験)、ブラジル(COV003 試験)及び南アフリカ共和国(COV005
試験)で日誌を配布された被験者の割合は、それぞれ 36%、2%及び 93%であった。ブラジルでは、被験
者の 98%ですべての有害事象が非特定有害事象として収集された結果、本剤群、対照群ともに、非特定
有害事象の発現割合が他の国より高くなったと考えられる。ブラジルで本剤群又は対照群のいずれかで
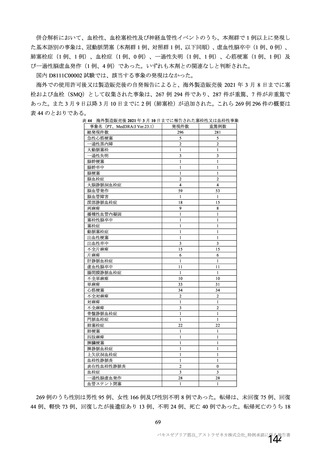
3 %以上に報告された非特定有害事象は本剤群で多い順に、ワクチン接種部位疼痛、頭痛、筋肉痛、発熱、
悪寒、疲労及び無力症であり、南アフリカ共和国及び英国で収集された特定有害事象と一致していた。
南アフリカ共和国では、特定有害事象の発現割合が英国及びブラジルと比較して低かったが、これは、
日誌で収集する特定有害事象の種類と日数が異なったこと等が原因であると考えられた。COV005 試験
では 5 種類の局所事象及び 5 種類の全身性事象を 7 日間収集し、COV001 試験、COV002 試験及び COV003
試験では、7 種類の局所事象及び 10 種類の全身性事象を 8 日間収集した。また、南アフリカ共和国で本
剤群とプラセボ群の非特定有害事象の発現割合が同程度であったが、南アフリカ共和国では被験者の大
部分に日誌が配布されたために、本剤接種から予期される副反応の徴候及び症状はほとんどが特定有害
64
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
139