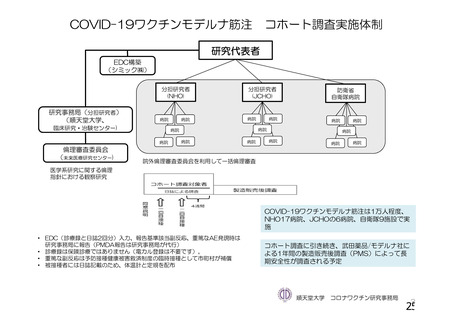
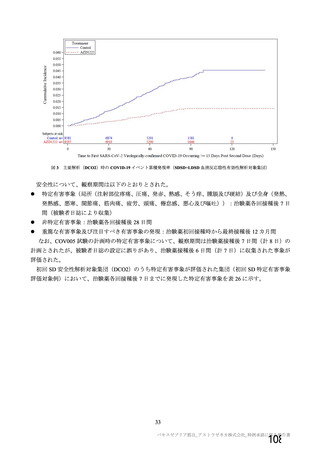
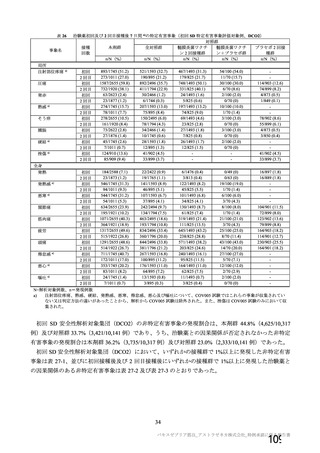
資 料4-1 令和3年度第6回安全技術調査会の審議結果について (101 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
群
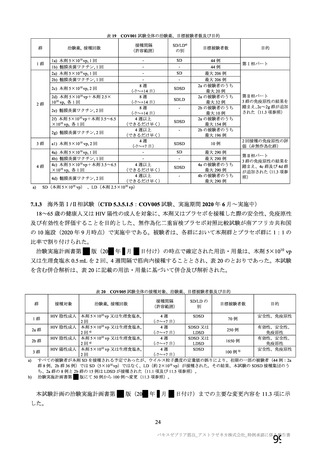
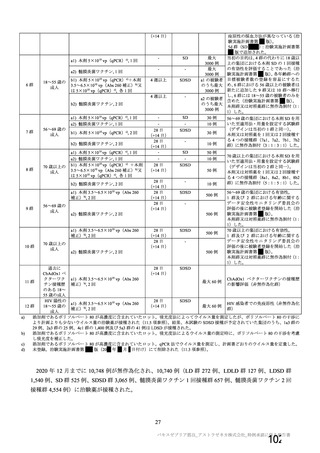
COV001 試験全体の治験薬、目標被験者数及び目的
接種間隔
(許容範囲)
治験薬, 接種回数
SD/LDa)
の別
本剤 5×1010 vp, 1 回
髄膜炎菌ワクチン, 1 回
本剤 5×1010 vp, 1 回
髄膜炎菌ワクチン, 1 回
8週
2c) 本剤 5×1010 vp, 2 回
(-7~+14 日)
8週
2d) 本剤 5×1010 vp+本剤 2.5×
10
vp,
各
1
回
(-7~+14
日)
10
2群
8週
2e) 髄膜炎菌ワクチン, 2 回
(-7~+14 日)
4 週以上
2f) 本剤 5×1010 vp+本剤 3.5~6.5
(できるだけ早く)
×1010 vp, 各 1 回
4 週以上
2g) 髄膜炎菌ワクチン, 2 回
(できるだけ早く)
4週
3群
a1) 本剤 5×1010 vp, 2 回
(-7~+7 日)
4a) 本剤 5×1010 vp, 1 回
4b) 髄膜炎菌ワクチン, 1 回
4 週以上
4c) 本剤 5×1010 vp+本剤 3.5~6.5
4群
(できるだけ早く)
×1010 vp, 各 1 回
4 週以上
4d) 髄膜炎菌ワクチン, 2 回
(できるだけ早く)
a) SD(本剤 5×1010 vp) 、LD(本剤 2.5×1010 vp)
1群
7.1.3
1a)
1b)
2a)
2b)
SD
SD
SDSD
SDLD
SDSD
-
目標被験者数
44 例
44 例
最大 206 例
最大 206 例
2a の被験者のうち
最大 20 例
2a の被験者のうち
最大 32 例
2b の被験者のうち
最大 10 例
2a の被験者のうち
最大 154 例
2b の被験者のうち
最大 196 例
目的
第Ⅰ相パート
第Ⅱ相パート
3 群の免疫原性の結果を
踏まえ、
2c~2g 群が追加
された(11.3 項参照)
SDSD
10 例
2 回接種の免疫原性の評
価(非無作為化群)
SD
-
最大 290 例
最大 290 例
4a の被験者のうち
最大 290 例
4b の被験者のうち
最大 290 例
第Ⅱ相パート
3 群の免疫原性の結果を
踏まえ、4c 群及び 4d 群
が追加された(11.3 項参
照)
SDSD
-
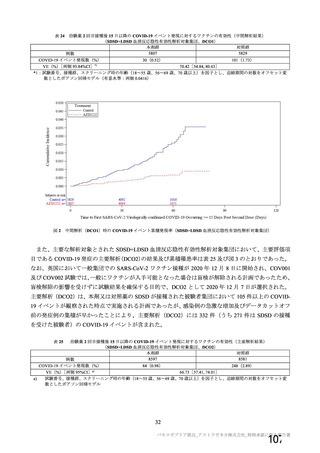
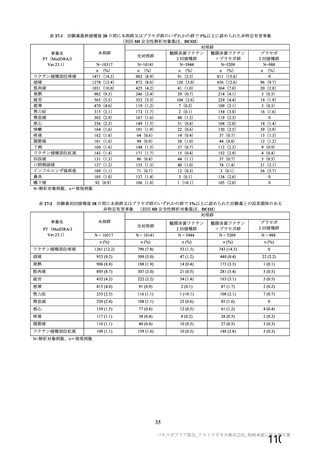
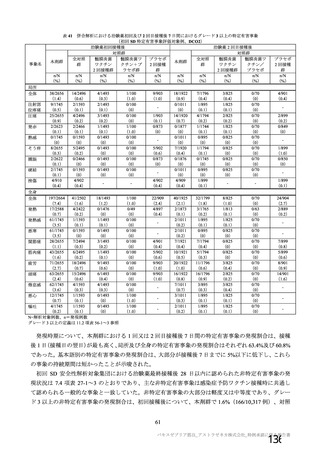
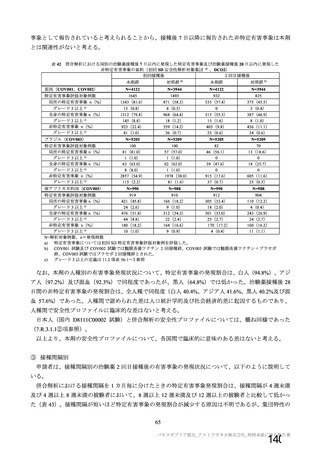
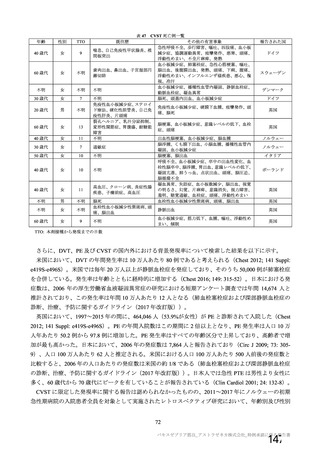
海外第Ⅰ/Ⅱ相試験(CTD 5.3.5.1.5:COV005 試験、実施期間 2020 年 6 月~実施中)
18~65 歳の健康人又は HIV 陽性の成人を対象に、本剤又はプラセボを接種した際の安全性、免疫原性
及び有効性を評価することを目的とした、無作為化二重盲検プラセボ対照比較試験が南アフリカ共和国
の 10 施設(2020 年 9 月時点)で実施中である。被験者は、各群において本剤群とプラセボ群に 1:1 の
比率で割り付けられた。
治験実施計画書第
版(20
年
月
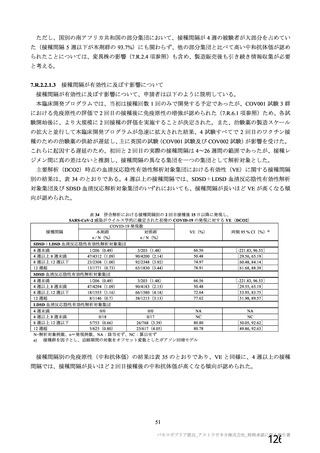
日付け)の時点で確定された用法・用量は、本剤 5×1010 vp
又は生理食塩水 0.5 mL を 2 回、4 週間隔で筋肉内接種することとされ、表 20 のとおりであった。本試験
を含む併合解析は、表 20 に記載の用法・用量に基づいて併合及び解析された。
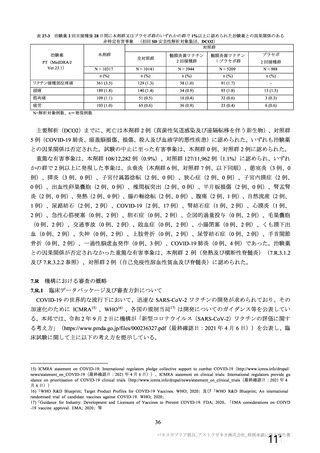
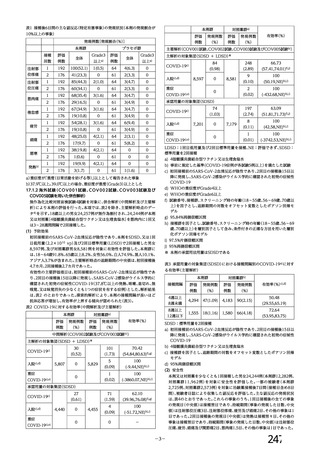
表 20
群
接種対象
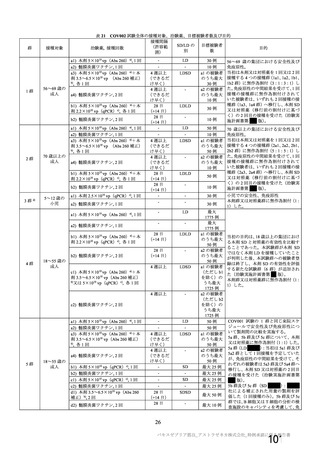
COV005 試験全体の接種対象、治験薬、目標被験者数及び目的
治験薬, 接種回数
接種間隔
(許容範囲)
SD/LD の
別
目標被験者数
目的
本剤 5×1010 vp 又は生理食塩水,
4週
SDSD
安全性、免疫原性
70 例
2回
(-7~+7 日)
4週
SDSD 又は
有効性、安全性、
HIV 陰性成人 本剤 5×1010 vp 又は生理食塩水,
250 例
2a 群
(-7~+7 日)
LDSD
免疫原性
2 回 a)
HIV 陰性成人 本剤 5×1010 vp 又は生理食塩水,
4週
SDSD 又は
有効性、安全性、
2b 群
1650 例
2 回 a)
(-7~+7 日)
LDSD
免疫原性
HIV 陽性成人 本剤 5×1010 vp 又は生理食塩水,
安全性、免疫原性
4週
SDSD
b)
3群
100 例
2回
(-7~+7 日)
a) すべての被験者が本剤 SD を接種される予定であったが、ウイルス粒子濃度の定量値の誤りにより、初期の一部の被験者(44 例:2a
群 8 例、2b 群 36 例)では SD(5×1010 vp)ではなく、LD(約 2×1010 vp)が接種された。その結果、本試験の SDSD 接種集団のう
ち、2a 群の 8 例と 2b 群の 15 例は LDSD が接種された(11.1 項及び 11.5 項参照)。
b) 治験実施計画書第
版にて 50 例から 100 例へ変更(11.3 項参照)。
1群
HIV 陰性成人
本試験計画の治験実施計画書第
版(20
年
月
日付け)までの主要な変更内容を 11.3 項に示
した。
24
バキスゼブリア筋注_アストラゼネカ株式会社_特例承認に係る報告書
99