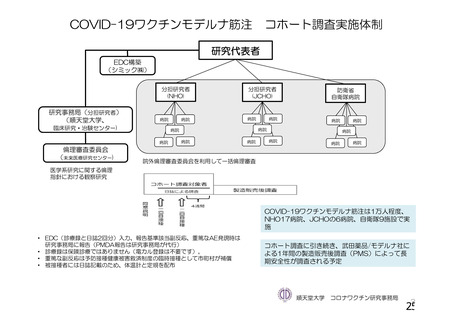
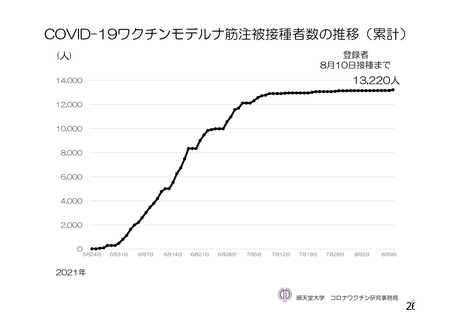
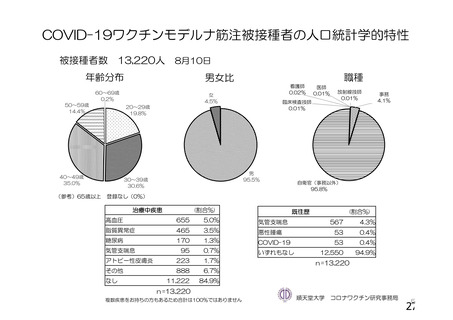
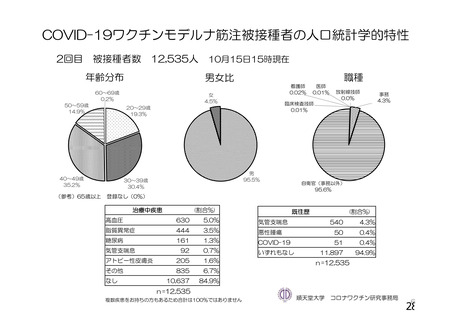
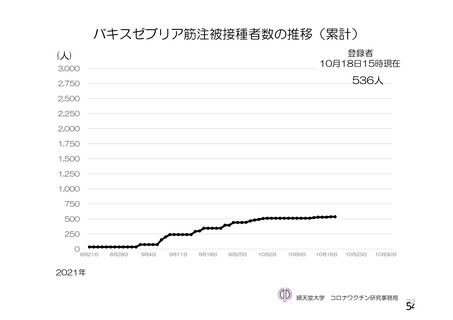
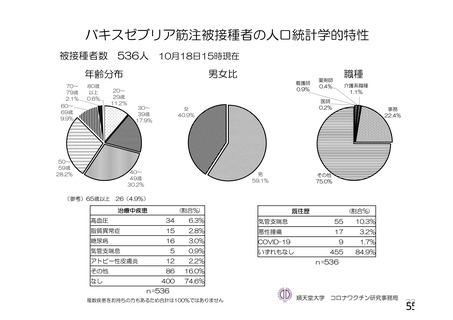
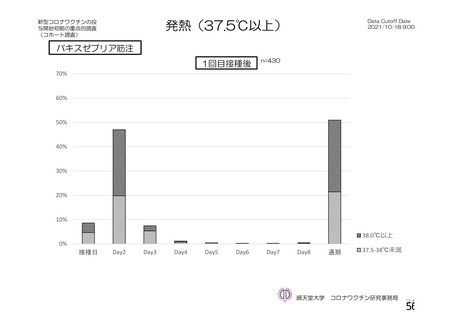
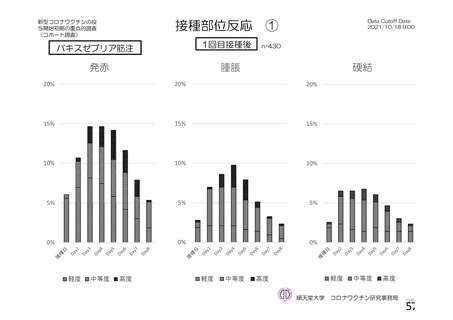
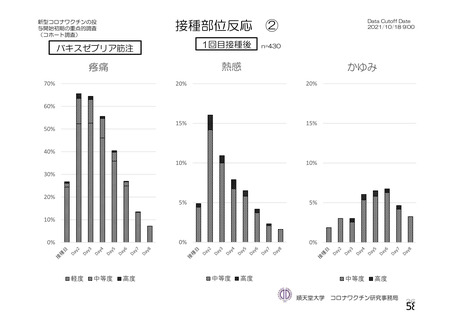
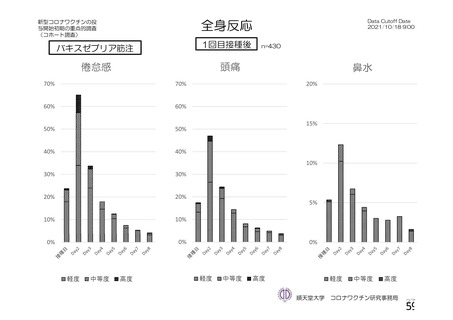
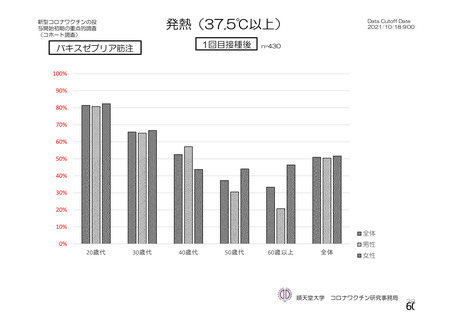
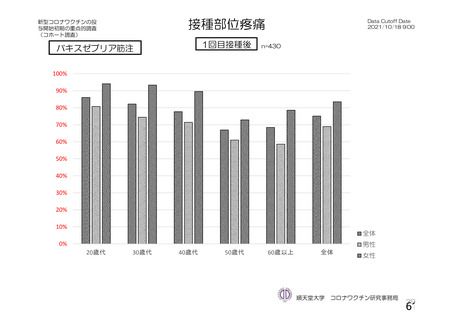
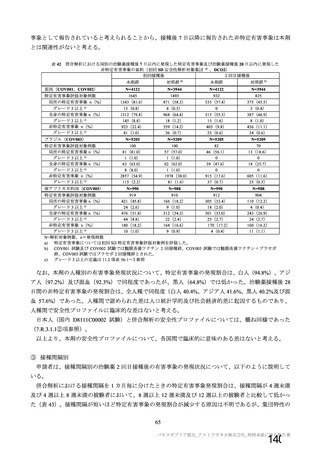
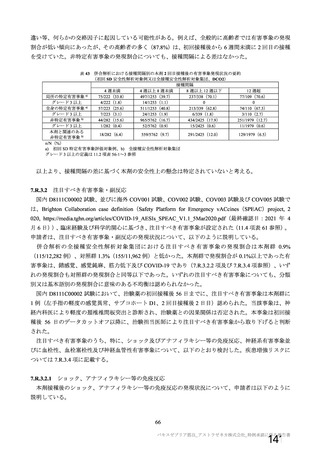
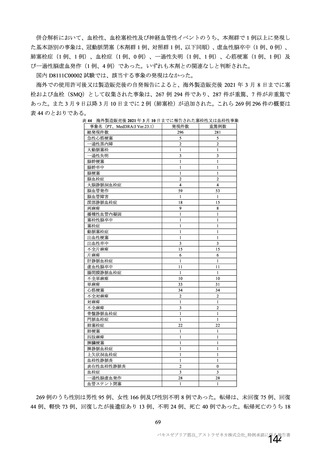
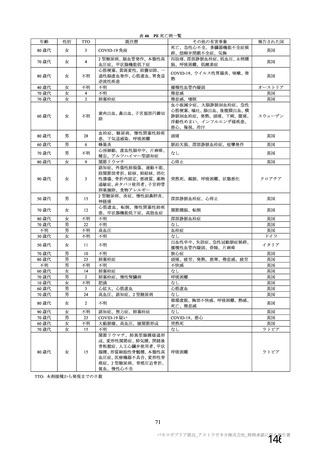
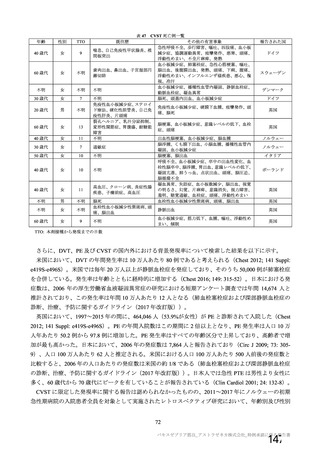
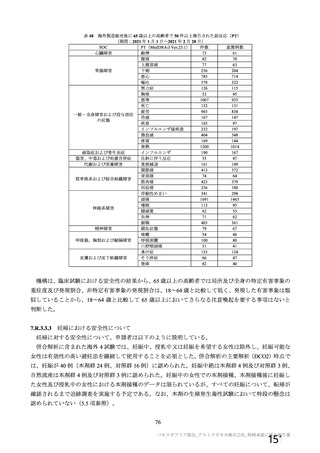
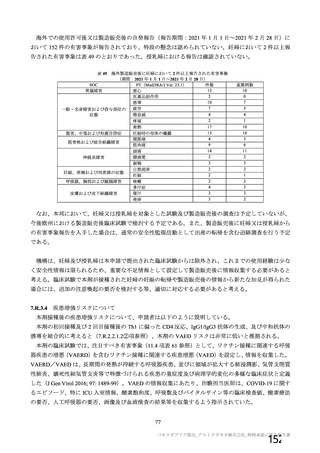
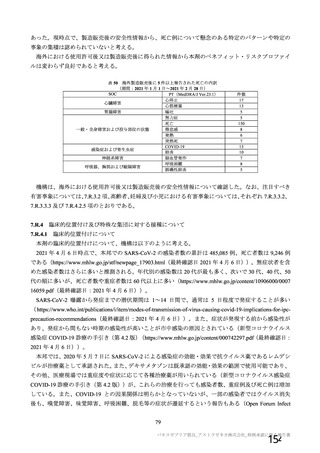
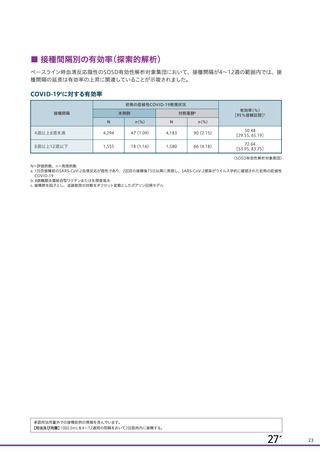
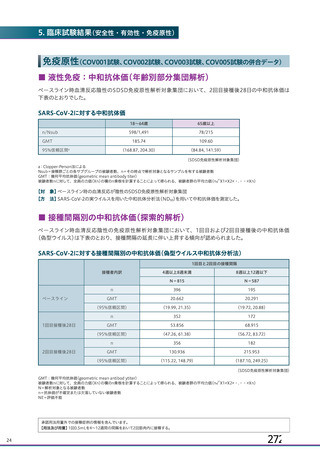
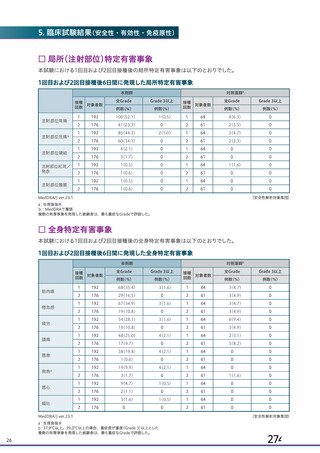
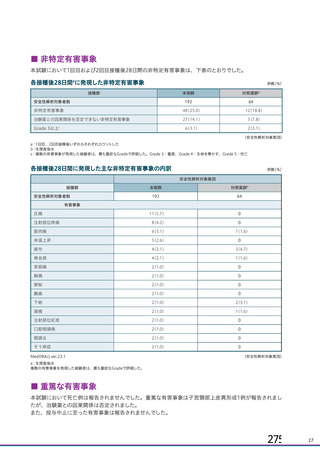
資 料4-1 令和3年度第6回安全技術調査会の審議結果について (251 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
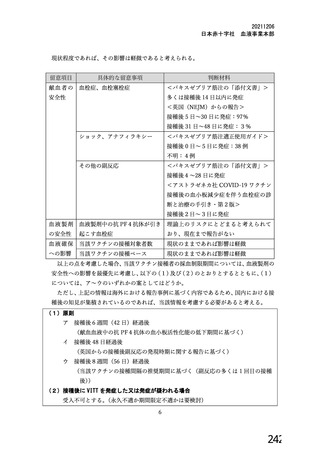
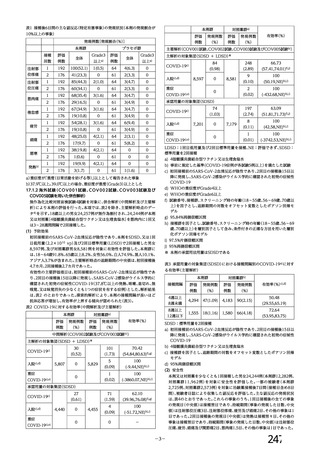
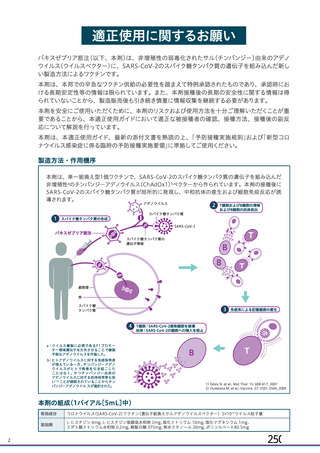
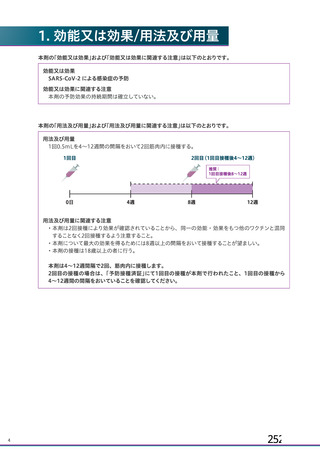
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
日本標準商品分類番号 876313
販売開始後6ヵ月間
適正使用ガイド
医薬品の適正使用に欠かせない情報ですので、ご使用前に必ずお読みください。
本剤は、本邦で特例承認されたものであり、承認時において長期安定性等に係る情報
は限られているため、製造販売後も引き続き情報を収集中である。
本剤の使用にあたっては、あらかじめ被接種者又は代諾者に、本剤に関する最新の有
効性及び安全性について文書で説明した上で、予診票等で文書による同意を得た上で
接種すること。また、有害事象が認められた際には、必要に応じて予防接種法に基づ
く副反応疑い報告制度等に基づき報告すること。なお、本剤の製造販売後に収集され
た情報については、最新の情報を随時参照すること。
本剤は、新型コロナウイルス感染症に係るワクチンの接種事業として接種されます。
本剤の接種にあたっては、最新の添付文書および安全性情報をご確認の上、適正使用をお
願いいたします。最新の添付文書および安全性情報については、アストラゼネカ新型コロ
ナウイルスワクチン 医療関係者向けサイト(https://azcovid-19.jp/)に掲載しております
ので、ご確認をお願いいたします。
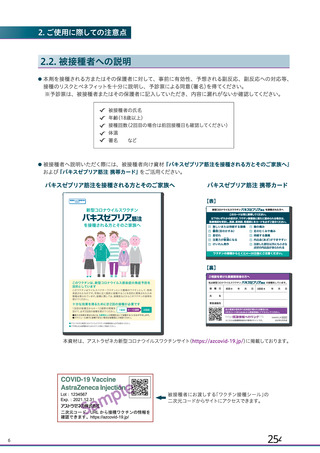
【被接種者に対する情報提供について】
被接種者向け資材「バキスゼブリア筋注を接種される方とそのご家族へ」をアストラゼネ
カ新型コロナウイルスワクチン 医療関係者向けサイトに掲載しておりますので、本剤の安
全性に関する情報、接種に関する注意事項、副反応が発生した場合の対応などについての
説明にご活用ください。
2. 接種不適当者(予防接種を受けることが適当でない者)
2.1 明らかな発熱を呈している者
2.2 重篤な急性疾患にかかっていることが明らかな者
2.3 本剤の成分に対し重度の過敏症の既往歴のある者[8.5、9.1.6、11.1.1 参照]
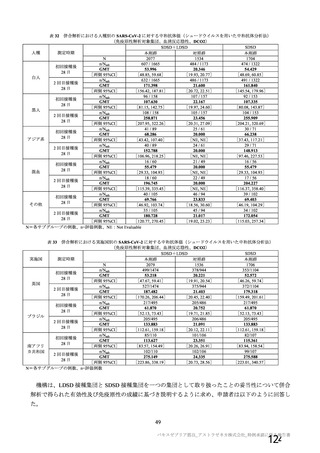
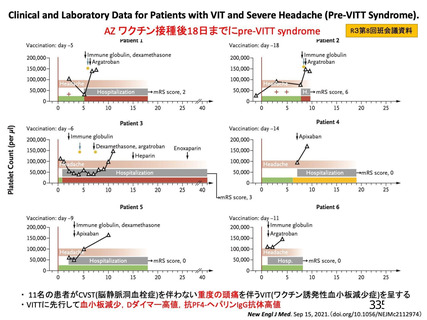
2.4 SARS-CoV-2ワクチンの接種後に血小板減少症を伴う静脈もしくは動脈の血栓症を
発現したことがある者[8.8、11.1.2、15.1 参照]
2.5 上記に掲げる者のほか、予防接種を行うことが不適当な状態にある者
249