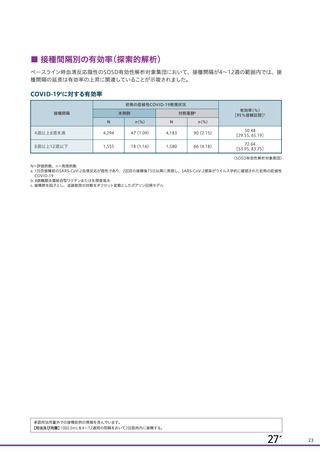
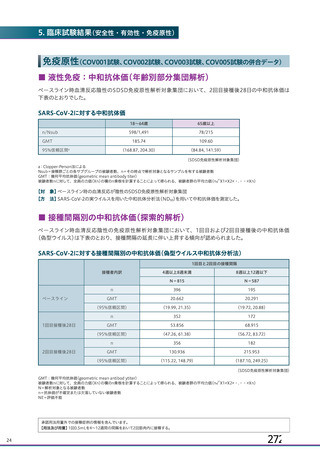
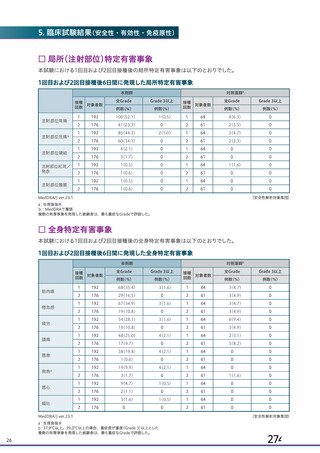
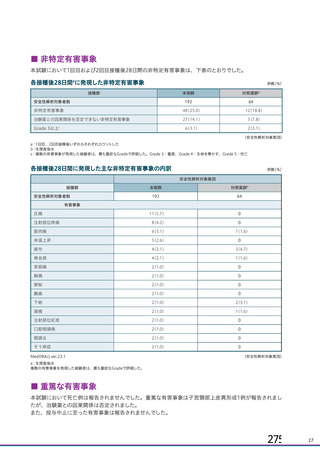
資 料4-1 令和3年度第6回安全技術調査会の審議結果について (244 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26025.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会血液事業部会(令和4年度第1回 6/8)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
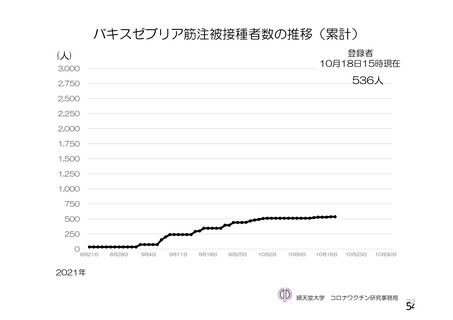
日本赤十字社 血液事業本部
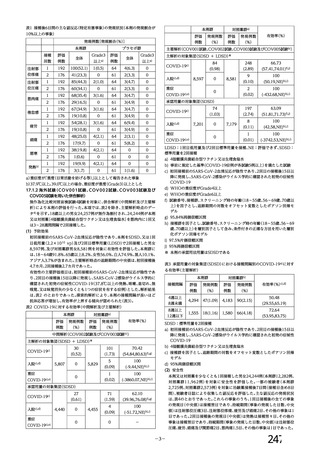
現状程度であれば、その影響は軽微であると考えられる。
留意項目
具体的な留意事項
献血者の
判断材料
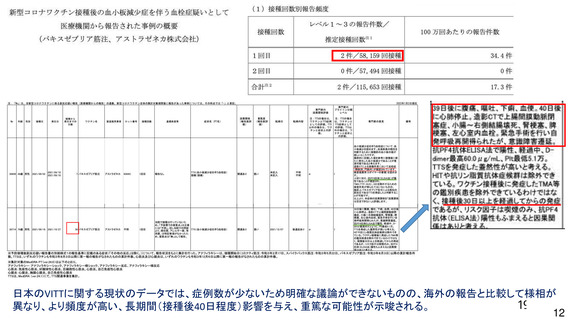
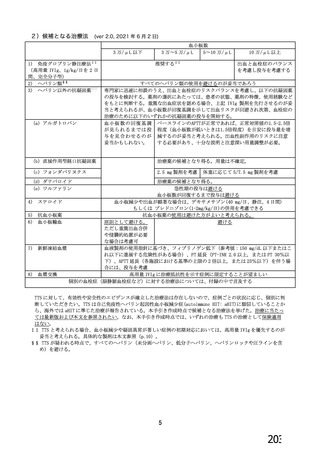
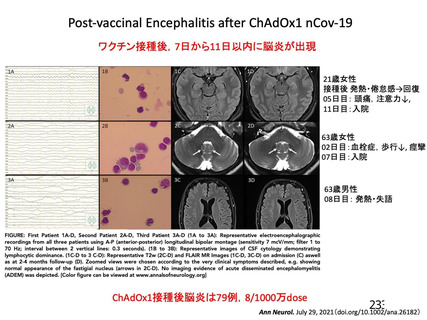
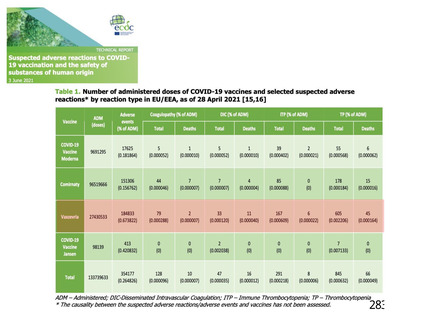
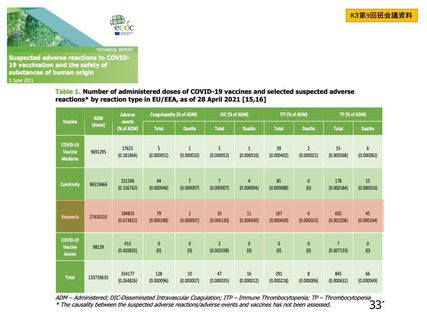
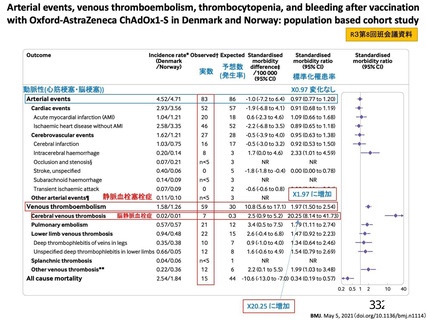
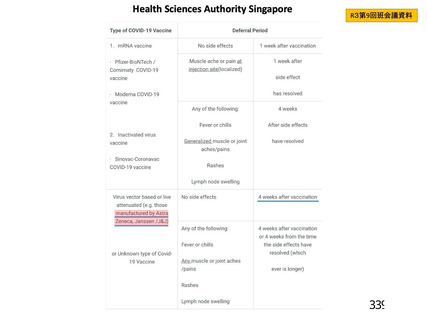
血栓症、血栓塞栓症
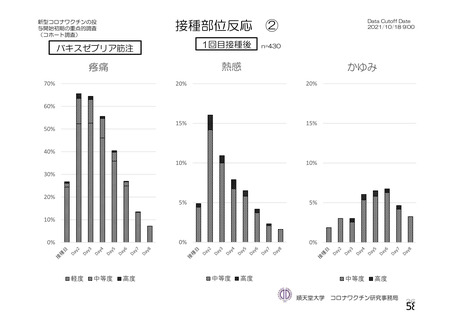
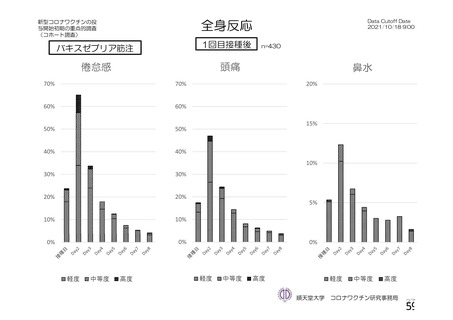
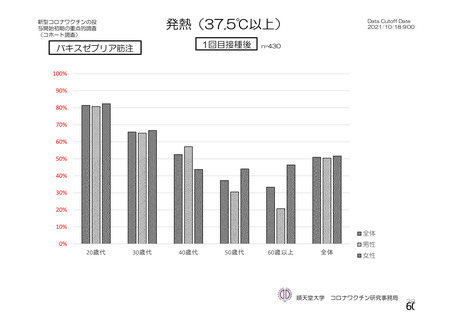
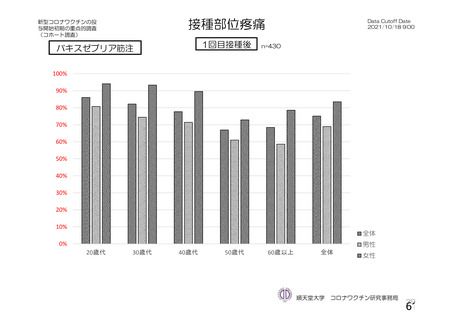
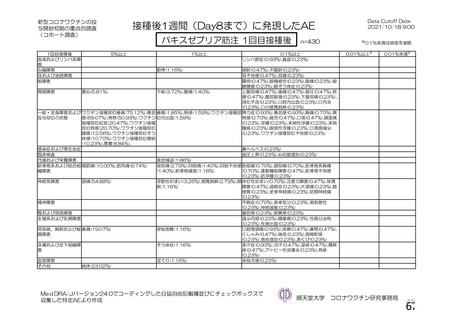
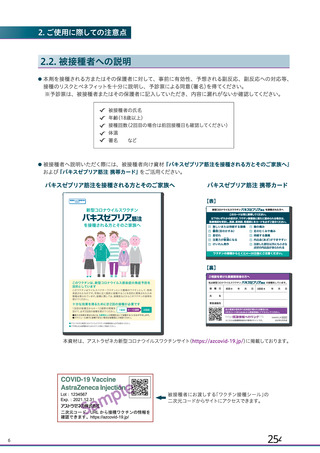
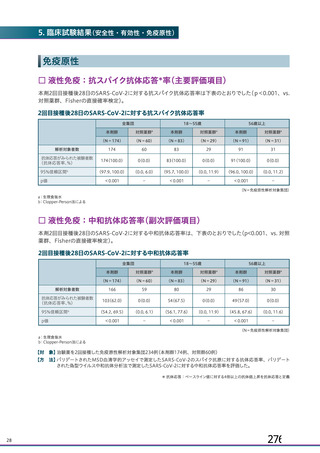
<バキスゼブリア筋注の「添付文書」>
安全性
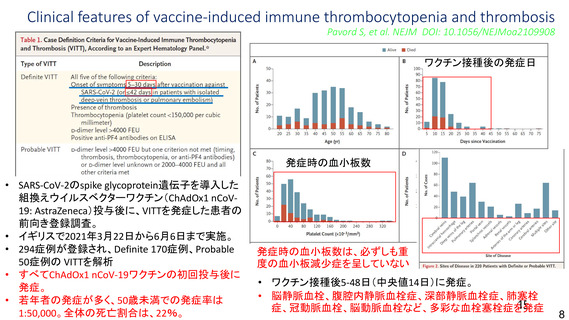
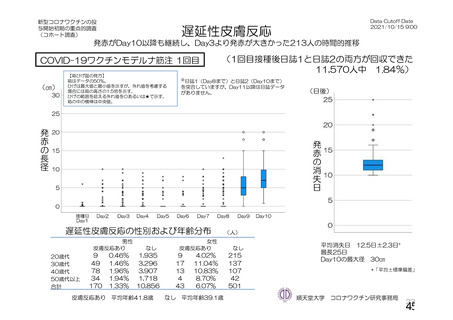
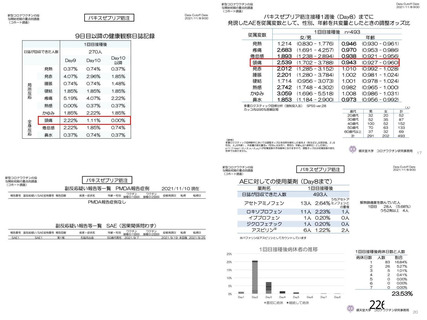
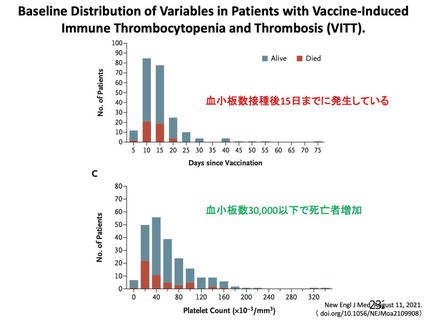
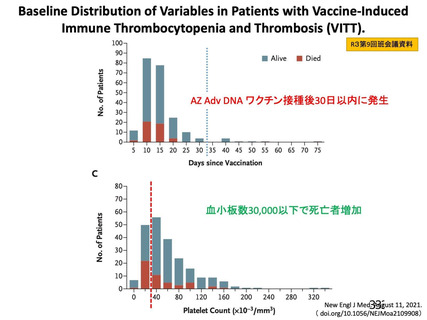
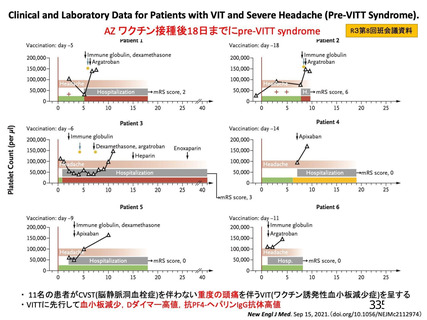
多くは接種後 14 日以内に発症
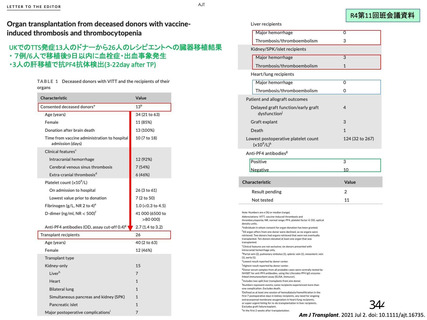
<英国(NEJM)からの報告>
接種後 5 日~30 日に発症:97%
接種後 31 日~48 日に発症:3%
ショック、アナフィラキシー
<バキスゼブリア筋注適正使用ガイド>
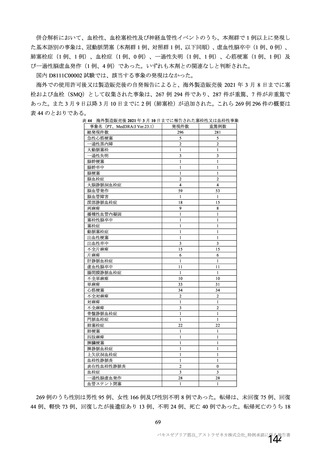
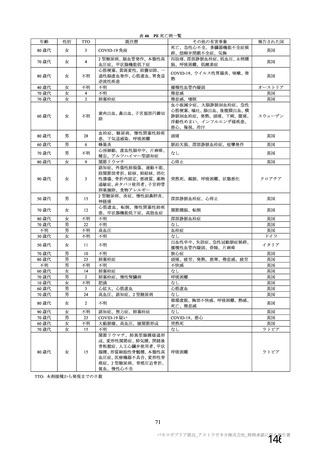
接種後 0 日~5日に発症:38 例
不明:4例
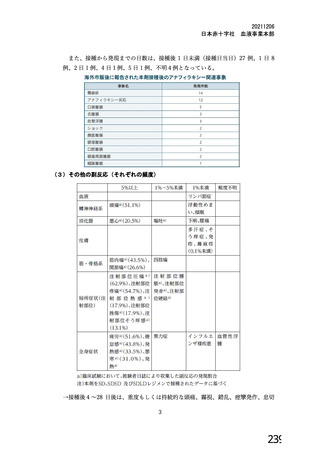
その他の副反応
<バキスゼブリア筋注の「添付文書」>
接種後4~28 日に発症
<アストラゼネカ社 COVID-19 ワクチン
接種後の血小板減少症を伴う血栓症の診
断と治療の手引き・第2版>
接種後2日~3日に発症
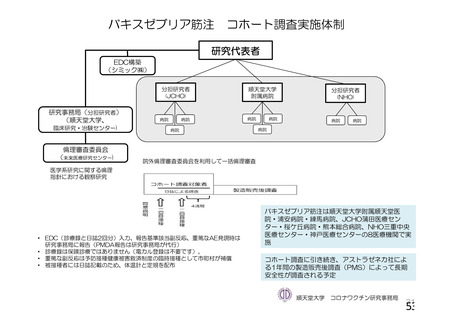
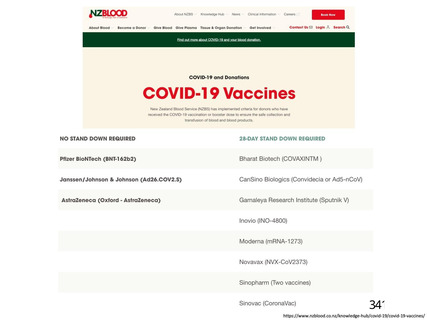
血液製剤
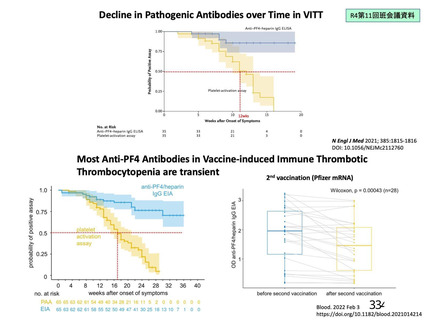
血液製剤中の抗 PF4抗体が引き
理論上のリスクにとどまると考えられて
の安全性
起こす血栓症
おり、現在まで報告がない
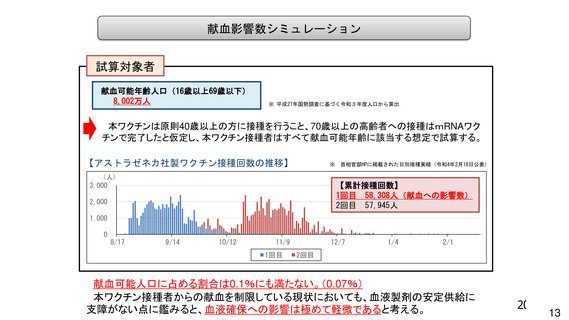
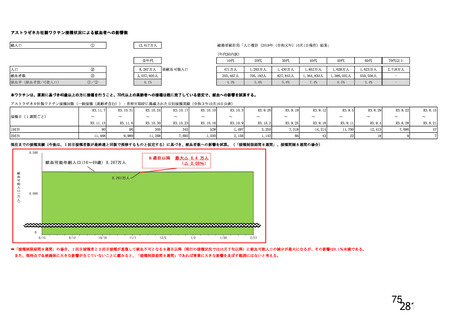
血液確保
当該ワクチンの接種対象者数
現状のままであれば影響は軽微
への影響
当該ワクチンの接種ペース
現状のままであれば影響は軽微
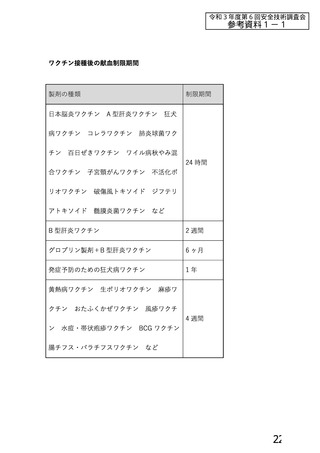
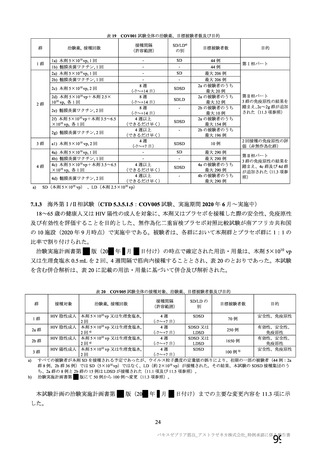
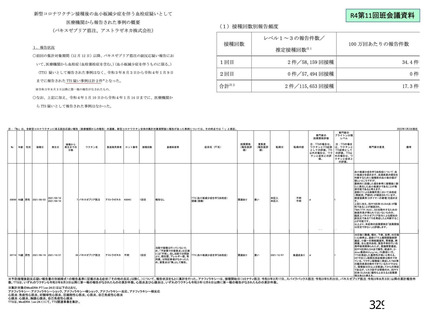
以上の点を考慮した場合、当該ワクチン接種者の採血制限期間については、血液製剤の
安全性への影響を最優先に考慮し、以下の(1)及び(2)のとおりとするとともに、
(1)
については、ア~ウのいずれかの案としてはどうか。
ただし、上記の情報は海外における報告事例に基づく内容であるため、国内における接
種後の知見が集積されているのであれば、当該情報を考慮する必要があると考える。
(1)原則
ア
接種後6週間(42 日)経過後
(献血血液中の抗 PF4抗体の血小板活性化能の低下期間に基づく)
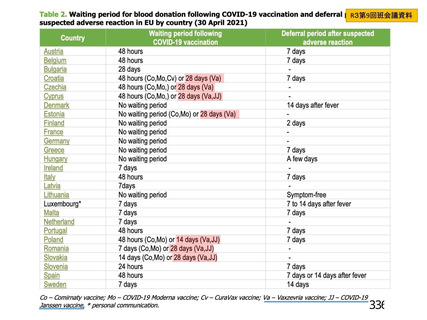
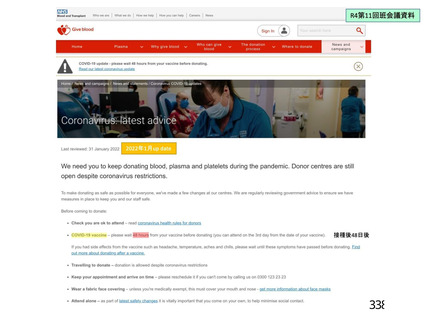
イ 接種後 48 日経過後
(英国からの接種後副反応の発現時期に関する報告に基づく)
ウ
接種後8週間(56 日)経過後
(当該ワクチンの接種間隔の推奨期間に基づく(副反応の多くは 1 回目の接種
後))
(2)接種後に VITT を発症した又は発症が疑われる場合
受入不可とする。
(永久不適か期間限定不適かは要検討)
6
242