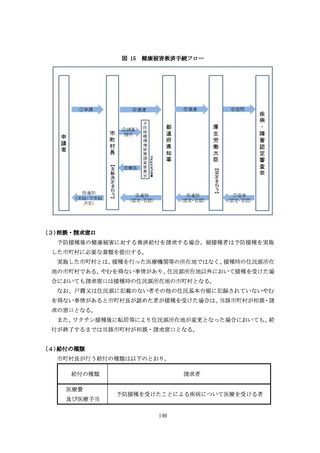
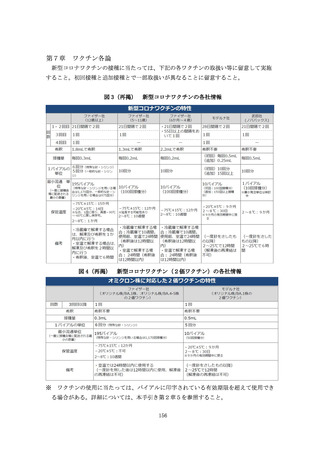
「新型コロナウイルス感染症に係る予防接種の実施に関する手引き」の改訂について(通知) (189 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/content/001004080.pdf |
| 出典情報 | 「新型コロナウイルス感染症に係る予防接種の実施に関する手引き」の改訂について(10/21付 通知)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
の予防接種を除く。)を同時に同一の接種対象者に対して行わないこと。
(エ)その他
接種箇所及び接種後の経過観察については、(1)ア(イ)d 及び e の記載事項
に従うこと。
ウ
「前条第一項各号の注射に相当するもの」について
実施規則附則第9条第2項の「新型コロナウイルス感染症に係る注射であって、前
条第一項各号の注射に相当するもの」は第一期追加接種とみなして、第二期追加接種
を行うこと。「前条第一項各号の注射に相当するもの」とは、初回接種完了後に次の
接種において行われた注射をいう。
(ア)海外在留邦人等向け新型コロナワクチン接種事業において行われた当該被接種
者にとって3回目の接種
(イ)在日米軍従業員接種において行われた当該被接種者にとって3回目の接種
(ウ)製薬メーカーの治験等において行われた当該被接種者にとって3回目の接種
(エ)海外において行われた当該被接種者にとって3回目の接種
(オ)上記の他、市町村長が第一期追加接種に相当する予防接種であると認めるもの
ただし、医薬品医療機器等法第 14 条の承認を受けた新型コロナワクチンを接種し
ている場合に限る。
なお、復星医薬(フォースン・ファーマ)/ビオンテック社が製造する「コミナテ
ィ(COMIRNATY)」及びインド血清研究所が製造する「コボバックス(COVOVAX)」に
ついては医薬品医療機器等法第 14 条の承認を受けた新型コロナワクチンと同一のも
のとして取り扱う。
(3)令和四年秋開始接種
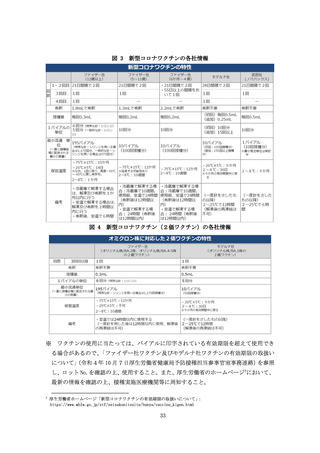
ア オミクロン株対応モデルナ社コロナウイルス修飾ウリジンRNAワクチン(SA
RS―CoV―2)
コロナウイルス修飾ウリジンRNAワクチン(SARS―CoV―2)(武田薬品
工業株式会社が令和3年5月 21 日に医薬品医療機器等法第 14 条の承認を受けたもの
であって、エラソメラン及びイムエラソメランを含むものに限る。以下「オミクロン
株対応モデルナ社コロナウイルス修飾ウリジンRNAワクチン(SARS―CoV―
2)」という。)の令和四年秋開始接種は、以下の方法により行うこととすること。
なお、1(4)イ予防接種要注意者の(ア)に関し、抗凝固療法を受けている者、
血小板減少症又は凝固障害を有する者については、接種後に出血又は挫傷があらわれ
ることがあり、予防接種要注意者に該当すること。
(ア)対象者
18 歳以上の者
15