令和8年度予算の主要事項 (49 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72833.html |
| 出典情報 | 社会保障審議会(第34回 4/27)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
令和 8 年度当初予算案 42厨方貼 ( - ) % Oda生度当初算字
1 事業の目的
〇 先行するバイオ医薬品と同等同質であり、安価なバイオ後続品 (【イオシミラー) について、医療保険制度の持
使用されやすい環境を整備する必要がある。
〇 医療機関におけるバイオ後続品の使用に関する考え方として、品質や有効性、安全性に疑問がないバイオ後続品は
積極的に使用するとの声が多く、普及啓発の観点からは、これらの情報を整理し、対外的に発信していくことが重要
である。また、ごこうした情報は、医療現場におけるバイオ後続品活用のために必要であり、迅速に取り組お必要があ
ると指摘されている。
〇 ごこのため、①品質の観点から同等性に関する客観的な評価を実施するとともに、⑦医療情報DBを活用 して切替時
の有効性及び安全性に関するデータを取得し、③ワンス トップで情報を公表し普及啓発を図ることにより、品質、有
効性及び安全性が確保されたバイオ後続品の活用推進につなげる。
続可能性を維持する上で更なる使用促進が不可欠。 バイオ後続品の特性や使用状況等を考慮しつつ、バイブ後続品が
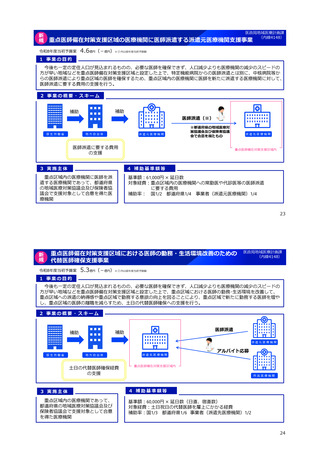
2 事業の概要・スキーム 3 実施主体等
EE 昌和
医療情報 ミ
費用内訳
品質デ ータのほか * 品質試験検査費
5えh和の有用人 ・使用実態下での上床的同等性評価
ジェネリック医楽品・ ・会議費
バイオシミラー品質情報検討会
評価結果の積極的な公表・周知
品質、有効性及び安全性が確保された
バイオシミラーの活用推進
ジエネリック医薬品等の承認申請に係るデータの適合性調査の 曲Es
医薬品審査管理課
体制強化事業 (内線2737)
令和 8 年度当初予算案 12中 (12生円) 0 MG年当初予算
1 事業の目的
7/5
〇 近年の医薬品の品質不良・供給不については、後発品市場において、共同開発 ※) や外部への製造委託などの
導入・活用による多数企業の参入が進み、少量多品目生産構造が生じたことが一因と指摘されている。
(※) 製造販売申請に必要な品質試験等のデータについて、ある企業が取得したデータを他の複数企業間で共有し、同じデータを用いて各社が
申請を行うこと。 後発品については、平成17年の改正薬事法施行にあわせ、認められるようになった。ただし、委託元の企業自身が、委旗
先のデータの信頼性や製造・品質管理の体制について、十分に把握し、責任を負うことが必須。
〇 本事業では、品質・供給問題の発生を未然に防止するため、後発唱の承認奮仁に当たり、以下の確認を実施する。
・適合性調査において、開発・製造を他社に委託する製品について、委託元 (申請者) が委託先における製品デー
夕の信頼性や製造・品質管理の状況を確認するための体制や実際の確認状況について、確認する。
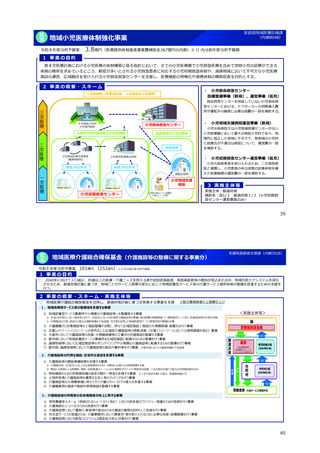
2 事業の概要・スキーム 3 実施主体等
ュ 発品 企 ーー
naa 承認申請 ME 実施主体 : PMDA
ーー 商用内訳:
会性
時 半 - ・人件費 (2名) :補助率50/100
しブー
@ 委託先における製品データの信頼性や製造・品
質管理の状況を適切に確認しているか
[実績|
後発医療用医薬品適合性調査件数 (新規) (令和6 年度) : 78件
76