資料3-1 リツキシマブ(遺伝子組換え)[2.5MB] (87 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第68回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号;IV-169
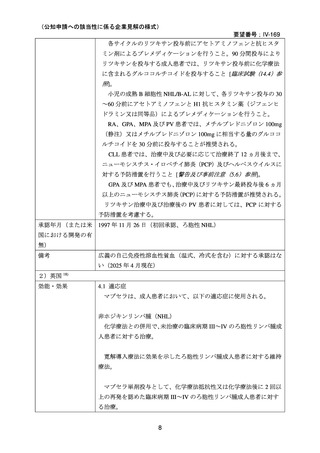
尋常性天疱瘡患者に対するマブセラの推奨投与量は 1 回当たり
1000mg の静脈内投与であり、グルココルチコイドの漸減コースと組み
合わせ、2 週間間隔で 2 回静脈内投与を行う。
維持療法
12、18 ヵ月に 500mg の維持投与を行い、その後は臨床評価に基づき、
必要に応じて 6 ヵ月毎に投与する。
再発の治療
再発時は、1000mg を静脈内投与する。医師は、臨床評価に基づき、
グルココルチコイドの投与量の維持又は増量も考慮すべきである。
その後の投与は、前回の投与から 16 週間以上間隔を空ける。
特別な患者集団への投与
小児
非ホジキンリンパ腫
6 ヵ月齢以上 18 歳未満の小児の未治療進行性 CD20 陽性
DLBCL/BL/BAL/BLL 患者において、マブセラは全身性の Lymphome
Malin B(LMB)化学療法と併用して投与すること(表 1、2 参照)。マ
ブセラの推奨投与量は 375 mg/m2(体表面積)で、投与方法は静脈内
投与とする。BSA 以外を用いた用量調整は実施しないこと。
未治療進行性 CD20 陽性 DLBCL/BL/BAL/BLL 以外の疾患における、
6 ヵ月齢以上 18 歳未満の小児患者に対するマブセラの有効性、安全性
は確立していない。なお、3 歳以下の患者に関するデータは限られて
いる。詳細については 5.1 の項を参照。誕生から 6 ヵ月齢未満の小児
の CD20 陽性 DLBCL 患者に対しては使用を控えること(5.1 参照)。
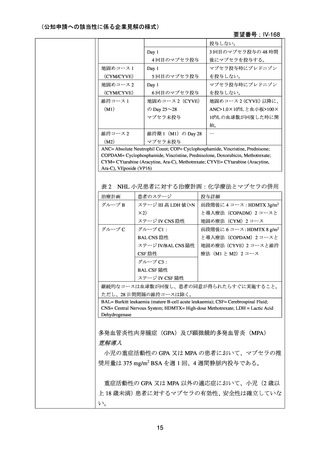
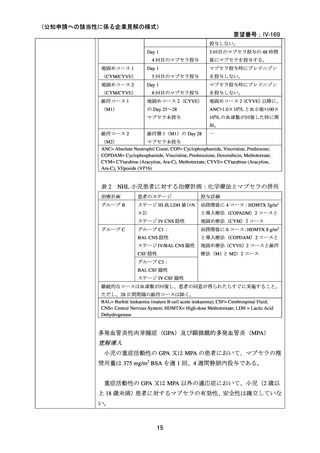
表1
NHL 小児患者に対するマブセラ投与量
サイクル
治療日
投与詳細
前段階(COP)
マブセラ未投与
―
導入コース 1
Day -2
初回導入コース期間中、マブセ
(COPDAM1)
(COP pre-phase の 6 日目
ラ投与前にプレドニゾンを化学
に対応)
療法コースの一部として投与す
初回マブセラ投与
る。
Day 1
初回のマブセラ投与から 48 時間
2 回目のマブセラ投与
導入コース 2
(COPDAM2)
Day -2
3 回目のマブセラ投与
14
後にマブセラを投与する。
2 回目の導入コースにおいて、マ
ブセラ投与時にプレドニゾンを