資料3-1 リツキシマブ(遺伝子組換え)[2.5MB] (113 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第68回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号;IV-169
(3)AIHA(共通)に関する報告
1)AIHA を対象としたリツキシマブの有効性及び安全性に関する後方視的解析 35)
AIHA 患者又は ITP 患者に対する本剤治療に関する多施設共同の後方視的解析がベルギ
ーで実施され、17 施設から AIHA 患者 53 例の解析結果が報告された。
対象患者は、特発性又は続発性の AIHA で、1 種類以上の前治療が奏効せず本剤治療が 1
コース以上実施された患者とした。女性が 28 例(53%)、本剤投与開始時の年齢中央値は
65 歳(範囲 1-87 歳)
、18 例(34%)で基礎疾患を認めず、温式 AIHA が 36 例(68%)、CAD
が 14 例(26%)、不明が 3 例(6%)
、前治療数中央値は 2(範囲 1-4)、脾摘実施例が 10 例
(19%)
、診断から初回本剤投与までの期間中央値は 10 ヵ月(範囲 0.5-132 ヵ月)
、本剤投
与前に輸血が必要だった症例が 26 例
(49%)
、ヘモグロビン値中央値が 8.8 g/dL
(範囲 4.0-14.2
g/dL)であった。
92.7%の症例に対して本剤 375 mg/m2 を週 1 回 4 週間投与し、
本剤単剤投与が 12 例
(22.6%)
でそれ以外の症例では副腎皮質ステロイド薬を含む併用治療が行われた。
CR は免疫抑制療法が実施されない状態でヘモグロビン値が正常化及び溶血の徴候を認
めない場合とし、PR は輸血を実施していた症例では輸血が不要となった場合、及び/又は
ヘモグロビン値が 2 g/dL 上昇とし、それら以外は非奏効とした。
本剤初回投与時の ORR は 79%(42/53 例、CR:47%、PR:32%)
、本剤単剤治療の 12 例
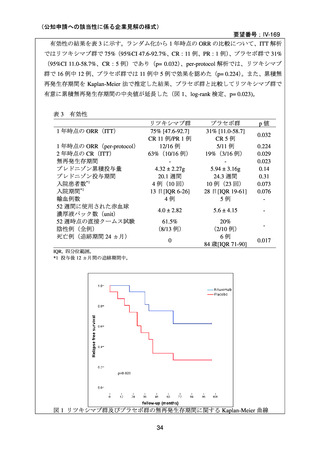
においても、ORR が 75%、CR が 42%、PR が 33%であった。本剤初回投与からの追跡期間
中央値 15 ヵ月(範囲 0-62 ヵ月)時点で、15 例で増悪、再発又は死亡を認め、1 年時及び 2
年時の無再発生存率は 72%及び 56%であった。9 例で本剤の再投与が行われ(2 コース:5
例、3 コース:2 例、4 コース:1 例、5 コース:1 例)
、再投与により奏効期間が長くなる
症例も認められたが、治療成績は初回投与時と同様であった。また、初回投与では効果を
得られなかったものの再治療で PR を認めた 1 例も報告された。
<日本における臨床試験等>
該当なし。
(2)Peer-reviewed journal の総説、メタ・アナリシス等の報告状況
2024 年 3 月 26 日に PubMed.gov(http://www.ncbi.nlm.nih.gov/pubmed)において“rituximab and
(autoimmune hemolytic anemia)”で検索し、日本語又は英語で記載された文献 634 報を得た。
そのうち、英国診療ガイドラインに引用されているリツキシマブ治療に関するメタ・アナ
リシス 1 報及び最新(2023 年公表分)の総説 5 報について以下に概要を示した。
1)Efficacy and safety of rituximab in auto-immune hemolytic anemia: A meta-analysis of 21
studies.(Autoimmun Rev 2015; 14(4): 304-313. 英国診療ガイドライン引用文献)36)
2014 年 3 月時点の MEDLINE から解析対象試験を選択し、2 名の独立した担当者が試験デ
40