資料3-1 リツキシマブ(遺伝子組換え)[2.5MB] (109 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00042.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第68回 7/4)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
要望番号;IV-169
CR を認め、もう 1 例は重症の IgA 関連温式 AIHA であり、MMF で効果を認めなかったが、
脾摘で PR を認めた。
安全性について、2 例(7%)で蕁麻疹及び一時的な多発性関節炎を認めた。CLL(Stage A)
を併存する 1 例(74 歳)で重症の好中球減少症を認め(本剤 2 回目投与の 4 日目に 0.4×
、5 ヵ月後に回復を認めた。2 例で重症の感染症を認め、1 例(73 歳、膀胱がんの既
109/L)
往、糖尿病が併存、脾摘後皮膚カポジ肉腫を発現)は本剤投与の 2 ヵ月後に大腸菌の血流
感染を伴う急性腎炎を発現し、また、本剤投与の 2 ヵ月後にニューモシスチス・イロベチ
イ肺炎(PCP)を発現し、薬剤治療で PCP は回復したが、敗血症による重症肢虚血で 6 ヵ
月後に死亡した。他の 1 例では、本剤投与の 2.5 ヵ月後に死亡し、心筋梗塞が原因とされ
た。
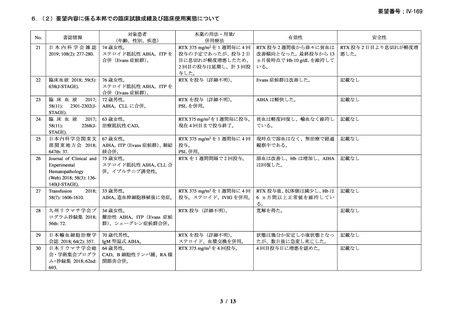
4)温式 AIHA を対象としたリツキシマブ投与に関する後方視的解析(英国診療ガイドラ
イン引用文献)28)
前治療で効果を認めなかった温式 AIHA 患者 34 例(特発性、続発性)に、本剤 375 mg/m2
を週 1 回 4 週間投与した場合の有効性、安全性及び効果持続期間について、後方視的解析
が行われた。
温式 AIHA の診断は、初回診断時のヘモグロビンが 100 g/L 未満、直接クームス試験が陽
性、溶血の徴候を認める患者とし、年齢中央値は 59 歳(範囲 14-38 歳)
、男女比は 1:1.2、
47%(16/34 例)に基礎疾患があり、続発性 AIHA(16 例中 8 例が CLL)に分類された。全
例で副腎皮質ステロイド薬による治療が行われており、
29 例で本剤投与時に併用された(プ
レドニゾンを 10mg から 100mg)
。11 例(32%)で、本剤投与前に 2 種類以上の治療が行わ
れていた。追跡期間中央値は 36 ヵ月(範囲 6-90 ヵ月)であった。
PR は、治療開始後 6 ヵ月以上、ヘモグロビン値がベースラインから 20 g/L 上昇、又は、
ヘモグロビン値 100 g/L 超を維持、CR はヘモグロビン値、ビリルビン及び/又は LDH の正
常化が 6 ヵ月以上継続と定義し、再発はヘモグロビン値が 100 g/L を下回る又は新たな治療
(副腎皮質ステロイド薬の再導入及び増量を含む)が必要な場合とした。
ORR は 70.6%(24/34 例)
、CR は 26.5%(9/34 例)であり、奏効例の 87.5%(21/24 例)
は本剤初回投与から 28 日以内に効果を認め、3 ヵ月時点では全例で奏効を認めた。
奏効例の追跡期間中央値 30 ヵ月(範囲 3-60 ヵ月)時点で、奏効例の 50%で再発を認め、
再発までの期間中央値は 16.5 ヵ月(範囲 9-60 ヵ月)であった。治療開始から 90 日で 70.5%
(24/34 例)が奏効を維持しており、36 ヵ月時点では 28.5%(6/21 例)が奏効を維持し治療
が不要であった。
3 例で、再発時に本剤再投与(375 mg/m2 を週 1 回、4 回投与)を実施し、奏効を認めた。
1 例目は PR で 9 ヵ月後に再発したため再投与を行い、32 ヵ月後の再発まで治療が不要であ
った。2 例目は CR で 5 年間奏効を維持し、本剤再投与後 3 ヵ月間の奏効を確認しており、
3 例目は CR で再発まで 19 ヵ月間奏効を維持し、本剤再投与後は再度 CR を認め、41 ヵ月
間 CR を維持した。
36