提案書18(3402頁~3601頁) (122 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000190899_00011.html |
| 出典情報 | 中央社会保険医療協議会 診療報酬調査専門組織・医療技術評価分科会(令和5年度第1回 11/20)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
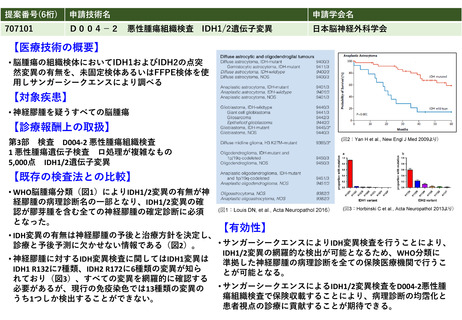
サンガーシークエンス法はIDH1/IDH2のすべての変異を検出できるので研究レベルでは標準となっている(参考文献4な
ど)。R132H以外の抗体を用いた研究は極めて限られており、汎用性に欠ける。
3
⑤ ④の根拠と
なる研究結果等
ガイドライン等での位置づけ
⑥普及性
現在作成・改訂が進められている脳腫瘍診療ガイドライン(日本
ガイドライン等での記載なし(右欄にガイドライン等の
脳腫瘍学会編)において、神経膠腫の診断にIDH変異検査が必須
改訂の見込み等を記載する。)
であることが明記される予定である
年間対象患者数(人)
4,600人
国内年間実施回数(回)
4,000回
※患者数及び実施回数の推定根拠等
2016年全国がん登録によると神経上皮腫瘍(神経膠腫)の年間登録数は4,621人であった(成田義孝、「脳腫瘍の分類と疫
学」日本臨牀79 巻増刊号1、2021)。これは、従来熊本県の1989-2008年の調査及び米国脳腫瘍統計(CBTRUS)のデータをも
とに計算した国内における原発性脳腫瘍の患者数と、脳腫瘍全国集計調査報告2005‐2008 (Narita, Neurol Med Chir
(Tokyo). 2017)による全ての脳腫瘍に対する神経膠腫の割合(22%)から神経膠腫の罹患数を推定した年間約4,400人とほぼ
一致している。本検査は診断確定のため神経膠腫を疑う脳腫瘍全例に行われる必要があるので、自施設で免疫染色などで検
査される症例を除き年間約4,000回実施されることを想定する。稀に再発時に再検査されることもあるが、原則として初回
手術時に検査される。
⑦医療技術の成熟度
・学会等における位置づけ
・難易度(専門性等)
2018年発行の脳腫瘍取扱い規約第4版(日本脳神経外科学会・日本病理学会編)においてIDH1/2変異に基づく神経膠腫の分
類が求められている。また日本脳腫瘍学会が日本脳神経外科学会専門医研修プログラムの全国基幹95施設に対して行った分
子診断の実態に関するアンケート調査(脳神経外科ジャーナル、2019)では保険未収載であるIDH1/2の変異検査が96%の施
設で行われており、検査の標準化と保険収載を望む声が高いという結果が得られた。以上の結果を踏まえ、脳腫瘍、神経膠
腫を扱うすべての保険医療機関での実施が望まれ、かつ神経膠腫の診断が可能な医師が勤務している保険医療機関であるこ
とが望まれる。
・施設基準
(技術の専門性
等を踏まえ、必
要と考えられる
要件を、項目毎
に記載するこ
と)
施設の要件
(標榜科、手術件数、検査や手術の体
制等)
脳神経外科を有する保険医療機関(検査は外注も可とする)
人的配置の要件
(医師、看護師等の職種や人数、専門
性や経験年数等)
脳神経外科専門医が勤務している保険医療機関
その他
(遵守すべきガイドライン等その他の
要件)
IDH変異の有無に基づく分子診断にあたっては脳腫瘍取扱い規約第4版(日本脳神経外科学会・日本病理学会編)およびWHO
脳腫瘍分類(第5版、2021)を参考にすること
⑧安全性
・副作用等のリスクの内容と頻度
本検査は通常の病理組織検体を用いて行われるので、新たなリスクは存在しない。
⑨倫理性・社会的妥当性
(問題点があれば必ず記載)
問題なし
D
妥当と思われる診療報酬の区分
⑩希望する診療
報酬上の取扱い
関連して減点
や削除が可能と
考えられる医療
技術(③対象疾
患に対して現在
行われている医
療技術を含む)
点数(1点10円)
5,000
その根拠
D004ー2悪性腫瘍組織検査の診療報酬点数において、1悪性腫瘍遺伝子検査
た
区分
区分をリストから選択
5,000点に準拠し
特になし
番号
特になし
技術名
特になし
具体的な内容
本検査は現在行われている免疫染色を補完するので、現行の医療技術の減点や削除の必要はない
増(+)
プラスマイナス
予想影響額
ロ処理が複雑なもの
予想影響額(円)
200,000,000
その根拠
(診療報酬点数)5,000点x(年間対象患者数)4,000人x(一人当たりの年間実施回数)1回
備考
特になし
⑪提案される医療技術において使用される医薬品、医療機
器又は体外診断薬
該当なし
(主なものを記載する)
⑫提案される医療技術の海外における公的医療保険(医療
保障)への収載状況
※ 該当する場合、国名、制度名、保険適用上の特徴
(例:年齢制限)等
1)収載されている
1)を選択した場合は、下の欄に詳細を記載。
米国ではIDH検査が神経膠腫に対する標準治療の一環としてMedicareをはじめ各種保険でカバーされている。英国では複数
のNHS施設が検査を提供している。
⑬提案される医療技術の先進医療としての取扱い
d. 届出はしていない
⑭その他
IDH変異を持つ神経膠腫はIDH野生型の腫瘍に比べて有意に予後が良好であり、IDH変異の有無は診断のみならず予後予測と
患者への説明において重要な意義がある。
⑮当該申請団体以外の関係学会、代表的研究者等
該当なし
3523