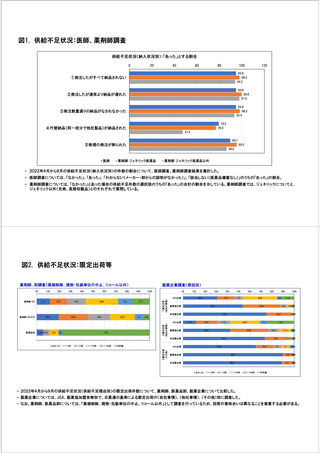
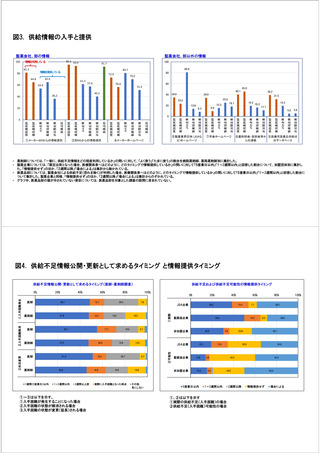
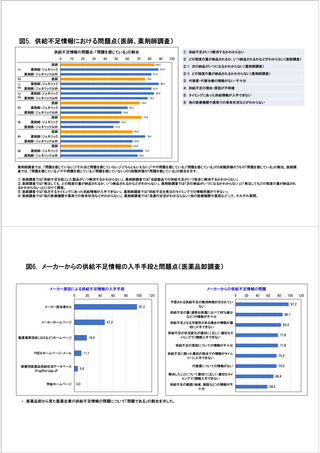
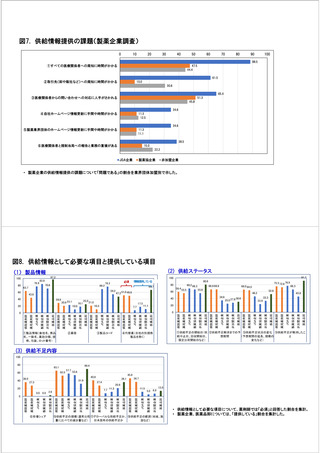
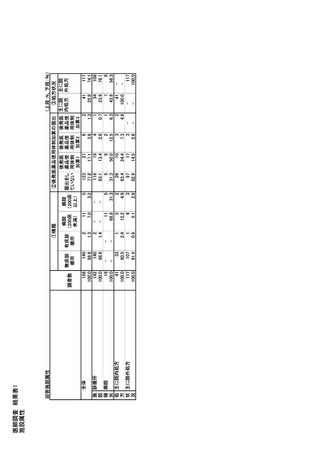
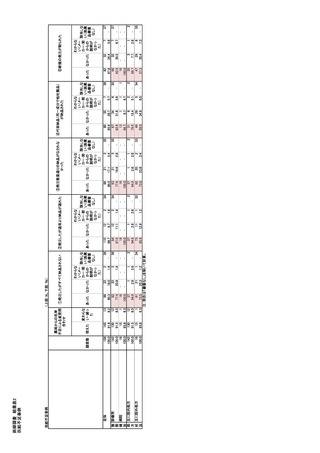
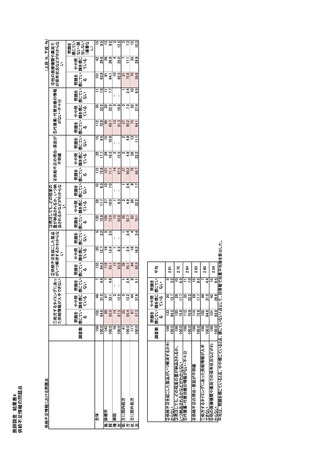
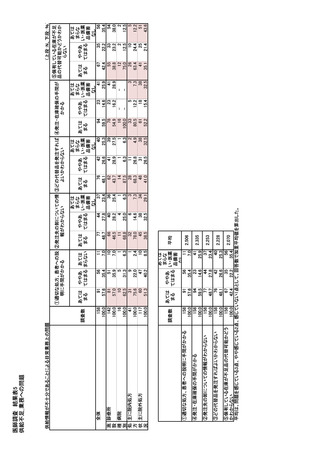
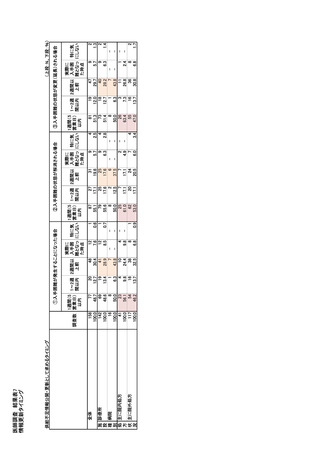
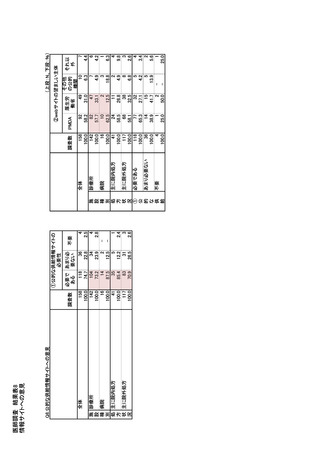
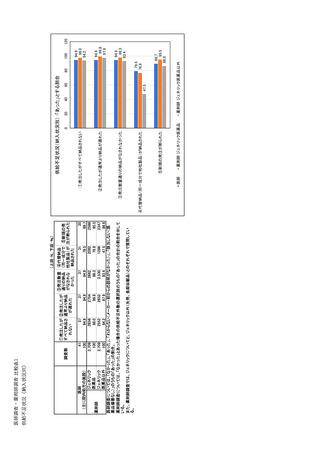
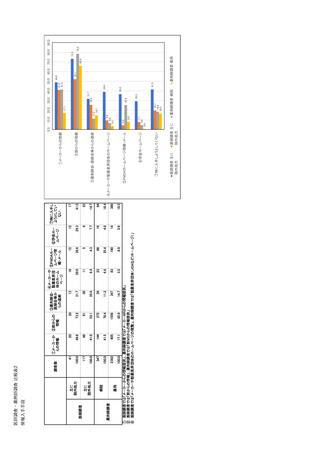
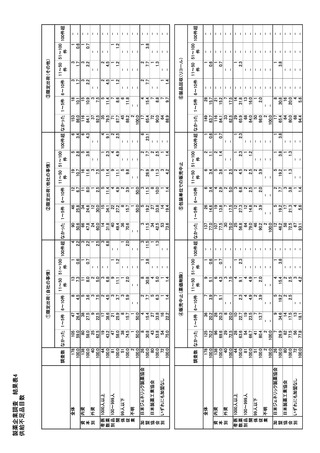
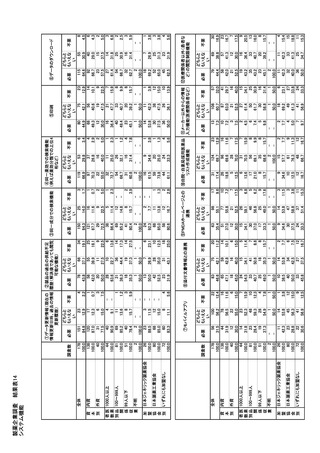
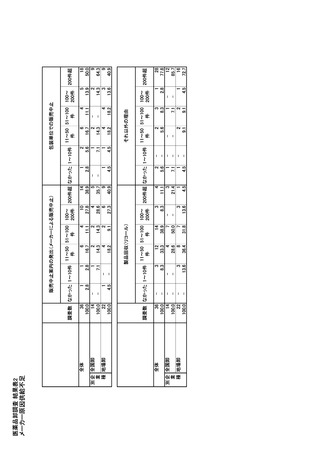
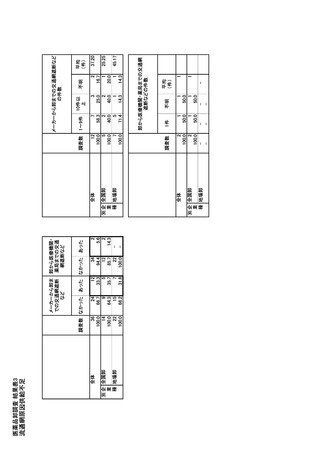
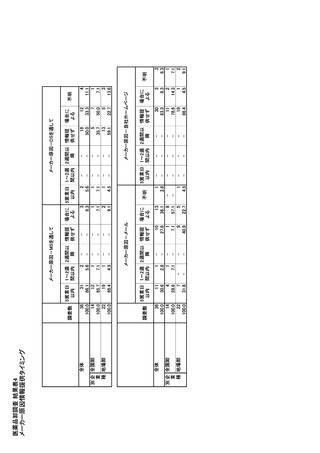
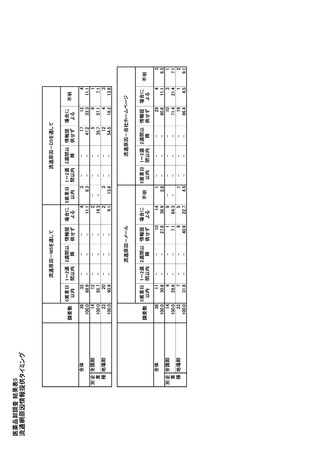
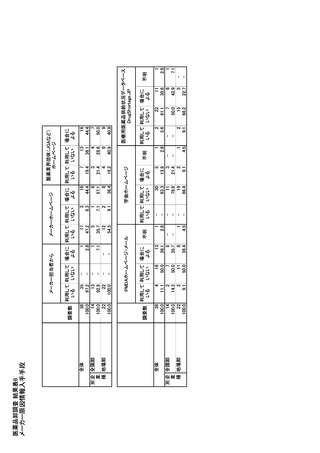
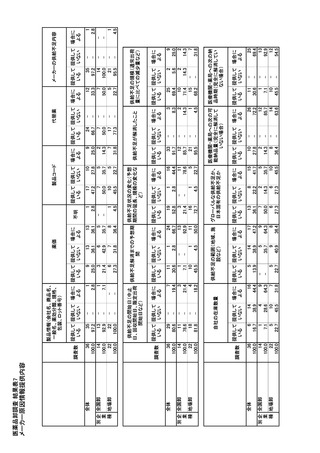
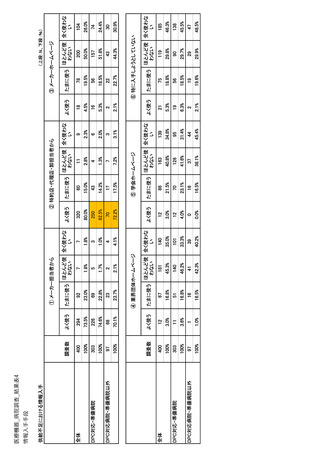
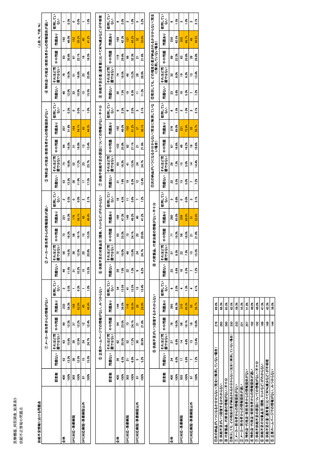
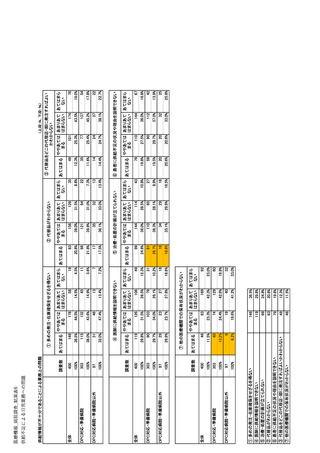
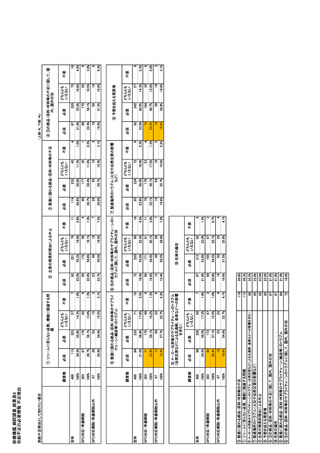
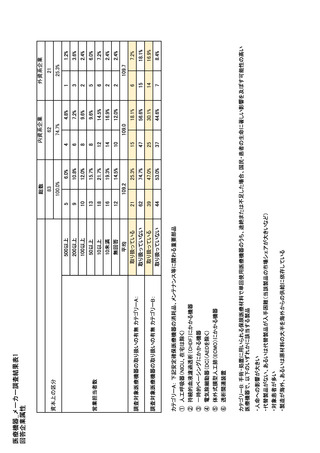
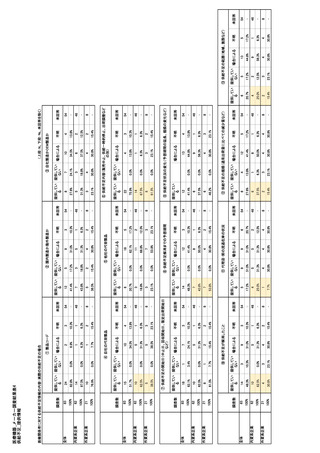
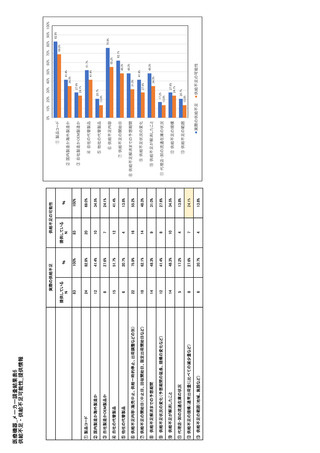
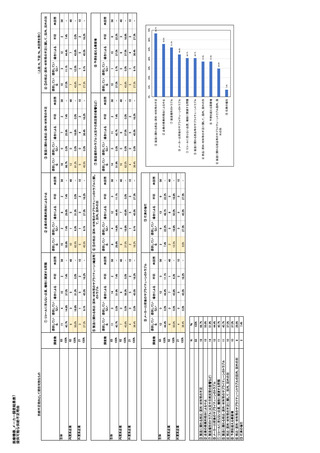
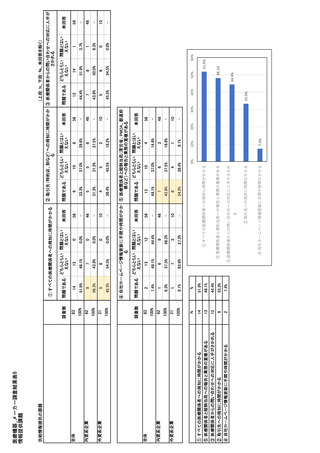
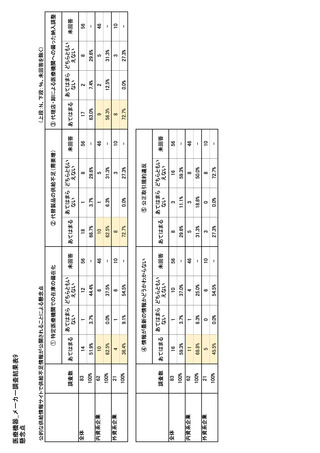
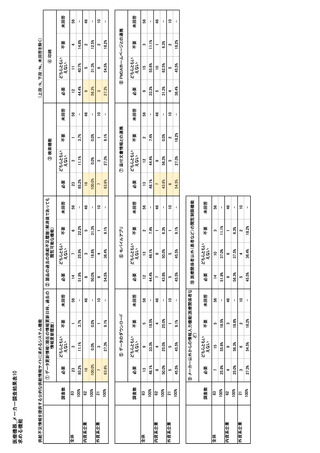
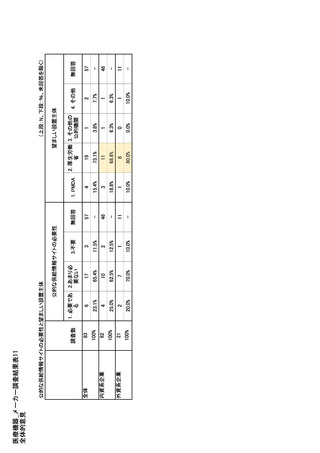
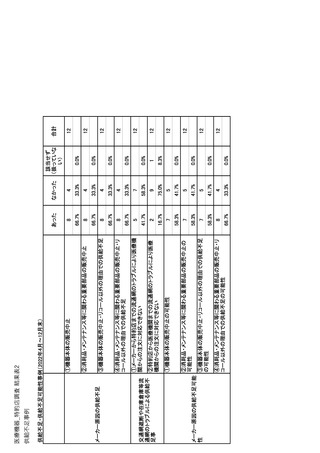
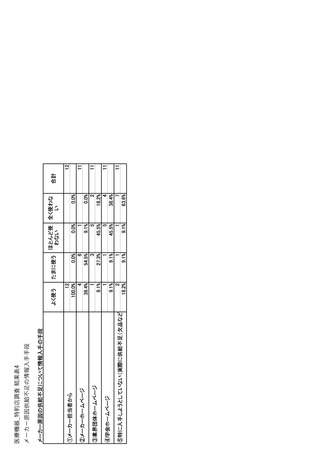
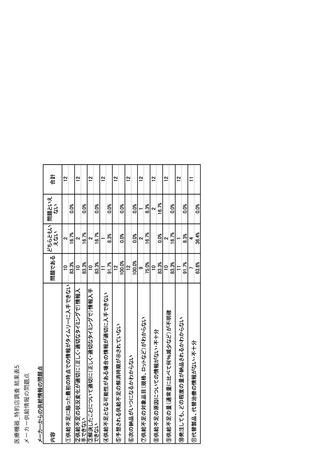
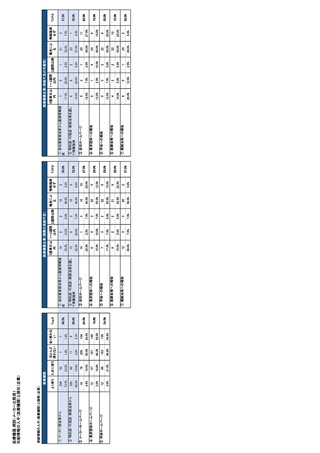
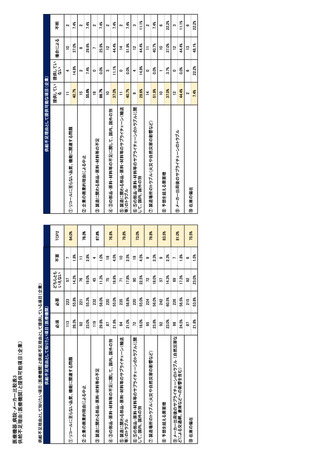
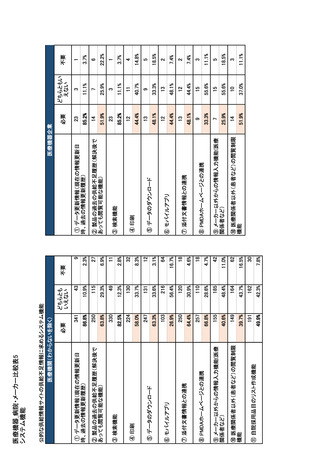
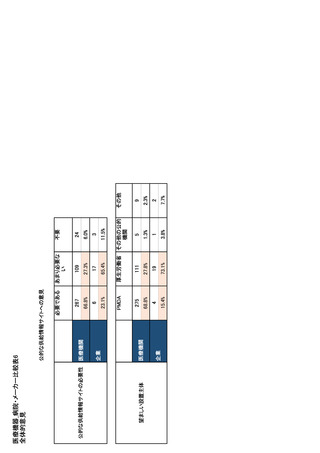
参考資料6 令和4年度厚生労働科学特別研究事業「医療用医薬品・医療機器等の供給情報を医療従 事者等へ適切に提供するための情報システムの構築に向けた研究」(研究代表者:坂巻弘之) (245 ページ)
出典
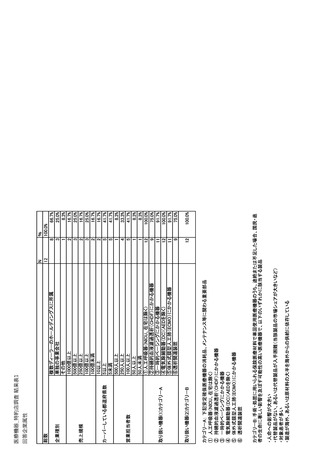
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35103.html |
| 出典情報 | 医療用医薬品の安定確保策に関する関係者会議 供給情報ワーキンググループ(第1回 9/7)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
を行い、ご意見があれば EMA 内に提出する;
に従って連合レベルでとられる措置に関連して、その
(b)
第 8 条(3)及び(4)に言及する勧告並びに第 12 条(c)
措置を調整すること;
に言及するガイドラインを考慮すること;
(c)
(d)
(b)
MSSG に、医薬品の実際の又は潜在的な不足の解消
第 11 条および第 12 条に従って連合国または加盟国
に関する情報の提供を含む、取られた措置及び(a)の
レベルでとられた措置に従うこと;
措置の結果について報告すること。
MSSG に、実際に発生した又は発生しうる医薬品の不
第 1 号、(a)及び(b)の目的のため、国レベルで代替
足の解消に関する情報の提供を含め、講じられた措置
措置をとる加盟国は、その理由を適時に MSSG と共
について報告し、その監視及び結果について報告す
有するものとする。
ること。
第 1 項第(a)号に掲げる勧告、指針及び行動並びに
得られた教訓の概要報告書は、第 14 条に掲げるウ
第 11 条 医薬品の不足の監視と緩和における加盟国の役割
1.
ェブポータルを通じて一般に公開されるものとする。
第 7 条にいうモニタリングを容易にするため、当該情報
が ESMP で入手可能である場合を除き、当機関は、加
第 12 条 医薬品の不足の監視と緩和に関する欧州委員会の
盟国に対し、以下のことを要求することができる:
役割(略)
(a) 第 3 条(6)に規定する単一の窓口を通じて、第 9 条(1)の(b)
(b)
(c)
及び(c)に基づき確立された報告方法及びシステムを
第 13 条 欧州供給不足監視プラットフォーム
それぞれ用いて、需要量及び需要予測に関する入手
1.
EMA は、欧州供給不足監視プラットフォーム(ESMP)と
及び推定データを含む第 6 条(4)の情報セットを提出
呼ばれる IT プラットフォームを設置、維持、管理するも
すること;
のとし、このプラットフォームは、規則(EC)No
第 10 条(4)に従い、商業上の機密情報の存在を示し、
726/2004 の第 57 条(1)項(l)に言及するデータベー
その情報が商業上の機密性を有する理由を説明する
ス通りンクするものとする。
こと;
ESMP は、医薬品の不足、供給及び需要に関する情
は、要求された情報の提供の不履行、及び第 10 条(3)
報の収集を促進するために使用されるものとし、これに
に従って EMA が定めた期限までに当該情報を提供す
は、医薬品が加盟国において市場に置かれるか、又は
ることの遅延の有無について示すこと。
置かれなくなったかに関する情報も含まれる。(以下
略)
加盟国は、EMA の定める期限までに EMA の要請に
応じるものとする。
2.
第 14 条 MSSG に関する連絡事項(略)
第 1 項の目的のため、重要医薬品リストに含まれる医
薬品を公衆に供給する権限又は権利を有する卸売販
第三章(公衆衛生上の緊急事態に対処する可能性のある医
売業者及びその他の者又は法人は、当該加盟国の要
薬品)(略)
請に応じて、当該医薬品の在庫水準に関する情報及
第 15 条 緊急対策本部「ETF」
びデータを含む関連情報及びデータを当該加盟国に
第 16 条 臨床試験に関するアドバイス
提供するものとする。
3.
第 17 条 臨床試験や製造販売承認に関する情報を公開す
加盟国は、本条第 1 項および第 2 項に従って提供さ
る。
れる情報に加えて、指令 2001/83/EC の第 23a 条第 3
第 18 条 医薬品のレビューとその使用に関する推奨事項
項に言及されるデータを含む、重要医薬品リストに含ま
第 19 条 ETF に関する連絡事項
れる医薬品の実際の不足または潜在的不足を証明す
第 20 条 IT ツール・データ
る医薬品の販売量および処方量に関する情報を有す
る場合には、本規則の第 3 条第 6 項に言及するそれ
第四章(重要な医療機器の不足の監視と緩和、および専門家
ぞれの単一の連絡先を通じて、当該情報を直ちに
委員会のサポート)(略)
MSSG に提供するものとする。
4.
第 21 条 医療機器の不足に関するエグゼクティブ・ステアリン
第 7 条にいうモニタリングの結果に関する報告及び第
グ・グループ
8 条(3)及び(4)に従って提供される予防措置又は緩和
第 22 条 重要な医療機器と提供される情報のリスト
措置に関する勧告に続いて、加盟国は、以下を行うも
第 23 条 公衆衛生緊急重要機器リストの医療機器の不足を
のとする:
(a)
監視する
第 12 条(c)にいう勧告及び指針を考慮し、第 12 条(a)
第 24 条 医療機器の欠品に関する報告・勧告について
243