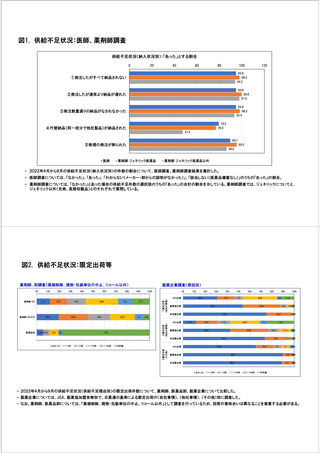
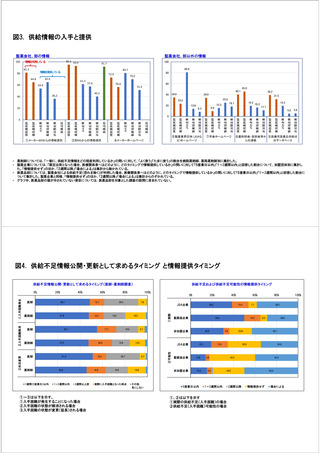
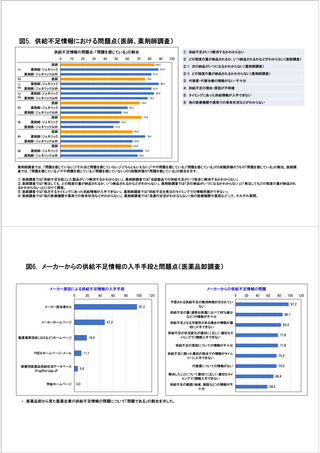
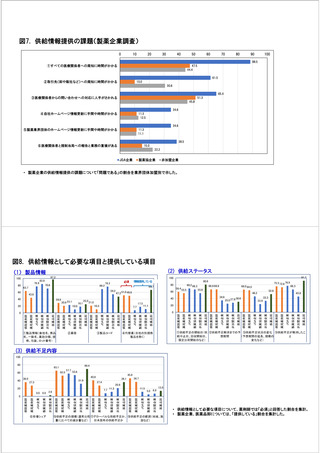
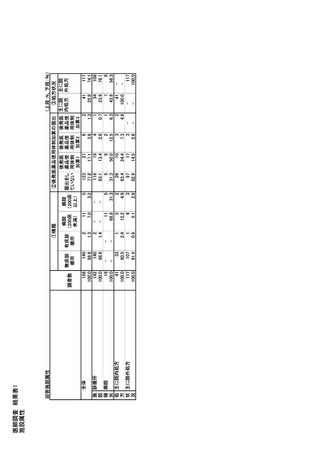
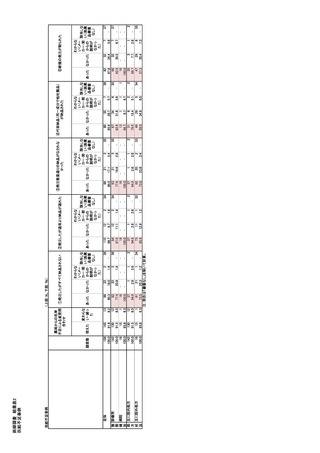
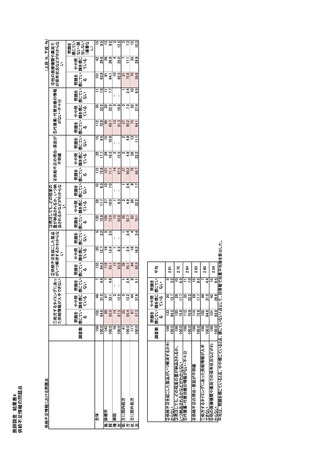
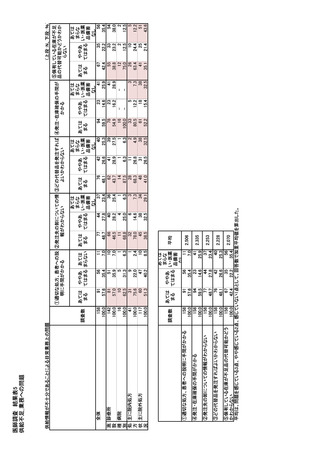
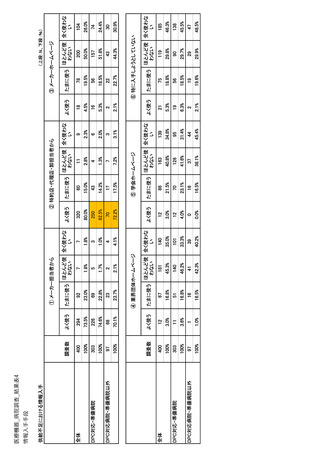
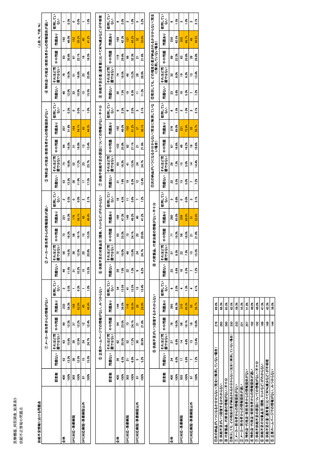
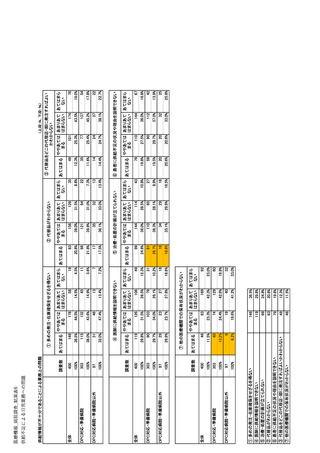
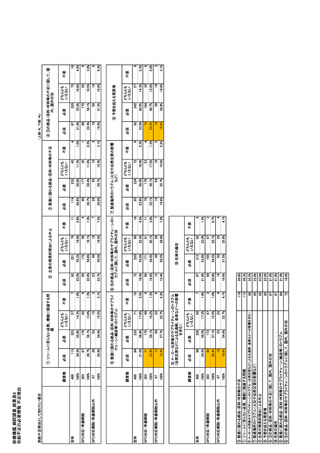
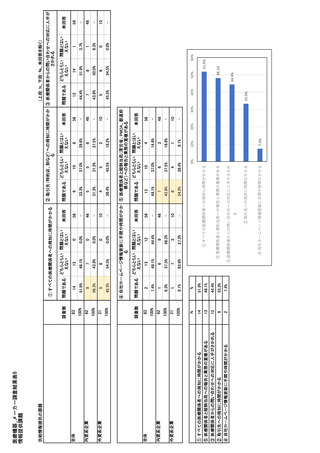
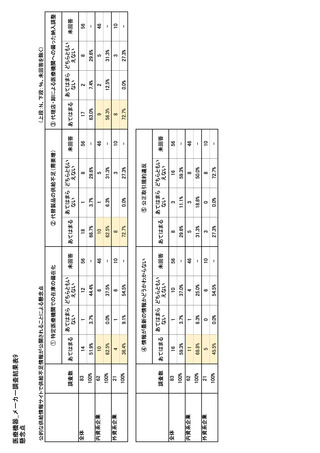
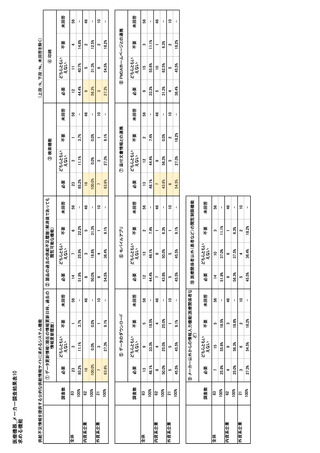
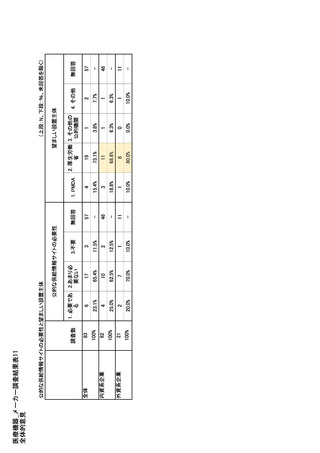
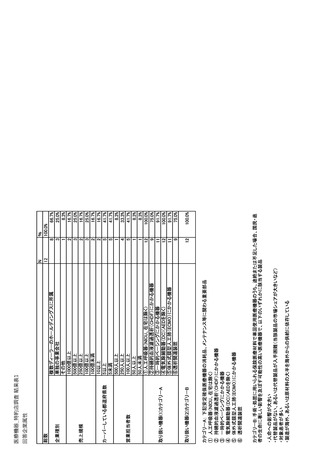
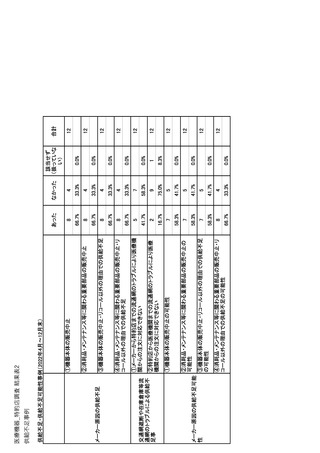
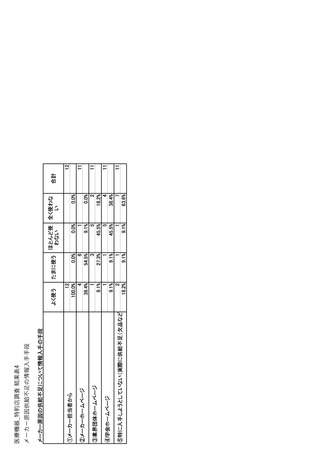
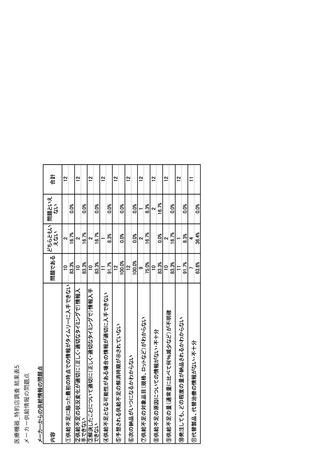
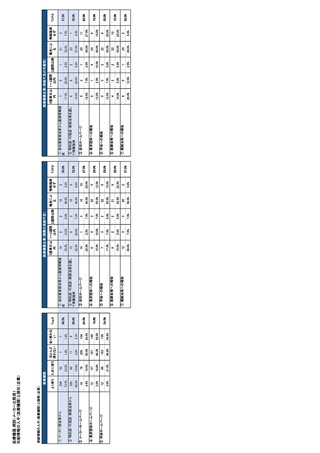
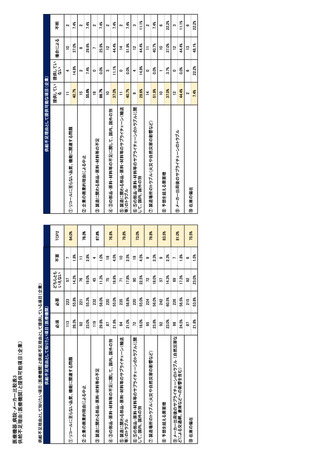
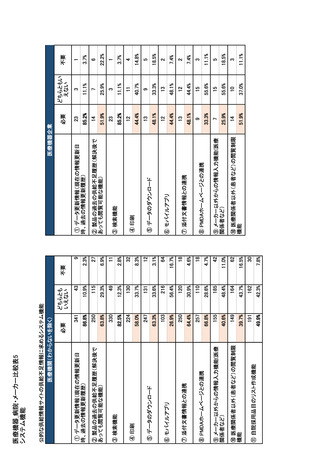
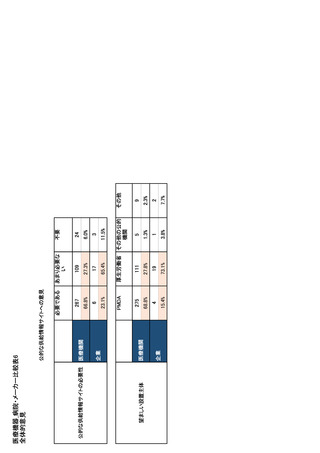
参考資料6 令和4年度厚生労働科学特別研究事業「医療用医薬品・医療機器等の供給情報を医療従 事者等へ適切に提供するための情報システムの構築に向けた研究」(研究代表者:坂巻弘之) (231 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35103.html |
| 出典情報 | 医療用医薬品の安定確保策に関する関係者会議 供給情報ワーキンググループ(第1回 9/7)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
保健省および医薬品サプライチェーンと共同で作成
することができる。有資格者の処方せんは、薬局ある
したガイダンスとして、「ヒト用医薬品の取引:不足とサ
いは薬剤師から、薬剤師の管理下のもとで交付され
プライチェーンの義務」(2013 年 1 月)がある。
る。
(2)供給情報提供
一般用医薬品(Over-the-counter (OTC) drugs:P お
英国においても、医薬品供給不足は深刻な問題
よび GSL)は、一般医薬品評議会(General
であるとされる 10)。英国の供給不足は、EU 離脱によ
Pharmaceutical Council)に登録された薬局におい
る輸入の遅延による影響が懸念される一方で、EU 諸
て、一般消費者に販売できる。なお、医療用医薬品
国と同様に COVID-19 パンデミックやジェネリック医
規制は、開業医、開業歯科医師については管轄外
薬品の価格低下など、根本的な医薬品供給不足リス
である。
ク要因が改善していないとされる 。ここでは、EU 離脱
以前からの英国での医薬品供給不足への一般的な
「卸売り」とは、医薬品のエンドユーザー以外への
制度について概説する。
販売、供給、調達と定義され、卸売り業者が営業して
いる英国または欧州経済領域(European Economic
英国保健省 DHSC は、2019 年 1 月、英国製薬産
業協会 ABPI および英国ジェネリック製薬業協会
BGMA と合意し、医薬品不足を報告するための指針
を公表した 11)。製薬企業は、この指針に基づき、医
薬品不足を DHSC に報告するとともに、供給の問題
を管理し、患者への潜在的な影響を軽減するための
措置をとる必要がある。また、供給情報提供しなかっ
た場合のペナルティとしは、罰金(£1,000)の支払い
義務が生ずる 12)。関連する通知、マニュアルの概要
は以下の通りである。
Area :EEA)の他の国において、その製品の販売承
認がある場合に許可される。卸売業者の免許は、
MAH(販売承認者)から医薬品供給に関わる活動を
認められたものである。英国における卸売業者のライ
センス申請は、eSubmissions ポータルを通じて
MHRA に対して行われる。MHRA は、英国における
卸売販売業者の活動に適用される「医薬品製造業者
および販売業者の規則およびガイダンスのオレンジ
ガイド(Orange Guide of the Rules and Guidance for
① 医薬品の供給と不足を管理するためのガイド
Pharmaceutical Manufacturers and Distributors)」を発
A Guide to Managing Medicines Supply and
Shortages(2019 年 11 月初版発効)13)
行している。
○ DHSC と NHS イングランド・NHS インプルーブメント(NHS
5.医薬品の供給義務と供給不足への対応
England and NHS Improvement:NHSE&I)が共同で 作成
(1)供給義務
したもので、国、地域、地方における医薬品供給問題の管
製品ライセンスの保有者(MHA)は、英国内の患
理・連絡経路を示したもの。中央レベルでの供給不足につ
者のニーズが満たされるように、薬局および製品を供
いて、国、NHS 等の責務、医薬品供給問題に対応する組
織の役割を示し、企業からの情報提供と公表プロセス、ス
給する権限を有する者に対して、証明書に関連する
キームを提示している。また、セカンダリケア、プライマリケ
製品の適切かつ継続的な供給を確保する一般的な
アレベルでの供給不足管理についても示されており、ここ
義務を負う(「ヒト医薬品規則 2012 年第 118 条」
では、薬局の役割等についても記載されている。
regulation 118, Human Medicines Regulations 2012)
② DHSC の報告要件-医薬品の供給不足と製造中
止
8)
。また、MHRA は、2013 年 1 月に公表された「患者
への医薬品の効率的な供給と流通を確保するための
DHSC Reporting Requirements for Medicines
Shortages and Discontinuations(2021 年 4 月 21
日発効)13)
ベストプラクティスに関するガイドライン(Trading
Medicines for Human Use: Shortages and Supply
Chain Obligations)」9)に業界と合意している。さらに、
229