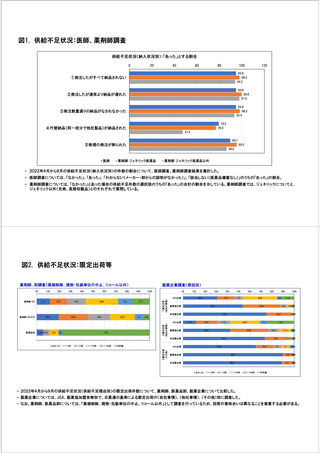
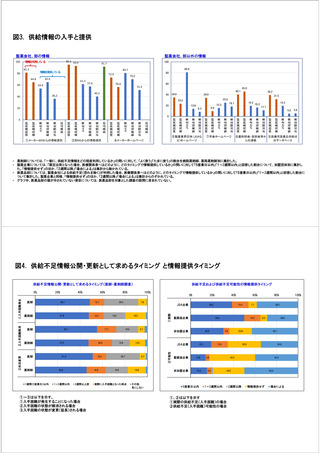
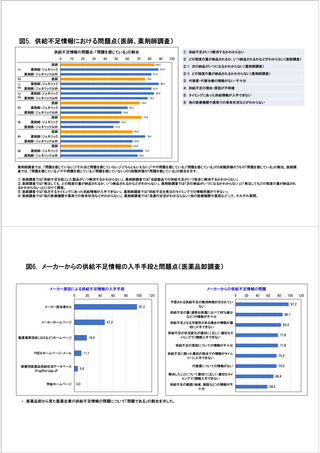
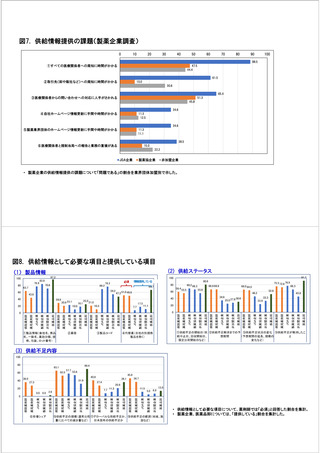
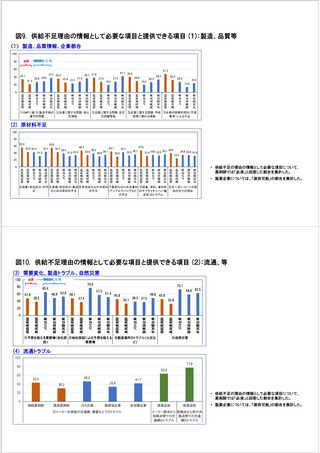
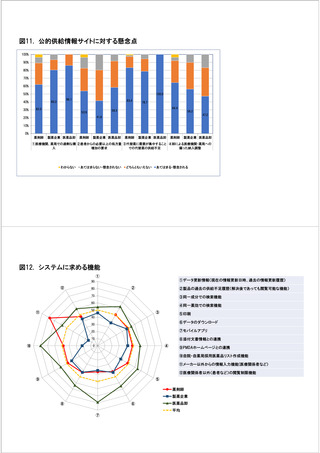
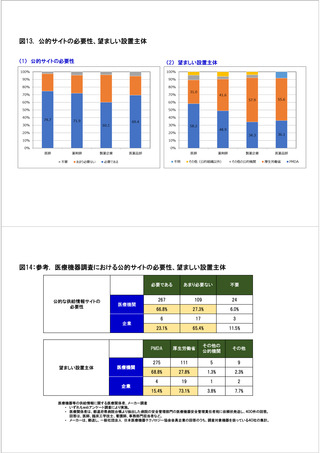
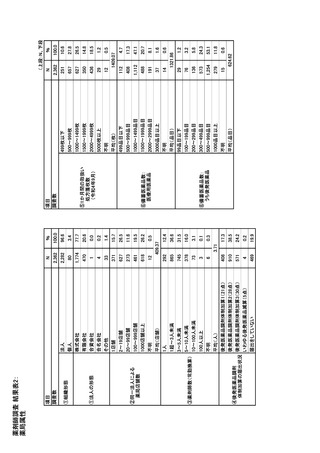
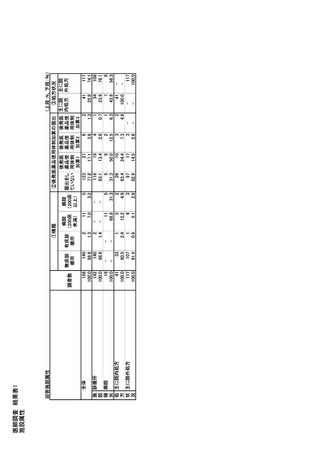
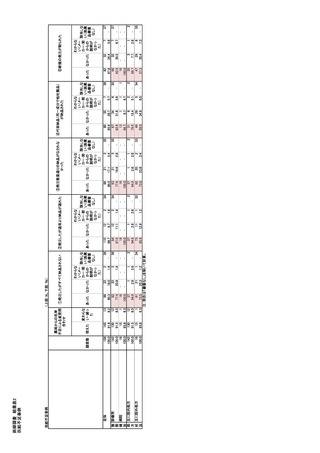
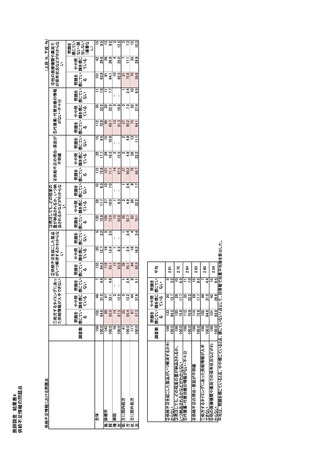
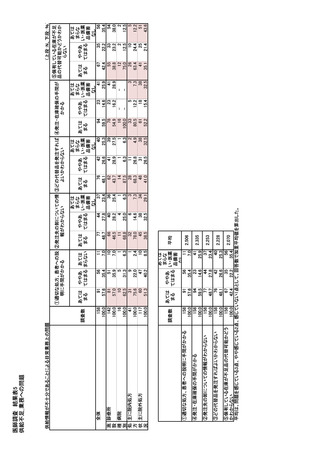
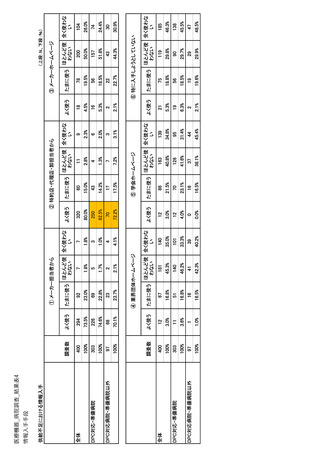
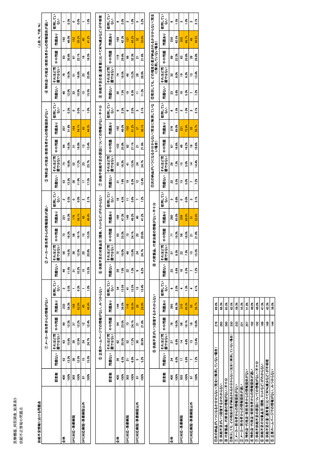
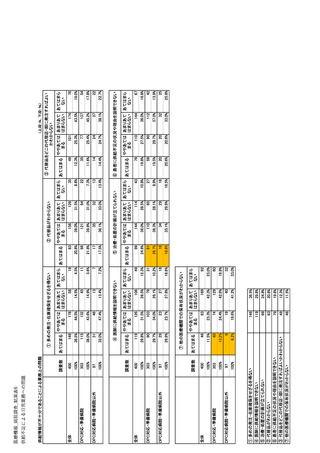
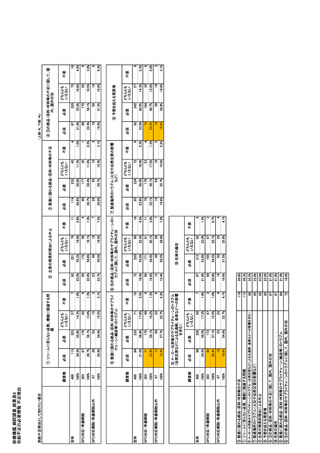
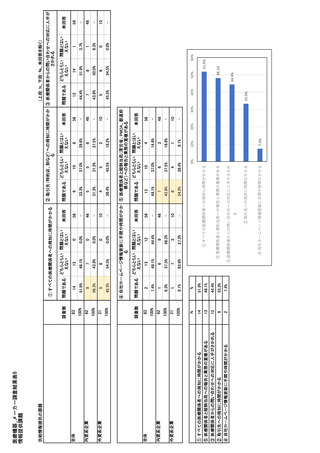
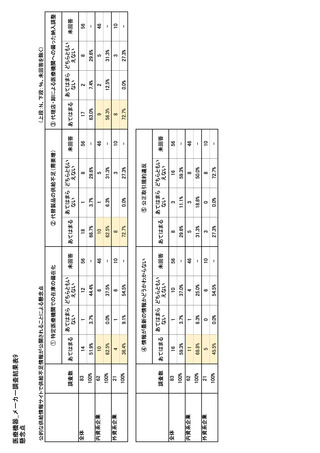
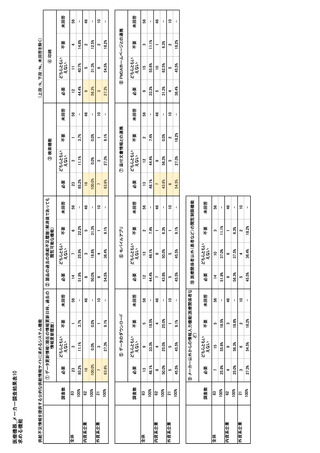
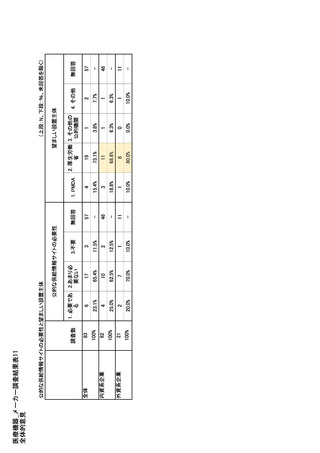
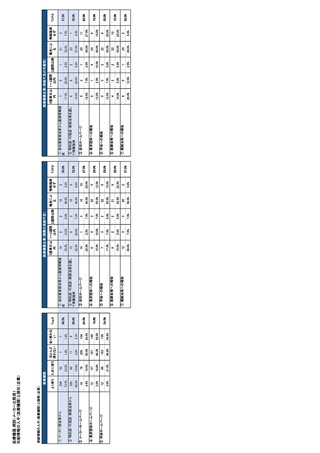
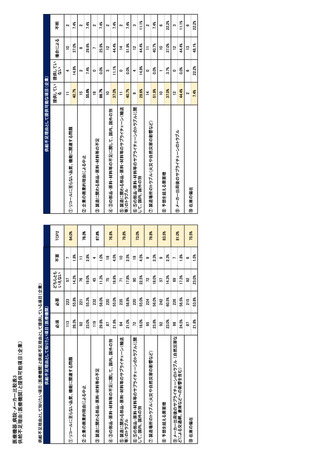
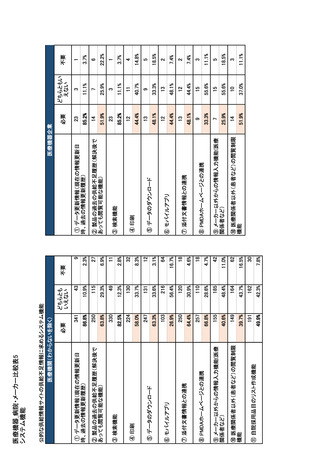
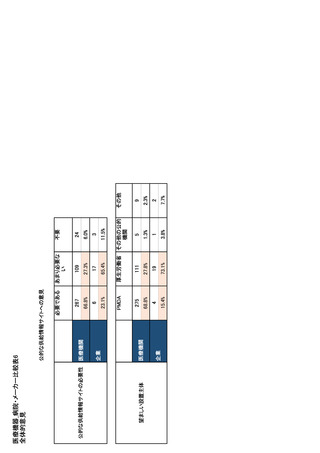
参考資料6 令和4年度厚生労働科学特別研究事業「医療用医薬品・医療機器等の供給情報を医療従 事者等へ適切に提供するための情報システムの構築に向けた研究」(研究代表者:坂巻弘之) (178 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_35103.html |
| 出典情報 | 医療用医薬品の安定確保策に関する関係者会議 供給情報ワーキンググループ(第1回 9/7)《厚生労働省》 |
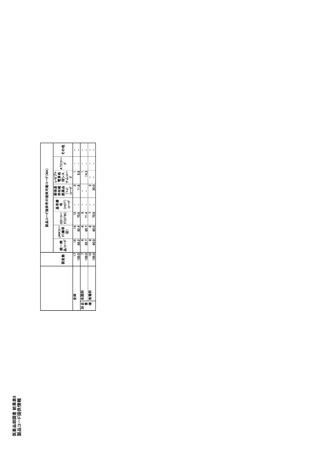
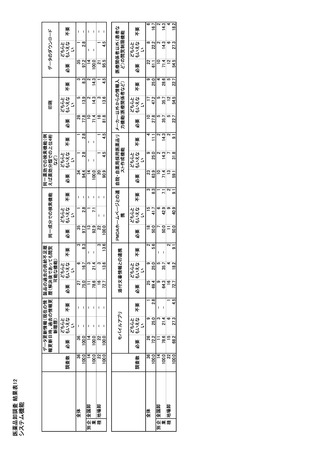
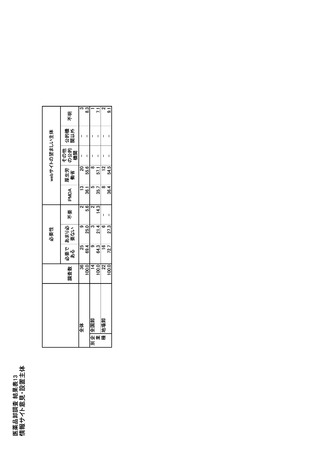
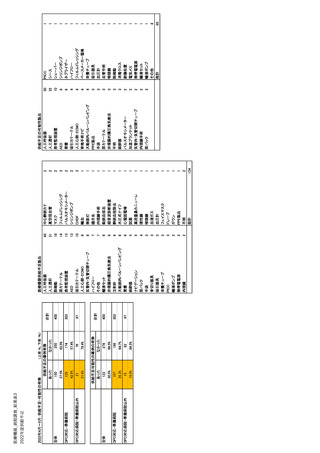
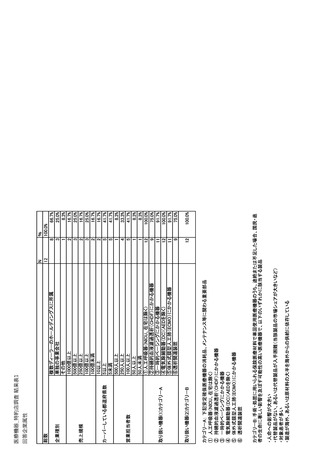
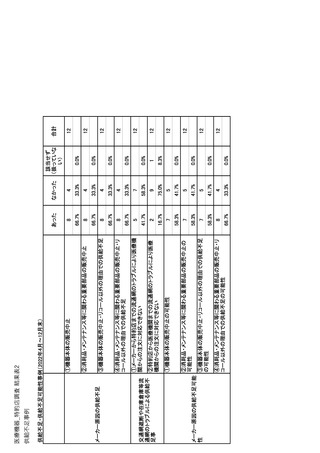
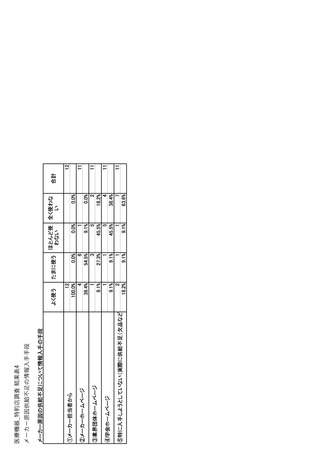
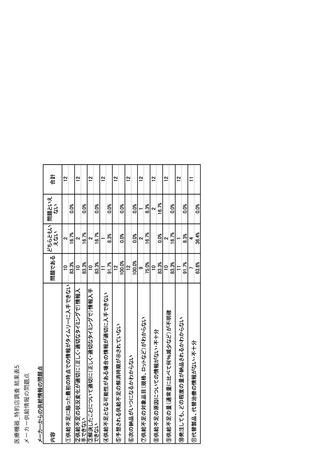
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
定がされていないか審査される。
識別番号(DIC:Drug Identification Number)が発行
先発医薬品は、カナダ保健省によって承認され
される。また、製造においても、食品医薬品規制
ると、その後カナダ医薬品・医療技術庁
(FDR)に規定される適正製造基準(GMP)に適合し
(CADTH:The Canadian Agency for Drugs and
なければならず、メーカーは NOC(Notice of
Technologies in Health)により、医療技術評価を受け
Compliance)及び医薬品識別番号の取得に加え、
る。カナダ医薬品・医療技術庁は審査プロセスを通
GMP 適合を証明する Establishment License を申請
じて、医薬品に関する臨床的、経済的といった客観
する必要がある。
的な評価を総合的に実施し、その医薬品が公的に
償還されるべきか、連邦、州(ケベック州を除く)、準
また、カナダは、医薬品に関する相互認証協定
州の公的な医薬品計画に勧告される 11)。ただし、ケ
(MRA)に加盟しており、GMP 適合証明書を実際の
ベック州においては国立衛生社会福祉研究所
検査に代えて共有することでより迅速に認可取得が
(INESSS)が医療技術評価を実施する。
可能である 7)。
汎カナダ製薬アライアンス (pCPA: pan-Canadian
Pharmaceutical Alliance)は、臨床的に効果的で手
(2) 医療用医薬品分類 8)
頃な価格の薬物治療へのアクセスを増加および管
カナダでは、食品医薬品法(FDA:Food and
理するために、さまざまな公的薬物計画イニシアチ
Drugs Act)第 2 条及び Natural Health Products
ブで協力する、州、準州、および連邦政府の同盟で
Regulations 第 1 条にある「天然健康製品」(NHP)
ある。汎カナダ製薬アライアンス(pCPA)は、カナダ
の定義に基づいて、医薬品、食品、器具、化粧品を
医薬品・医療技術庁もしくは国立衛生社会福祉研
分類している。各分類は以下の規則に基づいて管
究所の推奨事項及びその他の要因を基に、医薬品
理される。
の共同交渉について判断し、交渉成功後に契約条
・食品医薬品規則
件を設定する同意書を発行する。製品リスト契約が
・自然健康製品規則
結ばれると、公的医薬品計画の元、医薬品が公的
・医療機器規則(Medical Devices Regulations)
資金で支払われるようになる 12)。
・化粧品規則
医薬品の分類はさらに、天然健康製品(NHP)、
先発医薬品は、承認時期による分類とその分類
生物製剤、および医薬品と分類される。天然健康製
に応じて価格設定される。分類は以下の 4 つであ
品(NHP)は自然健康製品規則で管理され、医薬
る。
品、生物製剤は食品医薬品規則に基づいて管理さ
●Grandfathered 医薬品:2019 年 8 月 21 日以前
れる。さらに医薬品の中の分類には、処方箋医薬品
に医薬品識別番号(DIN)を取得したもの。
および非処方箋医薬品、消毒剤、消毒をうたった除
●Line Extensions 医薬品:2019 年 8 月 21 日以
降に医薬品識別番号(DIN)を取得した、
菌剤などが含まれる。
Grandfathered 医薬品の新剤形及び力価のも
の。
(3) 外来薬の価格設定(新薬)9), 10)
●Gap 医薬品:2019 年 8 月 21 日以降、2021
カナダでは、特許法及び特許薬品規則に基づき、
特許医薬品価格審査委員会(PMPRB:Patented
7 月 1 日以前に医薬品識別番号(DIN)を取得
Medicine Prices Review Board)により医薬品の価格
し、2021 年 7 月 1 日以前にカナダで最初に販
が調査・管理されている。新薬は、発売時から特許が
売されたもの。
●新薬:上記の分類以外の特許医薬品
満了するまで、年 2 回価格と販売情報を特許医薬品
価格審査委員会(PMPRB)に提出し、過剰な価格設
176