よむ、つかう、まなぶ。
2 先進医療Bに係る新規技術の科学的評価等について(別紙2)[3.7MB] (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00111.html |
| 出典情報 | 先進医療会議(第149回 12/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
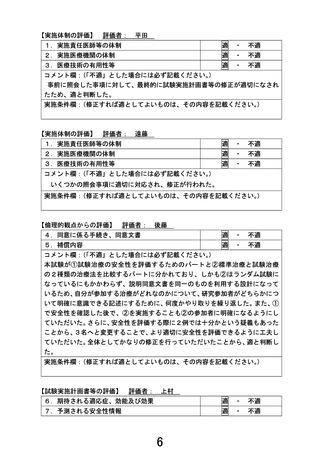
8.被験者の適格基準及び選定方法
適
・
不適
9.治療計画の内容
適
・
不適
10.有効性及び安全性の評価方法
適
・
不適
11.モニタリング体制及び実施方法
適
・
不適
12.被験者等に対して重大な事態が生じた場合の
対処方法
適
・
不適
13.試験に係る記録の取扱い及び管理・保存方法
適
・
不適
14.患者負担の内容
適
・
不適
15.起こりうる利害の衝突及び研究者等の関連組織
との関わり
適
・
不適
16.個人情報保護の方法
適
・
不適
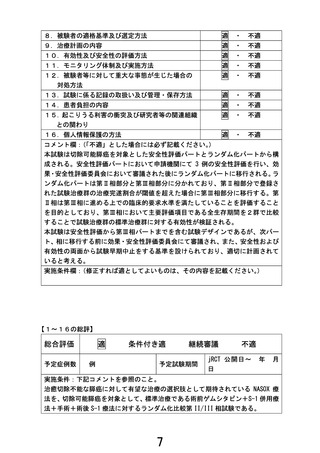
コメント欄:(「不適」とした場合には必ず記載ください。)
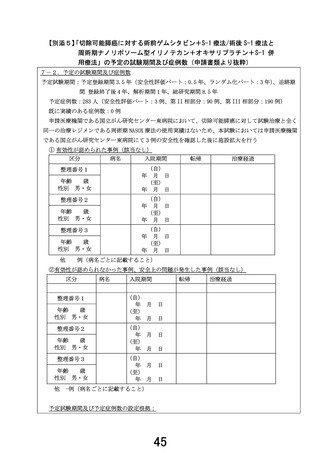
本試験は切除可能膵癌を対象とした安全性評価パートとランダム化パートから構
成される。安全性評価パートにおいて申請機関にて 3 例の安全性評価を行い、効
果・安全性評価委員会において審議された後にランダム化パートに移行される。ラ
ンダム化パートは第Ⅱ相部分と第Ⅲ相部分に分かれており、第Ⅱ相部分で登録さ
れた試験治療群の治療完遂割合が閾値を超えた場合に第Ⅲ相部分に移行する。第
Ⅱ相は第Ⅲ相に進める上での臨床的要求水準を満たしていることを評価すること
を目的としており、第Ⅲ相において主要評価項目である全生存期間を2群で比較
することで試験治療群の標準治療群に対する有効性が検証される。
本試験は安全性評価から第Ⅲ相パートまでを含む試験デザインであるが、次パー
ト、相に移行する前に効果・安全性評価委員会にて審議され、また、安全性および
有効性の両面から試験早期中止をする基準を設けられており、適切に計画されて
いると考える。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数
適
例
条件付き適
継続審議
予定試験期間
不適
jRCT 公開日~
日
年
月
実施条件:下記コメントを参照のこと。
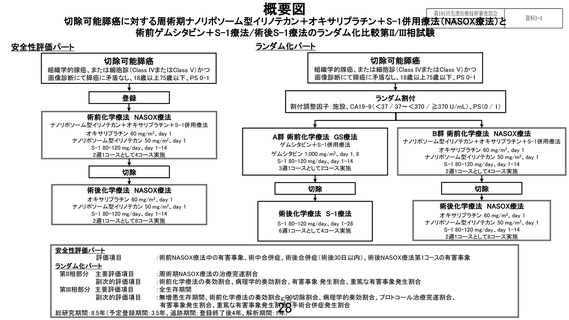
治癒切除不能な膵癌に対して有望な治療の選択肢として期待されている NASOX 療
法を、切除可能膵癌を対象として、標準治療である術前ゲムシタビン+S-1 併用療
法+手術+術後 S-1 療法に対するランダム化比較第 II/III 相試験である。
7
適
・
不適
9.治療計画の内容
適
・
不適
10.有効性及び安全性の評価方法
適
・
不適
11.モニタリング体制及び実施方法
適
・
不適
12.被験者等に対して重大な事態が生じた場合の
対処方法
適
・
不適
13.試験に係る記録の取扱い及び管理・保存方法
適
・
不適
14.患者負担の内容
適
・
不適
15.起こりうる利害の衝突及び研究者等の関連組織
との関わり
適
・
不適
16.個人情報保護の方法
適
・
不適
コメント欄:(「不適」とした場合には必ず記載ください。)
本試験は切除可能膵癌を対象とした安全性評価パートとランダム化パートから構
成される。安全性評価パートにおいて申請機関にて 3 例の安全性評価を行い、効
果・安全性評価委員会において審議された後にランダム化パートに移行される。ラ
ンダム化パートは第Ⅱ相部分と第Ⅲ相部分に分かれており、第Ⅱ相部分で登録さ
れた試験治療群の治療完遂割合が閾値を超えた場合に第Ⅲ相部分に移行する。第
Ⅱ相は第Ⅲ相に進める上での臨床的要求水準を満たしていることを評価すること
を目的としており、第Ⅲ相において主要評価項目である全生存期間を2群で比較
することで試験治療群の標準治療群に対する有効性が検証される。
本試験は安全性評価から第Ⅲ相パートまでを含む試験デザインであるが、次パー
ト、相に移行する前に効果・安全性評価委員会にて審議され、また、安全性および
有効性の両面から試験早期中止をする基準を設けられており、適切に計画されて
いると考える。
実施条件欄:(修正すれば適としてよいものは、その内容を記載ください。)
【1~16の総評】
総合評価
予定症例数
適
例
条件付き適
継続審議
予定試験期間
不適
jRCT 公開日~
日
年
月
実施条件:下記コメントを参照のこと。
治癒切除不能な膵癌に対して有望な治療の選択肢として期待されている NASOX 療
法を、切除可能膵癌を対象として、標準治療である術前ゲムシタビン+S-1 併用療
法+手術+術後 S-1 療法に対するランダム化比較第 II/III 相試験である。
7