よむ、つかう、まなぶ。
2 先進医療Bに係る新規技術の科学的評価等について(別紙2)[3.7MB] (43 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000205617_00111.html |
| 出典情報 | 先進医療会議(第149回 12/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
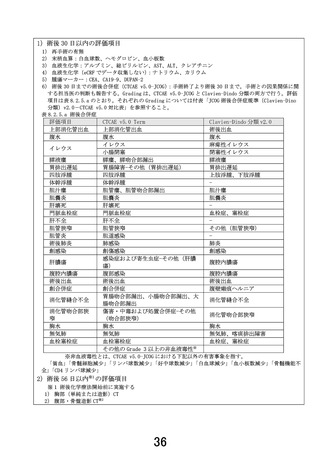
・ 性別(男性 / 女性)
・ 年齢(65 歳未満 / 65 歳以上 70 歳未満 / 70 歳以上)
・ PS(0 / 1)
・ 登録時 CA19-9(37 U/mL 未満 / 37 U/mL 以上 370 U/mL 未満 / 370 U/mL 以上)
・ 腫瘍主占居部位(膵頭部 / 膵体尾部)
・ 登録時 cT 因子(T1 / T2 / T3)
(UICC-TNM 第 8 版に従う)
・ 登録時 cN 因子(N0 / N1-N2)
(UICC-TNM 第 8 版に従う)
4)補足的解析の方法
主たる解析結果の頑健性を確認するために、必要に応じて以下の補足的解析を行う。
全登録例を対象とした解析
5)欠測データの扱い
欠測値に対する補完は、原則として行わない。組織学的効果判定が実施できない患者は分母に
のみ含める。ただし、データ確定前に、解析結果に重大な影響を与え得る欠測値が存在すること
が分かった場合には、統計解析計画書にその対処方法を記載する。
中間解析
中間解析の目的
試験の途中で本試験の主たる目的が達成されたかどうかを判断する目的で 2 回の中間解析を行
う。1 回目の中間解析は、第 III 相部分の登録中に登録を続けることが妥当かどうかを判断する
目的で、2 回目の中間解析は第 III 相部分の登録終了後早期に、予定した期間の追跡を続けるか
どうかを判断する目的で行う。いずれの場合も試験の主たる目的が達成されていると判断された
場合は試験を中止し、速やかに試験結果を学会および論文にて公表する。
中間解析の時期
1 回目の中間解析は、原則として第 III 相部分の予定登録数の半数の登録が得られた時点以降
に問い合わせを行う最初の定期モニタリングのデータを用いて行い、2 回目の中間解析は、第 III
相部分の登録が終了し、すべての登録患者のプロトコール治療が終了する時期を目途に、データ
センターと研究事務局で相談した上で適切と思われる時期の定期モニタリングに合わせて行う。
ただし、中間解析時点のイベント数が想定よりも極端に少ない場合は、少なくとも無効中止の検
討に必要なイベント数(20 イベントを目安とする)が観察されるまで中間解析の実施を延期す
る。
原則として 1 回目の中間解析中も登録は停止しない。
なお、試験進捗が予定どおりであった場合、
「12.7. 予定登録数・登録期間・追跡期間」に示す
前提の下での中間解析実施時の期待イベント数は、第 1 回中間解析が第 III 相部分の登録開始後
1.5 年時点、第 2 回中間解析が第 III 相部分の登録終了後 2 年時点で行われるとした場合、それ
ぞれ 18、134 となることが予想される。
中間解析における多重性の調整方法
中間解析はデータセンターが行う。試験全体のαエラーを片側 5%に保つために、中間解析と主
たる解析における検定の多重性を Lan & DeMets のα消費関数を用いて調整し、群間の primary
endpoint の差について統計学的有意性を調べる。α消費関数として、O’Brien & Fleming タイ
プ 49 を用いる。
中間解析における判断規準
本試験の中間解析結果に基づく判断規準は以下のとおりとする。
・ 「12.2.1. 1)主たる解析の方法」に示す方法により A 群に対する B 群の primary endpoint での優越性が
証明された場合、原則として試験を中止する(有効中止)
。
・ B 群の primary endpoint が A 群のそれを下回っている場合には、検定による判断を行わず、総合的に試
験早期中止の是非を検討することとする(無効中止)。
・ 上の 2 つのいずれにも該当しない場合、試験継続とする。
無効中止判断の参考情報
無効中止するか否かを判断するための参考情報として、以下を算出する。
・ Primary endpoint に関する予測確率(predictive probability:Spiegelhalter らの方法 50 に基づき研究
43
・ 年齢(65 歳未満 / 65 歳以上 70 歳未満 / 70 歳以上)
・ PS(0 / 1)
・ 登録時 CA19-9(37 U/mL 未満 / 37 U/mL 以上 370 U/mL 未満 / 370 U/mL 以上)
・ 腫瘍主占居部位(膵頭部 / 膵体尾部)
・ 登録時 cT 因子(T1 / T2 / T3)
(UICC-TNM 第 8 版に従う)
・ 登録時 cN 因子(N0 / N1-N2)
(UICC-TNM 第 8 版に従う)
4)補足的解析の方法
主たる解析結果の頑健性を確認するために、必要に応じて以下の補足的解析を行う。
全登録例を対象とした解析
5)欠測データの扱い
欠測値に対する補完は、原則として行わない。組織学的効果判定が実施できない患者は分母に
のみ含める。ただし、データ確定前に、解析結果に重大な影響を与え得る欠測値が存在すること
が分かった場合には、統計解析計画書にその対処方法を記載する。
中間解析
中間解析の目的
試験の途中で本試験の主たる目的が達成されたかどうかを判断する目的で 2 回の中間解析を行
う。1 回目の中間解析は、第 III 相部分の登録中に登録を続けることが妥当かどうかを判断する
目的で、2 回目の中間解析は第 III 相部分の登録終了後早期に、予定した期間の追跡を続けるか
どうかを判断する目的で行う。いずれの場合も試験の主たる目的が達成されていると判断された
場合は試験を中止し、速やかに試験結果を学会および論文にて公表する。
中間解析の時期
1 回目の中間解析は、原則として第 III 相部分の予定登録数の半数の登録が得られた時点以降
に問い合わせを行う最初の定期モニタリングのデータを用いて行い、2 回目の中間解析は、第 III
相部分の登録が終了し、すべての登録患者のプロトコール治療が終了する時期を目途に、データ
センターと研究事務局で相談した上で適切と思われる時期の定期モニタリングに合わせて行う。
ただし、中間解析時点のイベント数が想定よりも極端に少ない場合は、少なくとも無効中止の検
討に必要なイベント数(20 イベントを目安とする)が観察されるまで中間解析の実施を延期す
る。
原則として 1 回目の中間解析中も登録は停止しない。
なお、試験進捗が予定どおりであった場合、
「12.7. 予定登録数・登録期間・追跡期間」に示す
前提の下での中間解析実施時の期待イベント数は、第 1 回中間解析が第 III 相部分の登録開始後
1.5 年時点、第 2 回中間解析が第 III 相部分の登録終了後 2 年時点で行われるとした場合、それ
ぞれ 18、134 となることが予想される。
中間解析における多重性の調整方法
中間解析はデータセンターが行う。試験全体のαエラーを片側 5%に保つために、中間解析と主
たる解析における検定の多重性を Lan & DeMets のα消費関数を用いて調整し、群間の primary
endpoint の差について統計学的有意性を調べる。α消費関数として、O’Brien & Fleming タイ
プ 49 を用いる。
中間解析における判断規準
本試験の中間解析結果に基づく判断規準は以下のとおりとする。
・ 「12.2.1. 1)主たる解析の方法」に示す方法により A 群に対する B 群の primary endpoint での優越性が
証明された場合、原則として試験を中止する(有効中止)
。
・ B 群の primary endpoint が A 群のそれを下回っている場合には、検定による判断を行わず、総合的に試
験早期中止の是非を検討することとする(無効中止)。
・ 上の 2 つのいずれにも該当しない場合、試験継続とする。
無効中止判断の参考情報
無効中止するか否かを判断するための参考情報として、以下を算出する。
・ Primary endpoint に関する予測確率(predictive probability:Spiegelhalter らの方法 50 に基づき研究
43